Clear Sky Science · fr
La gamma‑aminobutyrique transaminase médie la suppression tumorale dans le carcinome rénal via l’axe cGAS‑STING–interféron‑β
Transformer un neurotransmetteur en faiblesse du cancer
Le cancer du rein, en particulier sa forme la plus fréquente appelée carcinome à cellules rénales à claires, est notoirement difficile à traiter une fois qu’il se propage, résistant souvent à la chimiothérapie et à la radiothérapie. Cette étude révèle qu’une enzyme négligée, mieux connue en neurochimie — la gamma‑aminobutyrique transaminase, ou ABAT — peut agir comme une alliée cachée contre les tumeurs rénales. En augmentant cette enzyme à l’intérieur des cellules cancéreuses, les chercheurs ont pu réveiller un puissant système d’alerte immunitaire intrinsèque qui ralentit la croissance tumorale et reconfigure le microenvironnement immunitaire de la tumeur.
Un défenseur absent dans les tumeurs rénales
L’équipe a commencé par examiner de larges bases de données patientes et des échantillons tumoraux pour observer le comportement d’ABAT dans le cancer du rein. Dans les tissus sains, ABAT participe à la dégradation du messager calmant GABA, maintenant ses niveaux en équilibre. Dans les échantillons tumoraux, cependant, les niveaux d’ABAT étaient systématiquement beaucoup plus faibles que dans le tissu rénal normal adjacent, et les patients présentant les quantités les plus faibles d’ABAT avaient tendance à avoir un pronostic moins favorable. Ce schéma suggérait que les tumeurs pourraient réprimer ABAT pour gagner un avantage. 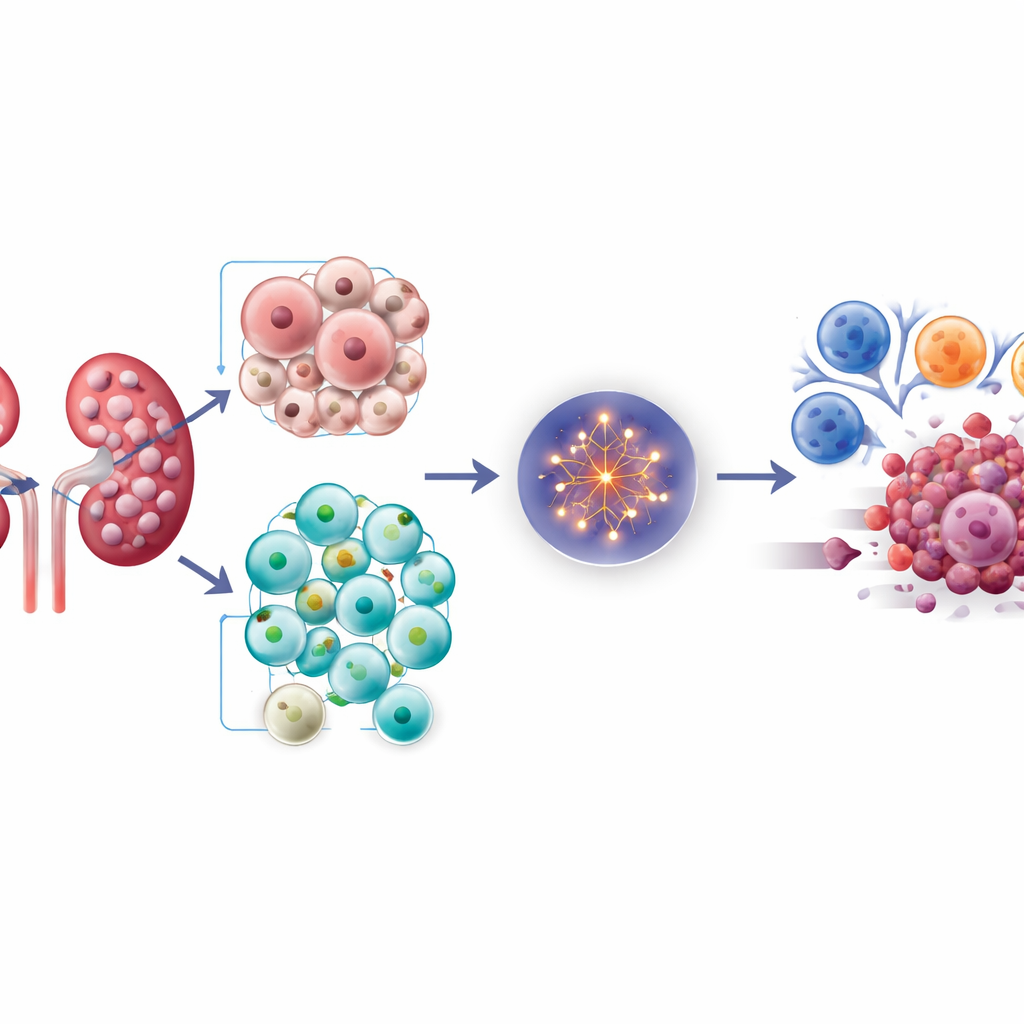
Réveiller l’alarme anti‑intrus de la cellule
Pour comprendre comment une enzyme métabolique pouvait avoir un effet antitumoral aussi marqué, les chercheurs ont comparé l’activité génique dans des cellules cancéreuses avec et sans surexpression d’ABAT. Ils ont observé une augmentation notable des gènes généralement activés par les signaux de défense antivirale, en particulier ceux contrôlés par une molécule appelée interféron‑β. Cela indiquait l’activation d’une « alarme » immunitaire innée normalement utilisée pour détecter des virus ou des dommages à l’ADN. En utilisant des médicaments sélectifs bloquant différentes voies de détection, ils ont retracé l’effet jusqu’à la voie cGAS‑STING — un système cellulaire qui répond lorsque de l’ADN apparaît au mauvais endroit à l’intérieur de la cellule. Lorsque cette voie fut chimiquement inhibée, ABAT ne put plus induire des niveaux élevés d’interféron‑β ni supprimer efficacement les tumeurs, montrant que son pouvoir anti‑cancer dépend de ce système d’alarme interne.
Stress à l’intérieur des centrales énergétiques cellulaires
ABAT se situe habituellement dans les mitochondries, les centrales énergétiques de la cellule. Les auteurs ont découvert qu’augmenter les niveaux d’ABAT perturbe la santé mitochondriale : le potentiel de membrane qui les alimente diminuait, leurs formes devenaient anormales à la microscopie électronique, et des fragments d’ADN mitochondrial fuyaient dans le fluide intracellulaire. Ces bouts d’ADN échappés sont précisément le type de signal qui active cGAS‑STING. L’équipe a aussi constaté qu’ABAT se lie à une autre enzyme, PRMT5, qui a été liée à la croissance tumorale et à l’atténuation des signaux d’alerte immunitaires. Lorsque PRMT5 fut réduit, l’activité de STING et d’interféron‑β augmenta, suggérant qu’ABAT pourrait à la fois endommager les mitochondries et contrebalancer PRMT5 pour lever les freins sur la voie d’alarme, bien que les détails fins restent à élucider. 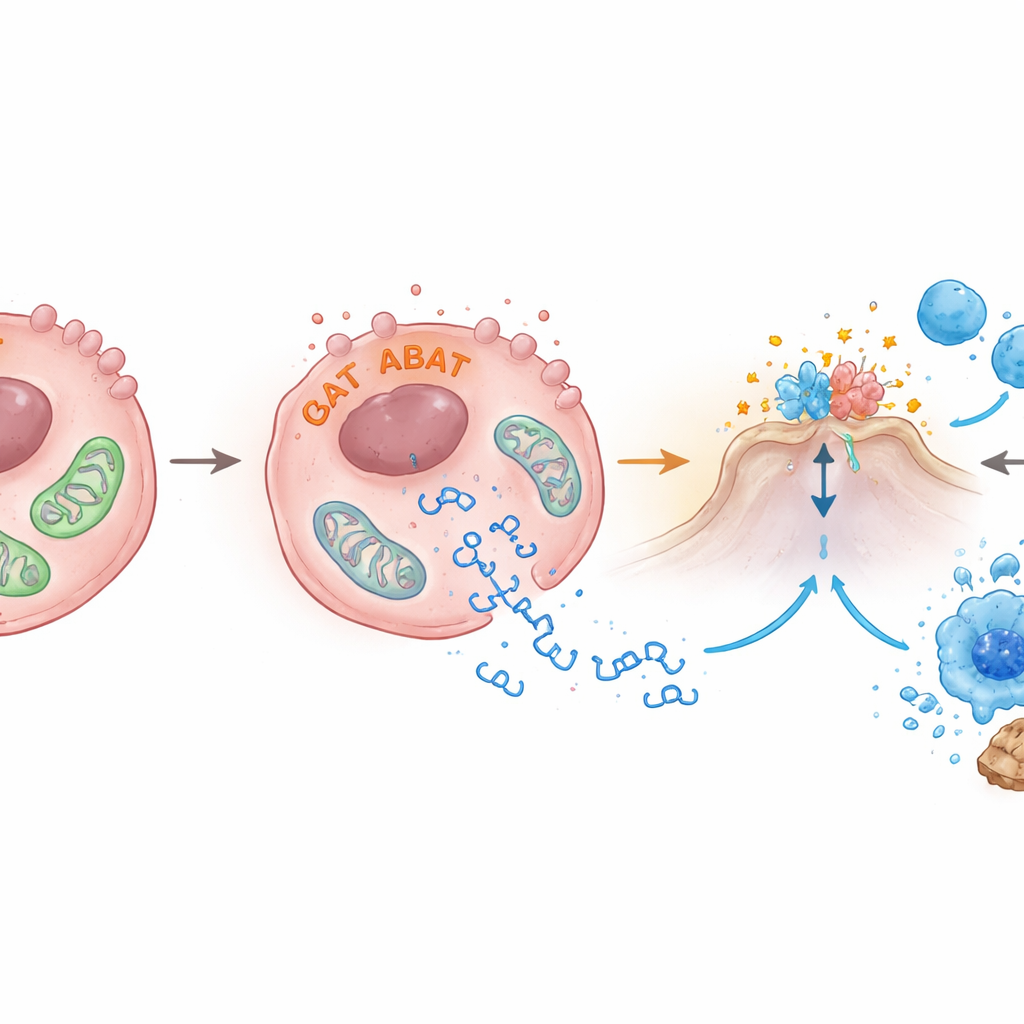
Modifier l’équilibre immunitaire autour de la tumeur
Le cancer ne croît pas isolément ; il vit dans un voisinage complexe de cellules immunitaires qui peuvent soit l’attaquer soit le protéger. Chez des souris immunocompétentes, les tumeurs issues de cellules de cancer rénal riches en ABAT non seulement croissaient plus lentement mais présentaient également une composition immunitaire différente. La proportion de cellules T régulatrices — des cellules immunitaires qui calment normalement les réponses et sont souvent détournées par les tumeurs pour se protéger — était sensiblement plus faible, tandis que l’équilibre penchait en faveur des lymphocytes T cytotoxiques. Cela suggère qu’ABAT, en déclenchant des signaux d’interféron et de dommage, peut faire basculer le microenvironnement local loin de l’immunosuppression et vers une activité anti‑tumorale, potentiellement en rendant d’autres traitements comme les inhibiteurs de points de contrôle plus efficaces.
Ce que cela pourrait signifier pour les traitements futurs
Au total, l’étude dépeint ABAT comme plus qu’une enzyme d’entretien métabolique : dans le cancer du rein, elle se comporte comme un suppresseur tumoral intrinsèque qui, une fois restaurée, inflige un stress aux centrales énergétiques des cellules cancéreuses, libère des signaux de danger et déclenche une alarme interne qui appelle le système immunitaire à l’action. Étant donné qu’ABAT est fréquemment réduite dans les tumeurs de patients, des stratégies visant à augmenter son activité — ou à imiter les effets mitochondriaux et activateurs immunitaires qu’elle provoque — pourraient ouvrir de nouvelles voies thérapeutiques pour le cancer du rein avancé, notamment en combinaison avec les immunothérapies et traitements ciblés existants.
Citation: Feng, Y., Cao, S., Cai, T. et al. Gamma-aminobutyric acid transaminase mediates tumor suppression in renal cell carcinoma through the cGAS-STING–interferon-β axis. Sci Rep 16, 13082 (2026). https://doi.org/10.1038/s41598-026-42861-w
Mots-clés: cancer du rein, immunité innée, microenvironnement tumoral, mitochondries, signalisation de l’interféron