Clear Sky Science · es
La transaminasa del ácido gamma-aminobutírico media la supresión tumoral en el carcinoma de células renales a través del eje cGAS-STING–interferón-β
Convertir un químico nervioso en una debilidad del cáncer
El cáncer de riñón, en especial su forma más común llamada carcinoma de células renales de tipo claro, es notoriamente difícil de tratar una vez que se disemina, resistiendo a menudo tanto la quimioterapia como la radiación. Este estudio revela que una enzima pasada por alto, conocida principalmente por su papel en la química cerebral —la transaminasa del ácido gamma-aminobutírico, o ABAT— puede actuar como un aliado oculto contra los tumores renales. Al aumentar esta enzima dentro de las células cancerosas, los investigadores consiguieron activar un potente sistema de alarma inmune incorporado que frena el crecimiento tumoral y remodela el entorno inmune del tumor.
Un defensor ausente en los tumores renales
El equipo comenzó examinando grandes bases de datos de pacientes y muestras tumorales para ver cómo se comporta ABAT en el cáncer de riñón. En el tejido sano, ABAT ayuda a descomponer el mensajero cerebral calmante GABA, manteniendo sus niveles en equilibrio. Sin embargo, en las muestras tumorales, los niveles de ABAT eran consistentemente mucho más bajos que en el tejido renal normal adyacente, y los pacientes con las cantidades más bajas de ABAT tendían a tener peor pronóstico. Este patrón sugirió que los tumores podrían silenciar ABAT para obtener una ventaja. 
Despertando la alarma de intrusos de la célula
Para entender cómo una enzima metabólica podía tener un efecto antitumoral tan potente, los investigadores compararon la actividad génica en células cancerosas con y sin ABAT adicional. Encontraron un aumento llamativo en genes habitualmente activados por señales de defensa antiviral, especialmente aquellos controlados por una molécula llamada interferón-β. Esto apuntó a la activación de una «alarma de intrusos» innata normalmente usada para detectar virus o daño en el ADN. Mediante fármacos selectivos que bloquean diferentes rutas sensoriales, rastrearon el efecto hasta la vía cGAS-STING: un sistema celular que responde cuando el ADN aparece en un lugar inadecuado dentro de la célula. Cuando esta vía se inhibió químicamente, ABAT ya no pudo elevar los niveles de interferón-β ni suprimir los tumores tan eficazmente, lo que demuestra que su poder antitumoral depende de este sistema de alarma interna.
Estrés dentro de las centrales energéticas de la célula
ABAT suele localizarse dentro de las mitocondrias, las fábricas de energía celular. Los autores descubrieron que aumentar los niveles de ABAT altera la salud mitocondrial: el potencial de membrana que las impulsa disminuyó, sus formas se volvieron anormales bajo microscopía electrónica y fragmentos de ADN mitocondrial se filtraron al fluido circundante dentro de la célula. Estos fragmentos de ADN escapados son precisamente el tipo de señal que activa cGAS-STING. El equipo también encontró que ABAT se une a otra enzima, PRMT5, que se ha relacionado con el crecimiento tumoral y con la supresión de las alarmas inmunes. Cuando PRMT5 se redujo, la actividad de STING e interferón-β aumentó, lo que sugiere que ABAT puede tanto dañar las mitocondrias como contrarrestar a PRMT5 para levantar los frenos sobre la vía de alarma, aunque los detalles finos siguen por dilucidar. 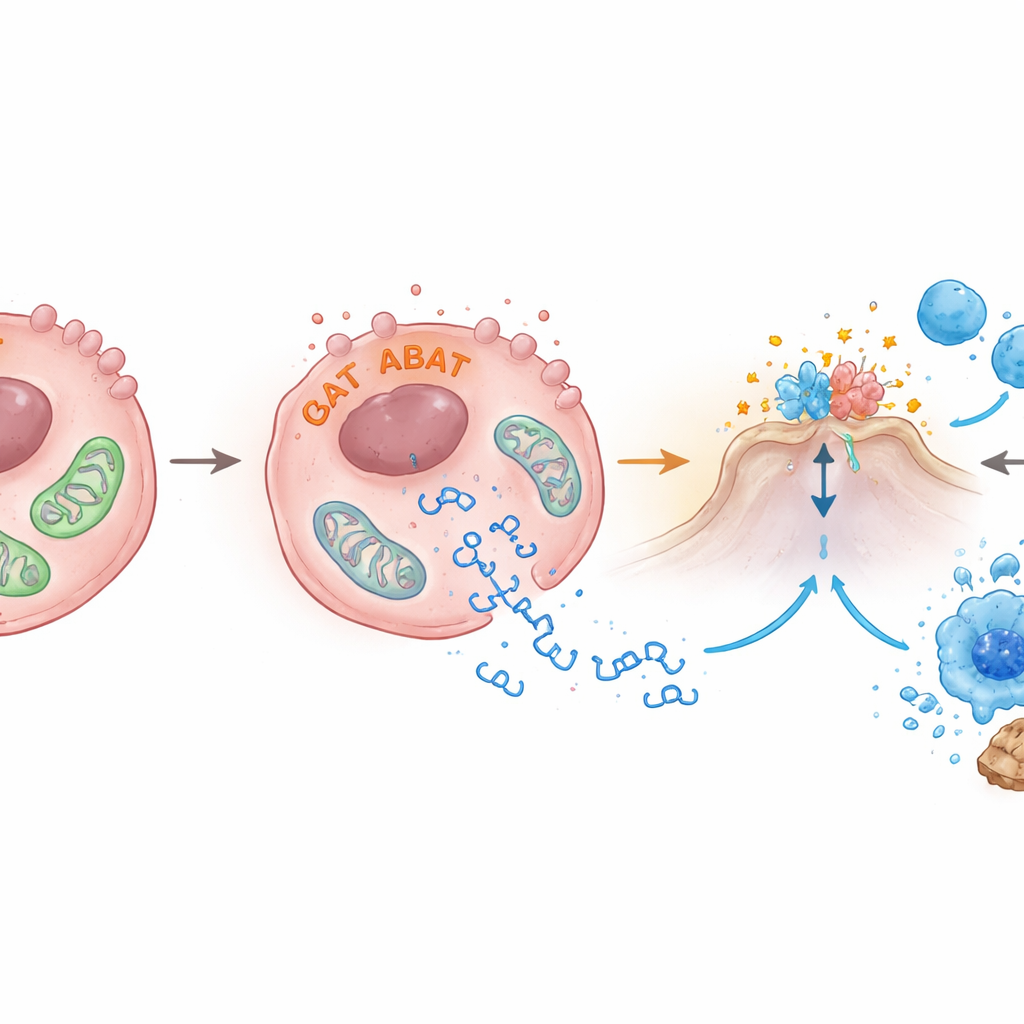
Trasladando el equilibrio inmunitario alrededor del tumor
El cáncer no crece aisladamente; vive dentro de un vecindario complicado de células inmunitarias que pueden atacarlo o protegerlo. En ratones con sistema inmune competente, los tumores formados por células de cáncer renal ricas en ABAT no solo crecieron más lentamente, sino que también mostraron una composición inmune diferente. La proporción de células T reguladoras —células inmunes que normalmente apagan las respuestas y que a menudo son cooptadas por los tumores para protegerse— fue notablemente menor, mientras que el equilibrio se desplazó a favor de las células T citotóxicas. Esto sugiere que ABAT, al desencadenar señales de interferón y daño, puede inclinar el entorno inmune local lejos de la supresión y hacia la actividad antitumoral, lo que potencialmente hace que otros tratamientos, como los inhibidores de puntos de control, sean más eficaces.
Qué podría significar esto para tratamientos futuros
En conjunto, el estudio presenta a ABAT como algo más que una enzima de mantenimiento metabólico: en el cáncer de riñón se comporta como un supresor tumoral incorporado que, cuando se restaura, inflige estrés en las centrales energéticas de las células cancerosas, libera señales de peligro y activa una alarma interna que convoca al sistema inmune. Dado que ABAT suele estar reducido en los tumores de pacientes, las estrategias que potencien su actividad —o que imiten los efectos mitocondriales y activadores inmunes que provoca— podrían abrir nuevas vías terapéuticas para el cáncer renal avanzado, especialmente en combinación con las terapias dirigidas e inmunoterapias existentes.
Cita: Feng, Y., Cao, S., Cai, T. et al. Gamma-aminobutyric acid transaminase mediates tumor suppression in renal cell carcinoma through the cGAS-STING–interferon-β axis. Sci Rep 16, 13082 (2026). https://doi.org/10.1038/s41598-026-42861-w
Palabras clave: cáncer de riñón, inmunidad innata, microambiente tumoral, mitocondrias, señalización de interferón