Clear Sky Science · zh
使用 CAS 核糖核蛋白复合体在莫桑比克罗非鱼细胞系中实现高效基因组编辑
这项研究对鱼类与粮食安全的意义
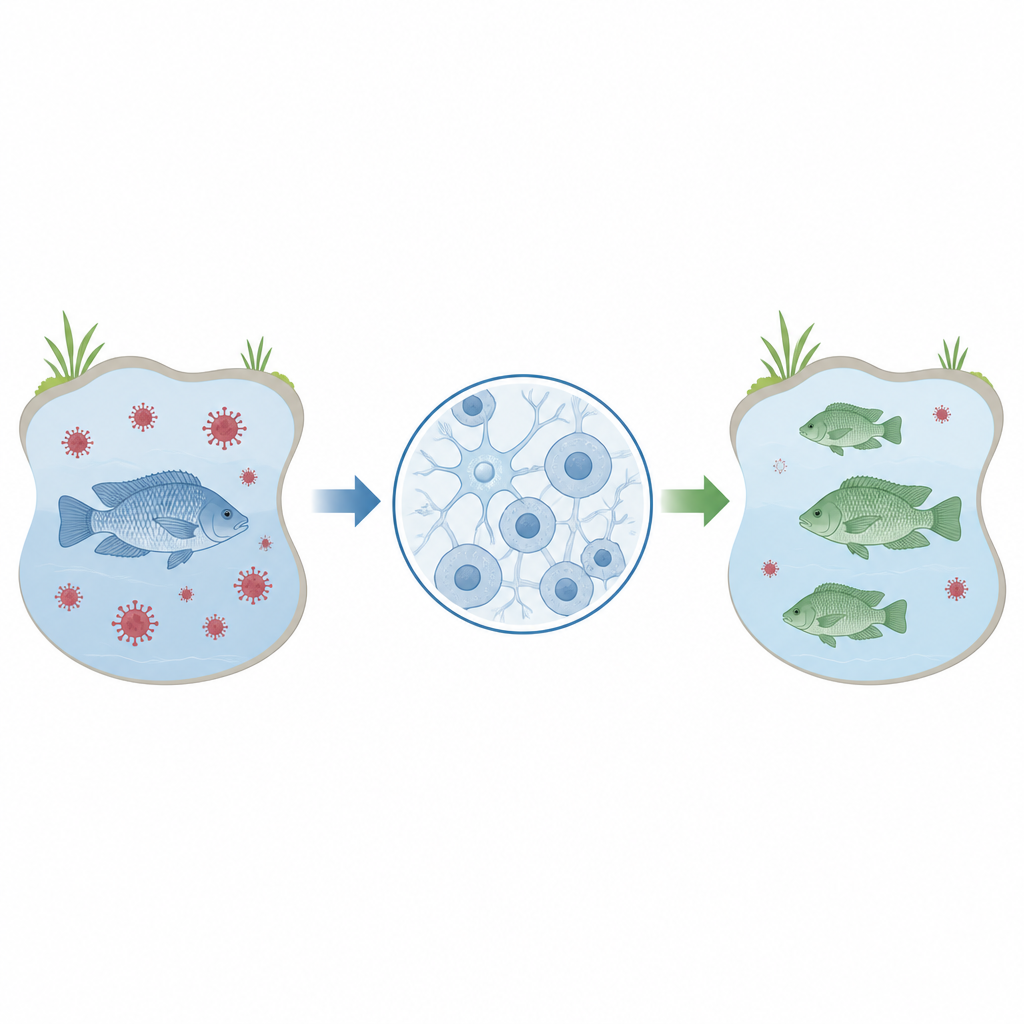
罗非鱼是世界各地餐桌上的主食性鱼类,尤其在那些急需廉价、高质量蛋白的地区。然 而,罗非鱼养殖场易受到诸如罗非鱼湖病毒等病毒性疾病的侵袭,这些疾病可毁灭鱼群并威胁生计。本研究描述了一种实验室方法,可在脑细胞中快速且精确地编辑罗非鱼基因,为今后培育更能抵抗疾病、支持全球粮食安全的鱼种奠定了基础。
处于粮食安全前线的鱼类
水产养殖已提供了全球约六分之一的动物蛋白,而罗非鱼是最容易、最常见的养殖对象之一。它们生长快、耐密集养殖且通常比较健壮。然而,传统的选择性育种在改善生长和抗病能力等性状方面速度缓慢,且受限于原有种群的自然变异。基因组编辑提供了一种在单代中引入有用遗传改变的方法,这对于提高养殖鱼类对严重病毒感染等性状的抵抗力尤其有价值。
构建有用的细胞模型
研究人员聚焦于一种名为 OmB 的细胞系,该细胞系来源于莫桑比克罗非鱼的大脑。这些细胞已知可被罗非鱼湖病毒感染,使其成为研究病毒与宿主相互作用的实用模型。在能广泛用于测试哪些基因影响感染或抗性之前,科学家需要一种可靠且高效的方式,在这些细胞中精确修改特定基因并测量后果。本研究旨在微调一个逐步的实验流程,使用一种流行的基因编辑工具 CRISPR 来实现这一目标。
优化编辑工具
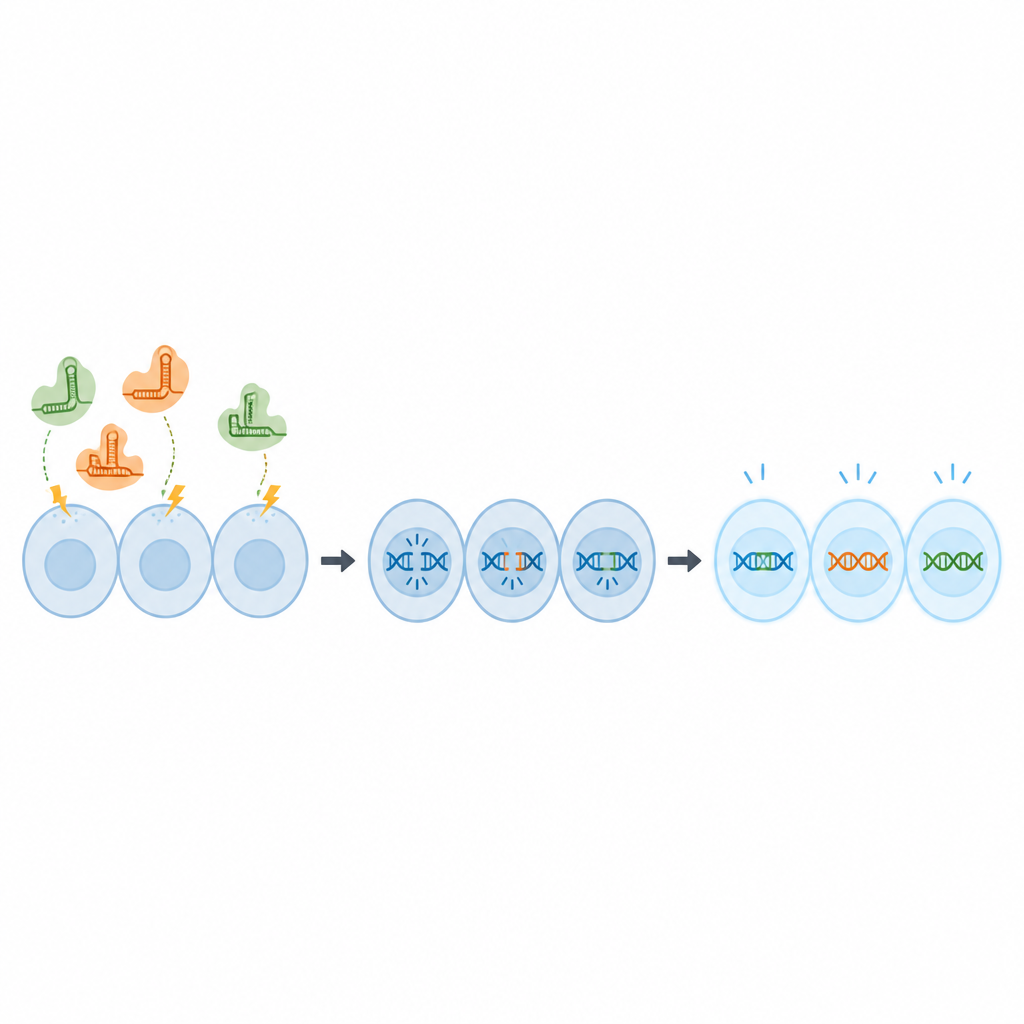
研究团队没有以 DNA 形式输送 CRISPR 组分(这种方式可能在细胞内滞留并带来安全顾虑),而是使用预制的蛋白-RNA 复合体,即核糖核蛋白(RNP)。通过一种称为电穿孔的技术,利用短促的电脉冲将这些复合体推入 OmB 细胞。首先,科学家用一种荧光示踪分子测试不同的电压、脉冲时长和浓度组合,以寻找能将示踪剂输送到几乎所有细胞且不损害细胞存活率的条件。他们发现示踪剂浓度为 2 微摩尔并配合特定脉冲设置时,几乎可实现完全摄取且细胞保持健康。
验证并证明方法可行
接着,团队考察这些条件是否真正能改变基因。他们使用了一个会发绿光的 OmB 细胞系版本,并设计 CRISPR 分子去切割编码绿色荧光蛋白的基因。在优化的电穿孔设置下,近 80% 的基因拷贝被编辑,两周后仅有少数细胞仍发绿光,表明该基因已被有效关闭。随后,科学家转向了两个普通的罗非鱼基因,选择它们是因为改变这些基因不会致死,同时能提供清晰的读出。使用相同的方案,他们取得了约 67% 到 70% 的编辑率,并预测基因功能被强烈敲除。
对未来鱼类健康的意义
该研究提供了一套适用于广泛使用的罗非鱼脑细胞系的高效基因编辑实用流程。通过证明 CRISPR 组分可安全递送,并且标记基因与原生基因都能在大多数细胞中被破坏,这项工作将 OmB 细胞转变为一个强大的测试平台。研究人员现在可以更容易地打开或关闭候选基因,以观察它们如何影响病毒感染、应激反应或其他性状。虽然本研究尚未直接培育出抗病鱼种,但它提供了一个关键工具,能帮助科学家识别最有可能增强养殖罗非鱼韧性的遗传改动。
引用: Wang, J., Bobrik, M., Pankaew, N. et al. Efficient genome editing in a Mozambique tilapia cell line using CAS ribonucleoprotein complexes. Sci Rep 16, 15125 (2026). https://doi.org/10.1038/s41598-026-42702-w
关键词: 罗非鱼, 水产养殖, CRISPR, 鱼类疾病, 基因组编辑