Clear Sky Science · sv
Effektiv genomredigering i en cellinje från Mozambique-tilapia med CAS-ribonukleoproteinkomplex
Varför denna studie är viktig för fisk och livsmedel
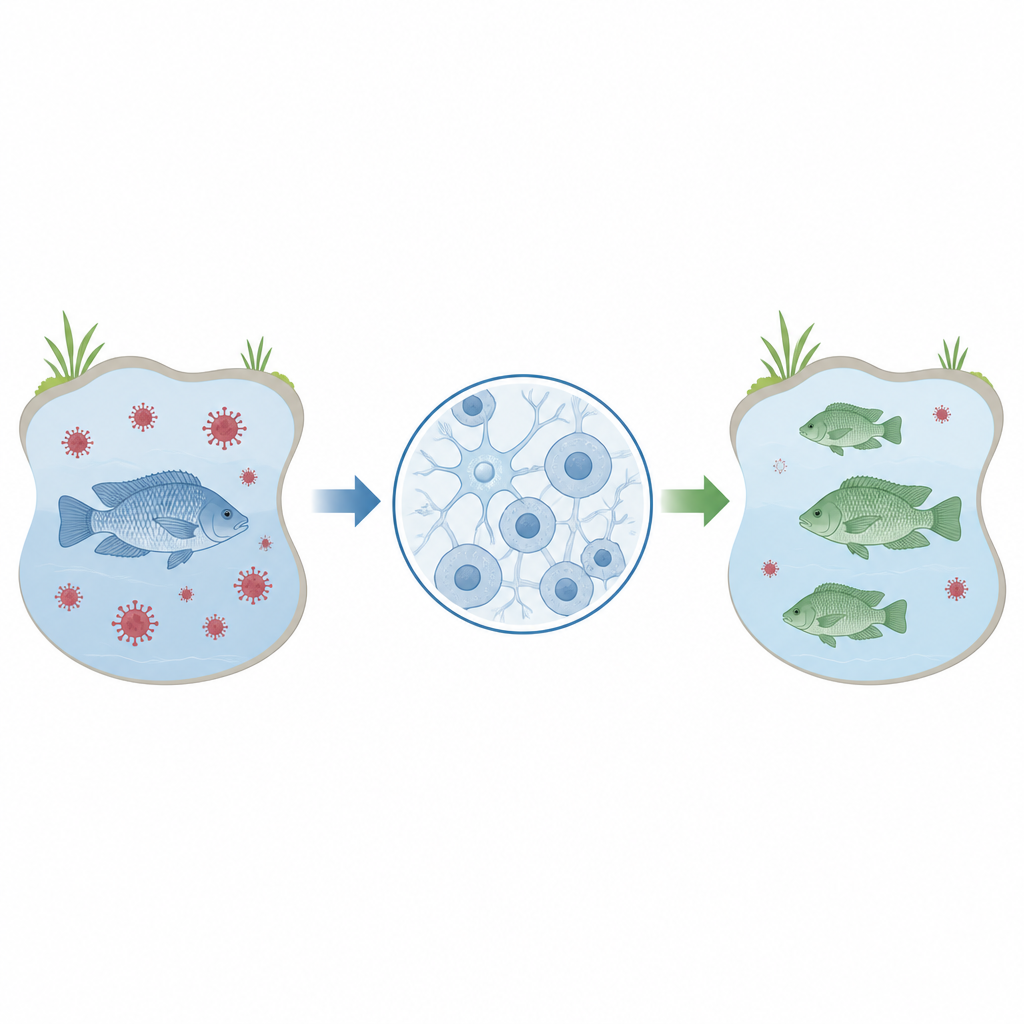
Tilapia är en basfisk på middagsbord runt om i världen, särskilt i områden där prisvärda, högkvalitativa proteiner är starkt efterfrågade. Ändå är tilapiaodlingar sårbara för virussjukdomar som Tilapia lake virus, vilket kan utplåna bestånd och hota försörjningen. Denna studie beskriver en laboratoriebaserad metod för att snabbt och precist redigera tilapiagener i hjärnceller, vilket lägger grunden för framtida arbete med att föda upp fiskar som bättre kan motstå sjukdom och stötta global livsmedelssäkerhet.
Fisk i frontlinjen för livsmedelssäkerhet
Akvakultur står redan för omkring en sjättedel av det animaliska proteinet som konsumeras globalt, och tilapia är bland de enklaste och vanligaste fiskarna att odla. De växer snabbt, tolererar trånga dammar och är generellt tåliga. Traditionell selektiv avel för att förbättra egenskaper som tillväxt och sjukdomsresistens är dock långsam och begränsad av den naturliga variation som finns i ett bestånd. Genomredigering erbjuder ett sätt att införa användbara genetiska förändringar på en generation, vilket kan vara särskilt värdefullt för egenskaper som motståndskraft mot allvarliga virusinfektioner i odlade fiskar.
Att bygga en användbar cellmodell
Forskarlaget fokuserade på en cellinje kallad OmB, härledd från hjärnan hos Mozambique-tilapia. Dessa celler är kända för att kunna infekteras av Tilapia lake virus, vilket gör dem till en praktisk modell för att studera hur viruset interagerar med sin värd. Innan sådana celler kan användas i stor utsträckning för att testa vilka gener som påverkar infektion eller motståndskraft behöver forskare ett tillförlitligt, effektivt sätt att ändra specifika gener i dessa celler och sedan mäta vad som händer. Denna studie syftade till att finslipa ett steg-för-steg-protokoll för att göra just det med ett populärt verktyg för genredigering känt som CRISPR.
Finslipning av redigeringsverktyget
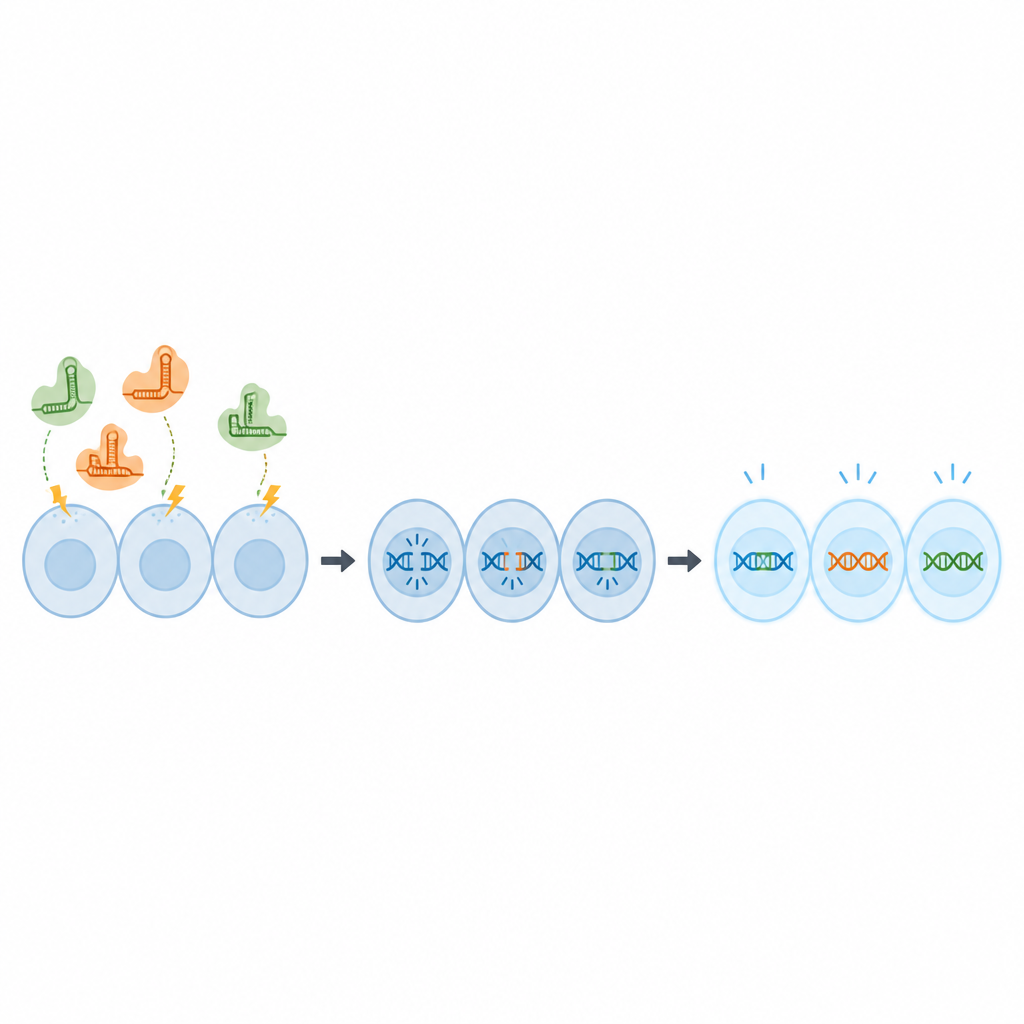
I stället för att leverera CRISPR-komponenter som DNA, vilket kan bestå kvar i celler och väcka säkerhetsfrågor, använde teamet färdiga protein–RNA-komplex som kallas ribonukleoproteiner. Dessa fördes in i OmB-celler med korta elektriska pulser i en teknik som kallas elektroporering. Först använde forskarna en fluorescerande spårmolekyl för att testa olika kombinationer av spänning, pulslängd och koncentration, för att hitta villkor som förde in spåraren i nästan alla celler utan att skada deras överlevnad. De fann att en koncentration på 2 mikromolar spårare och en specifik pulsinställning gav nästan full upptagning med friska celler.
Testa och bevisa metoden
Nästa fråga var om dessa villkor faktiskt kunde förändra gener. De använde en version av OmB-cellinjen som lyser grönt och designade CRISPR-molekyler för att klippa genen för det gröna proteinet. Under de optimerade elektriska inställningarna redigerades nära 80 procent av genkopiorna, och två veckor senare lystes bara en liten del av cellerna fortfarande, vilket visar att genen effektivt hade stängts av. Forskarlaget gick sedan vidare till två normala tilapiagener, valda eftersom förändring av dem inte dödar cellerna men ger ett tydligt utfall. Med samma protokoll uppnåddes redigeringsnivåer på omkring 67 till 70 procent och en stark förutsägbar knockout av genfunktionen.
Vad detta betyder för framtida fiskhälsa
Arbetet levererar ett praktiskt recept för genredigering med hög effektivitet i en allmänt använd tilapia-hjärncellinje. Genom att visa att CRISPR-komponenter kan levereras säkert och att både markör- och inhemska gener kan störas i de flesta celler, förvandlar studien OmB-celler till en kraftfull testbädd. Forskare kan nu enklare slå av och på kandidatgener för att se hur de påverkar virusinfektion, stressresponser eller andra egenskaper. Även om denna studie ännu inte skapade sjukdomsresistenta fiskar, tillhandahåller den ett nyckelverktyg som hjälper forskare att identifiera de genetiska förändringar som mest sannolikt gör uppfödd tilapia mer motståndskraftig i framtiden.
Citering: Wang, J., Bobrik, M., Pankaew, N. et al. Efficient genome editing in a Mozambique tilapia cell line using CAS ribonucleoprotein complexes. Sci Rep 16, 15125 (2026). https://doi.org/10.1038/s41598-026-42702-w
Nyckelord: tilapia, akvakultur, CRISPR, fisk-sjukdom, genomredigering