Clear Sky Science · pt
Edição genômica eficiente em uma linhagem celular de tilápia de Moçambique usando complexos ribonucleoproteicos CAS
Por que este estudo importa para peixes e para a alimentação
A tilápia é um peixe presente nas mesas ao redor do mundo, especialmente em regiões onde proteína de alta qualidade e acessível é urgentemente necessária. Ainda assim, os criadouros de tilápia são vulneráveis a doenças virais, como o Tilapia lake virus, que podem dizimar estoques e ameaçar meios de subsistência. Este estudo descreve um método em laboratório para editar genes de tilápia em células cerebrais de forma rápida e precisa, lançando as bases para trabalhos futuros voltados a criar peixes que suportem melhor doenças e contribuam para a segurança alimentar global.
Peixes na linha de frente da segurança alimentar
A aquicultura já fornece cerca de um sexto da proteína animal consumida globalmente, e a tilápia está entre os peixes mais fáceis e comuns de cultivar. Eles crescem rápido, toleram viveiros lotados e são, em geral, resistentes. Porém, o melhoramento seletivo tradicional para aprimorar características como crescimento e resistência a doenças é lento e limitado pela variação natural presente em um estoque. A edição do genoma oferece uma forma de introduzir alterações genéticas úteis em uma única geração, o que pode ser especialmente valioso para traços como resistência a infecções virais graves em peixes de criação.
Construindo um modelo celular útil
Os pesquisadores concentraram-se em uma linhagem celular chamada OmB, derivada do cérebro da tilápia de Moçambique. Sabe-se que essas células são infectadas pelo Tilapia lake virus, o que as torna um substituto prático para estudar como o vírus interage com seu hospedeiro. Antes que essas células possam ser amplamente usadas para testar quais genes afetam a infecção ou a resistência, os cientistas precisam de uma forma confiável e eficiente de alterar genes específicos nessas células e, em seguida, medir o que acontece. Este estudo buscou aperfeiçoar um protocolo passo a passo para fazer exatamente isso usando uma ferramenta de edição genética popular conhecida como CRISPR.
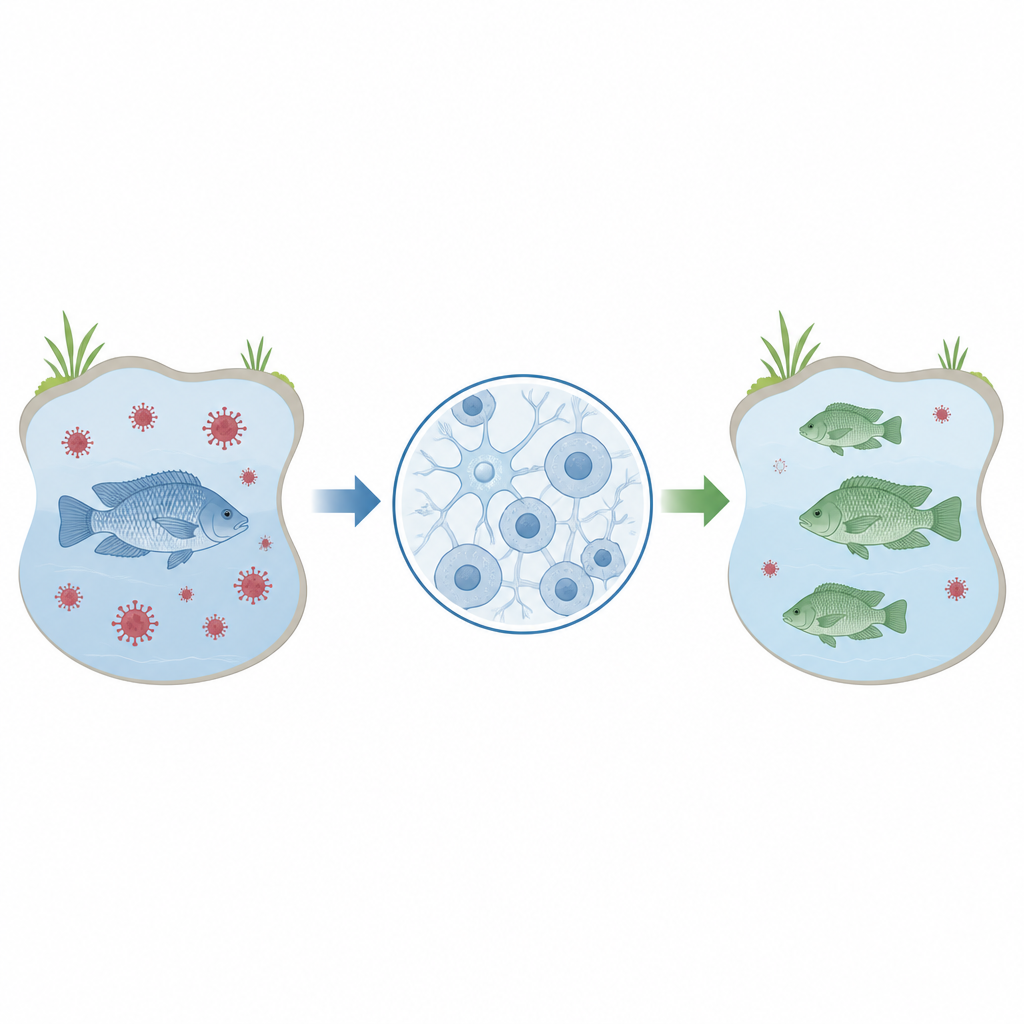
Ajustando finamente a ferramenta de edição
Em vez de entregar componentes CRISPR como DNA, que pode persistir nas células e levantar preocupações de segurança, a equipe usou complexos prontos de proteína e RNA conhecidos como ribonucleoproteínas. Estes foram introduzidos nas células OmB por meio de curtos pulsos elétricos em uma técnica chamada eletroporação. Primeiro, os cientistas usaram uma molécula traçadora fluorescente para testar diferentes combinações de voltagem, duração do pulso e concentração, buscando condições que levassem o traçador para quase todas as células sem prejudicar sua sobrevivência. Eles descobriram que uma concentração de 2 micromolar do traçador e uma configuração específica de pulso proporcionaram captação quase completa com células saudáveis.
Testando e comprovando o método
Em seguida, a equipe investigou se essas condições podiam realmente alterar genes. Eles usaram uma versão da linhagem OmB que brilha em verde e projetaram moléculas CRISPR para cortar o gene da proteína verde. Sob as configurações elétricas otimizadas, quase 80 por cento das cópias do gene foram editadas, e duas semanas depois apenas uma pequena fração das células ainda brilhava, mostrando que o gene havia sido efetivamente desligado. Os cientistas então passaram a dois genes nativos da tilápia, escolhidos porque alterá-los não mata as células, mas fornece uma leitura clara. Usando o mesmo protocolo, obtiveram taxas de edição em torno de 67 a 70 por cento e forte previsão de nocaute da função gênica.
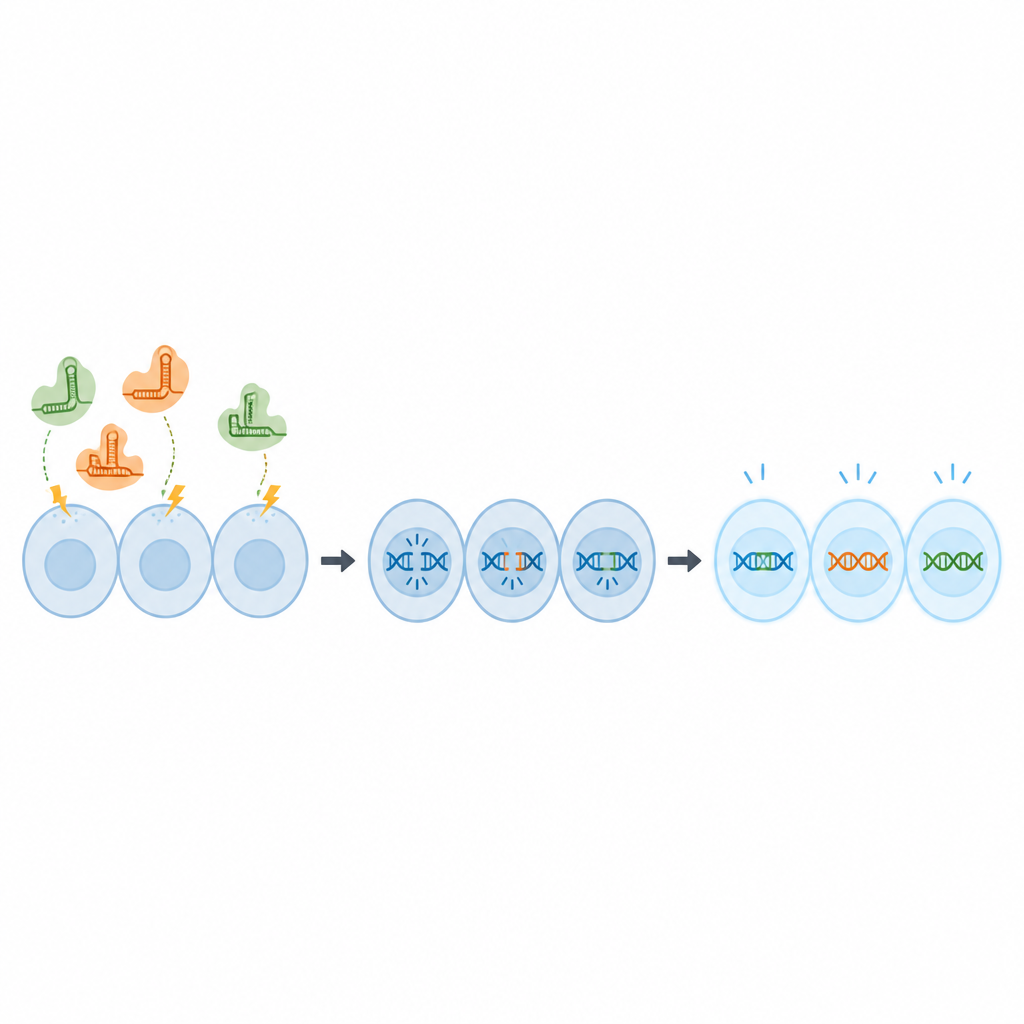
O que isso significa para a saúde futura dos peixes
O trabalho fornece uma receita prática para edição genética de alta eficiência em uma linhagem celular cerebral de tilápia amplamente utilizada. Ao demonstrar que os componentes do CRISPR podem ser entregues de forma segura e que tanto genes marcadores quanto nativos podem ser interrompidos na maioria das células, o estudo transforma as células OmB em um banco de testes poderoso. Pesquisadores agora podem, com mais facilidade, ligar ou desligar genes candidatos para ver como influenciam a infecção viral, respostas ao estresse ou outros traços. Embora este estudo ainda não tenha criado peixes resistentes a doenças, ele fornece uma ferramenta fundamental que ajudará os cientistas a identificar as mudanças genéticas mais prováveis de tornar a tilápia de cria mais resiliente no futuro.
Citação: Wang, J., Bobrik, M., Pankaew, N. et al. Efficient genome editing in a Mozambique tilapia cell line using CAS ribonucleoprotein complexes. Sci Rep 16, 15125 (2026). https://doi.org/10.1038/s41598-026-42702-w
Palavras-chave: tilápia, aquicultura, CRISPR, doença em peixes, edição do genoma