Clear Sky Science · ja
CASリボヌクレオタンパク複合体を用いたモザンビーク・ティラピア細胞株での効率的なゲノム編集
なぜこの研究が魚と食料に重要なのか
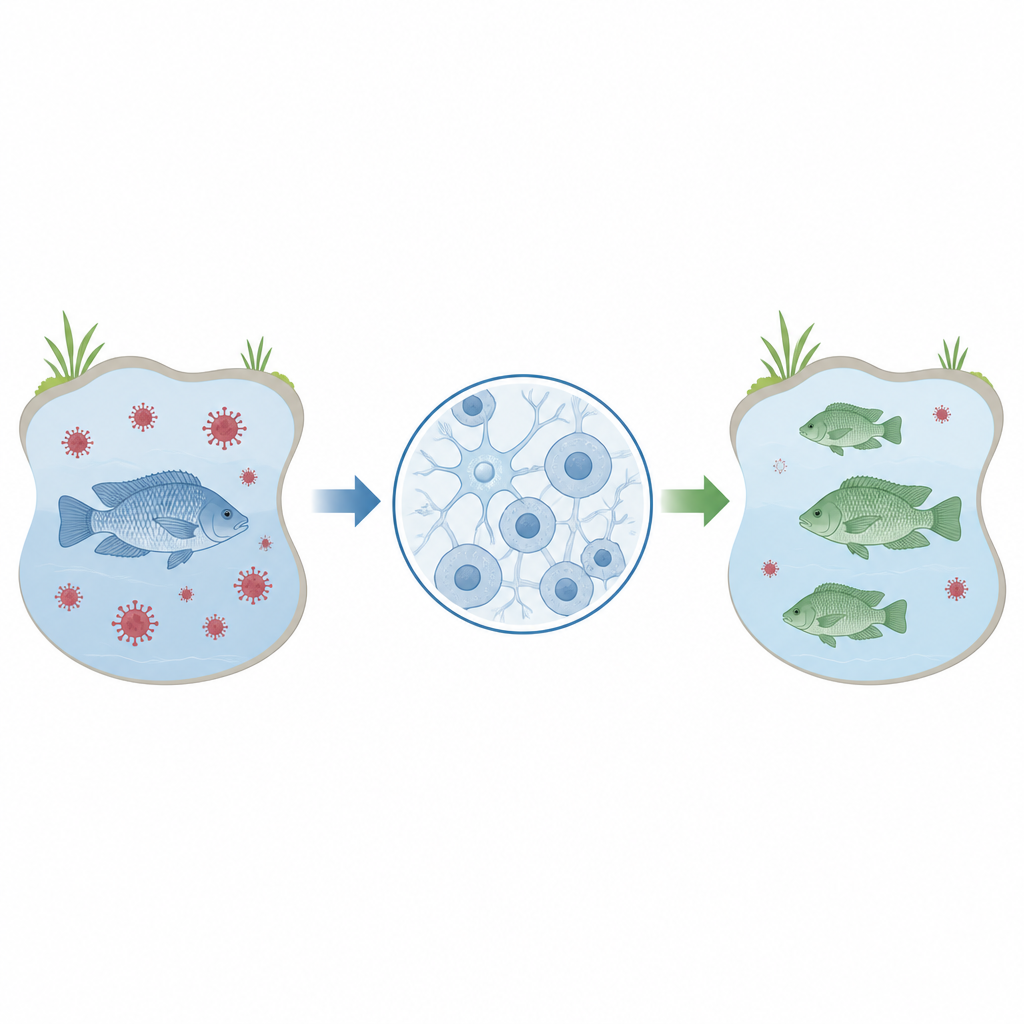
ティラピアは世界中の食卓で主要な魚であり、特に手ごろで良質なタンパク源が急務とされる地域で重要です。しかし、ティラピア養殖はTilapia lake virusのようなウイルス性疾患に脆弱で、養殖資源が一気に失われ、生計を脅かすことがあります。本研究は、ティラピアの脳由来細胞において迅速かつ正確に遺伝子を編集する実験室ベースの手法を示しており、将来的に病気に強い魚を育成し、世界の食料安全保障を支えるための基盤を築くものです。
食料安全保障の最前線に立つ魚類
水産養殖はすでに世界で消費される動物性タンパク質の約6分の1を供給しており、ティラピアは最も飼育が容易で一般的な魚の一つです。成長が早く、養殖池での混雑にも耐え、概して丈夫です。しかし、成長や疾病耐性といった形質を改良する従来の選抜育種は時間がかかり、在来の個体差に制約されます。ゲノム編集は一世代で有用な遺伝的変化を導入する手段を提供し、養殖魚における深刻なウイルス感染への抵抗性のような形質に特に有用となり得ます。
有用な細胞モデルの構築
研究者らはモザンビーク・ティラピアの脳から由来するOmBという細胞株に着目しました。これらの細胞はTilapia lake virusに感染することが知られており、ウイルスと宿主の相互作用を研究する実用的な代替となります。こうした細胞を使ってどの遺伝子が感染や抵抗性に影響するかを調べるには、特定の遺伝子を確実かつ効率的に改変してその結果を測定できる信頼できる方法が必要です。本研究は、広く使われる遺伝子編集ツールであるCRISPRを用いて、まさにそれを段階的に最適化することを目的としました。
編集ツールの微調整
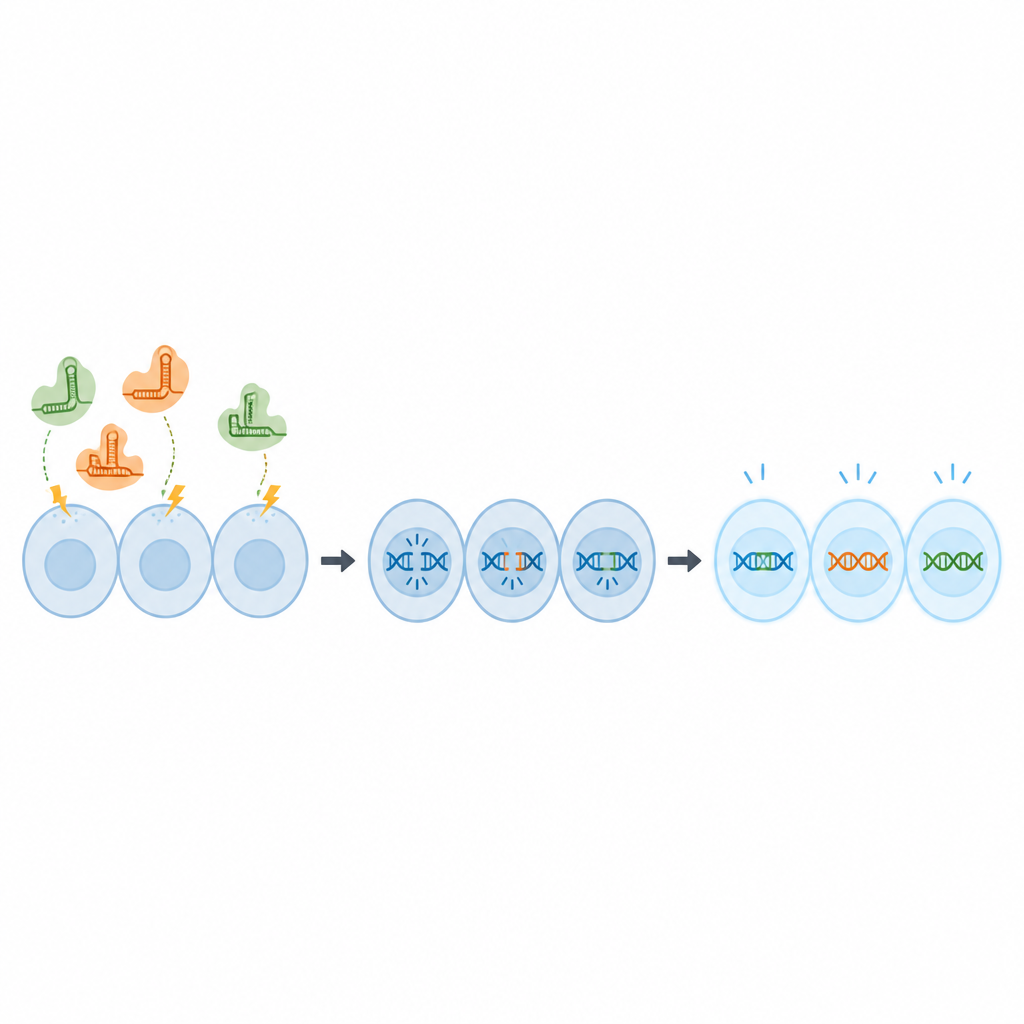
CRISPR成分をDNAとして導入すると細胞内に長く残留して安全性の懸念を生じる可能性があるため、研究チームは既製のタンパク質とRNAの複合体、すなわちリボヌクレオタンパク(RNP)を用いました。これらを電気穿孔法と呼ばれる短い電気パルスでOmB細胞に導入しました。まず、蛍光トレーサー分子を使って電圧、パルス長、濃度の異なる組み合わせを試し、ほぼすべての細胞にトレーサーが取り込まれつつ生存率が保たれる条件を探しました。トレーサー濃度2マイクロモルと特定のパルス設定が、ほぼ完全な取り込みと細胞の健康を両立することが分かりました。
方法の検証と実証
次に、これらの条件が実際に遺伝子を変化させるかを検証しました。研究者らは緑色に蛍光するOmB細胞株を用い、緑色蛍光タンパク質遺伝子を切断するようにCRISPR分子を設計しました。最適化した電気条件下でゲノムコピーの約80%が編集され、2週間後には蛍光を示す細胞はごく一部に減少し、遺伝子が効果的にオフになったことが示されました。次に、細胞を死なせず明瞭な指標を与える2つの通常のティラピア遺伝子を対象に同じプロトコルを適用したところ、約67〜70%の編集率と強い機能欠損(ノックアウト)が予測されました。
将来の魚類健康への意義
この仕事は、広く使われるティラピア脳細胞株における高効率な遺伝子編集の実用的なレシピを提供します。CRISPR成分を安全に導入でき、指標遺伝子や内在性遺伝子のほとんどを破壊できることを示すことで、OmB細胞を強力な試験場に変えました。研究者は候補遺伝子をオン・オフにして、それらがウイルス感染、ストレス応答、その他の形質にどのように影響するかをより容易に調べられます。本研究はまだ病気に耐える魚を直接作成したわけではありませんが、養殖ティラピアを将来より回復力のあるものにする可能性が高い遺伝学的変化を特定するための重要なツールを提供します。
引用: Wang, J., Bobrik, M., Pankaew, N. et al. Efficient genome editing in a Mozambique tilapia cell line using CAS ribonucleoprotein complexes. Sci Rep 16, 15125 (2026). https://doi.org/10.1038/s41598-026-42702-w
キーワード: ティラピア, 水産養殖, CRISPR, 魚類疾患, ゲノム編集