Clear Sky Science · fr
Édition efficace du génome dans une lignée cellulaire de tilapia du Mozambique à l’aide de complexes ribonucléoprotéiques CAS
Pourquoi cette étude compte pour le poisson et l’alimentation
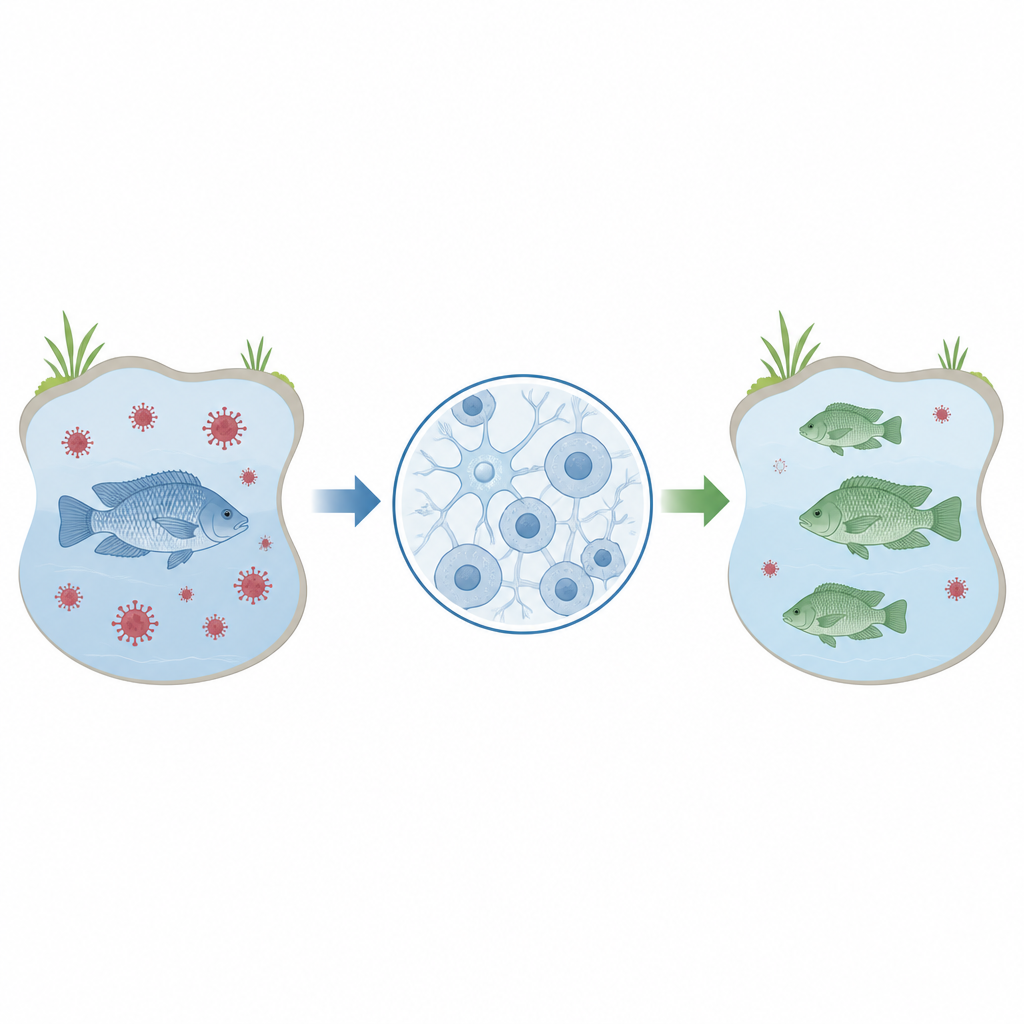
Le tilapia est un poisson de base dans de nombreux repas à travers le monde, notamment dans des régions où une source de protéines abordable et de qualité est essentielle. Pour autant, les élevages de tilapia sont vulnérables aux maladies virales comme le Tilapia lake virus, qui peuvent décimer les stocks et menacer des moyens de subsistance. Cette étude décrit une méthode en laboratoire pour éditer rapidement et précisément des gènes de tilapia dans des cellules cérébrales, posant les bases de travaux futurs visant à élever des poissons plus résistants aux maladies et à soutenir la sécurité alimentaire mondiale.
Des poissons en première ligne de la sécurité alimentaire
L’aquaculture fournit déjà environ un sixième des protéines animales consommées dans le monde, et le tilapia fait partie des poissons les plus faciles et courants à élever. Il croît rapidement, tolère des bassins denses et est généralement robuste. Cependant, l’amélioration traditionnelle par sélection pour des caractères comme la croissance ou la résistance aux maladies est lente et limitée par la variation naturelle présente dans un stock. L’édition du génome offre un moyen d’introduire des changements génétiques utiles en une seule génération, ce qui pourrait être particulièrement précieux pour des caractères tels que la résistance aux infections virales graves chez les poissons d’élevage.
Construire un modèle cellulaire utile
Les chercheurs se sont concentrés sur une lignée cellulaire appelée OmB, dérivée du cerveau du tilapia du Mozambique. Ces cellules sont connues pour être infectées par le Tilapia lake virus, ce qui en fait un substitut pratique pour étudier les interactions entre le virus et son hôte. Avant que ces cellules puissent être largement utilisées pour tester quels gènes influencent l’infection ou la résistance, les scientifiques ont besoin d’une méthode fiable et efficace pour modifier des gènes spécifiques dans ces cellules puis mesurer les conséquences. Cette étude avait pour objectif d’affiner un protocole étape par étape pour faire exactement cela en utilisant un outil d’édition génique populaire connu sous le nom de CRISPR.
Affiner l’outil d’édition
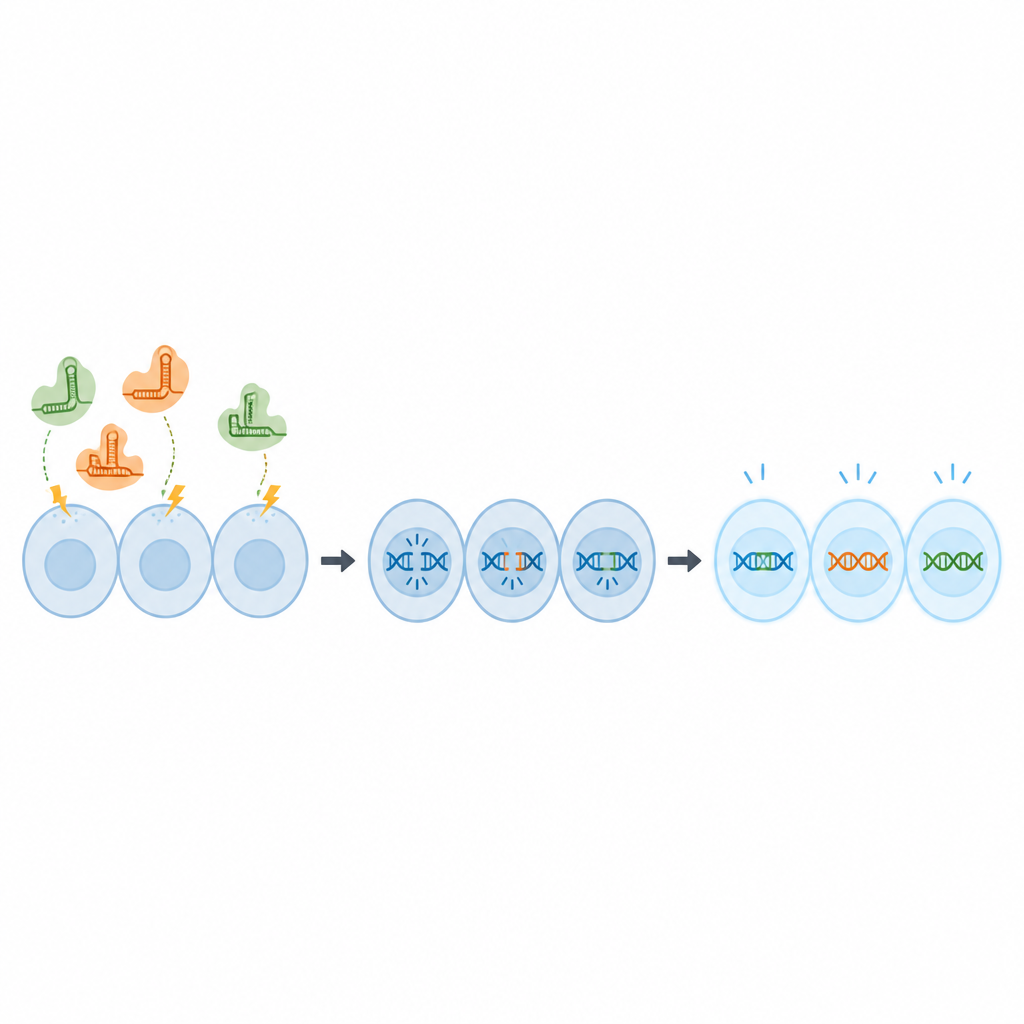
Plutôt que de livrer les composants CRISPR sous forme d’ADN, qui peut persister dans les cellules et soulever des préoccupations de sécurité, l’équipe a utilisé des complexes protéine‑ARN prêts à l’emploi, appelés ribonucléoprotéines. Ceux‑ci ont été introduits dans les cellules OmB par de courtes impulsions électriques dans une technique appelée électroporation. D’abord, les scientifiques ont utilisé une molécule traceuse fluorescente pour tester différentes combinaisons de tension, de durée d’impulsion et de concentration, cherchant des conditions qui faisaient entrer le traceur dans presque toutes les cellules sans nuire à leur survie. Ils ont trouvé qu’une concentration de traceur de 2 micromolaires et un réglage d’impulsion spécifique donnaient une capture quasi complète tout en conservant des cellules en bonne santé.
Tester et valider la méthode
Ensuite, l’équipe a vérifié si ces conditions pouvaient effectivement modifier des gènes. Ils ont utilisé une version de la lignée OmB qui brille en vert et ont conçu des molécules CRISPR pour couper le gène codant la protéine verte. Avec les réglages électriques optimisés, près de 80 % des copies du gène ont été éditées, et deux semaines plus tard seule une petite fraction des cellules brillait encore, montrant que le gène avait été efficacement inactivé. Les scientifiques sont ensuite passés à deux gènes tilapia normaux, choisis parce que leur modification n’est pas létale pour les cellules mais fournit un signal clair. En utilisant le même protocole, ils ont obtenu des taux d’édition d’environ 67 à 70 % et une prédiction forte d’inactivation de la fonction génique.
Ce que cela signifie pour la santé future des poissons
Ce travail fournit une recette pratique pour une édition génomique à haute efficacité dans une lignée cellulaire cérébrale de tilapia largement utilisée. En montrant que les composants CRISPR peuvent être délivrés en toute sécurité et que des gènes témoins et natifs peuvent être perturbés dans la plupart des cellules, l’étude transforme les cellules OmB en une plateforme d’essai puissante. Les chercheurs peuvent désormais plus facilement activer ou désactiver des gènes candidats pour observer leur influence sur l’infection virale, les réponses au stress ou d’autres caractères. Bien que cette étude n’ait pas encore produit des poissons résistants aux maladies, elle fournit un outil clé qui aidera les scientifiques à identifier les modifications génétiques les plus susceptibles de rendre le tilapia d’élevage plus résilient à l’avenir.
Citation: Wang, J., Bobrik, M., Pankaew, N. et al. Efficient genome editing in a Mozambique tilapia cell line using CAS ribonucleoprotein complexes. Sci Rep 16, 15125 (2026). https://doi.org/10.1038/s41598-026-42702-w
Mots-clés: tilapia, aquaculture, CRISPR, maladie des poissons, édition du génome