Clear Sky Science · ar
تحرير جينوم فعال في سلالة خلايا البلطي الموزمبيقي باستخدام مجمعات ريبونو بروتين CAS
لماذا تهم هذه الدراسة الأسماك والغذاء
يُعدّ البلطي سمكة أساسية على موائد العشاء حول العالم، لا سيما في المناطق التي تحتاج فيها البروتين عالي الجودة وبأسعار معقولة. ومع ذلك، فإن مزارع البلطي عرضة للأمراض الفيروسية مثل فيروس بحيرة البلطي، الذي قد يدمر المخزونات ويهدد سبل العيش. تصف هذه الدراسة طريقة مخبرية لتعديل جينات البلطي بسرعة ودقة في خلايا الدماغ، مما يمهد الطريق لأبحاث مستقبلية تهدف إلى تربية أسماك تتحمّل الأمراض بشكل أفضل وتدعم الأمن الغذائي العالمي.
الأسماك على خط المواجهة للأمن الغذائي
يوفر الاستزراع المائي بالفعل نحو سدس البروتين الحيواني المستهلك عالمياً، ويُعد البلطي من أسهل وأكثر الأنواع شيوعاً للاستزراع. فهو ينمو بسرعة، ويتحمل البرك المكتظة، وعموماً قوي التحمل. ومع ذلك، فإن التحسين الوراثي التقليدي لصفات مثل النمو ومقاومة الأمراض بطيء ومقيد بالتنوع الطبيعي الموجود في السلالة. يوفر تحرير الجينوم وسيلة لإدخال تغييرات جينية مفيدة في جيل واحد، وهو ما يمكن أن يكون ذا قيمة خاصة للصفات مثل المقاومة للعدوى الفيروسية الشديدة في الأسماك المستزرعة.
بناء نموذج خلوي مفيد
ركز الباحثون على سلالة خلوية تسمى OmB، مشتقة من دماغ بلطي موزمبيق. تُعرف هذه الخلايا بأنها قابلة لعدوى فيروس بحيرة البلطي، مما يجعلها بديلاً عملياً لدراسة كيفية تفاعل الفيروس مع العائل. قبل أن تُستخدم هذه الخلايا على نطاق واسع لاختبار أي الجينات تؤثر في العدوى أو المقاومة، يحتاج العلماء إلى طريقة موثوقة وفعالة لتعديل جينات محددة في هذه الخلايا ثم قياس النتائج. هدفت هذه الدراسة إلى ضبط بروتوكول خطوة بخطوة لتحقيق ذلك باستخدام أداة تحرير الجينات الشائعة المعروفة باسم CRISPR.
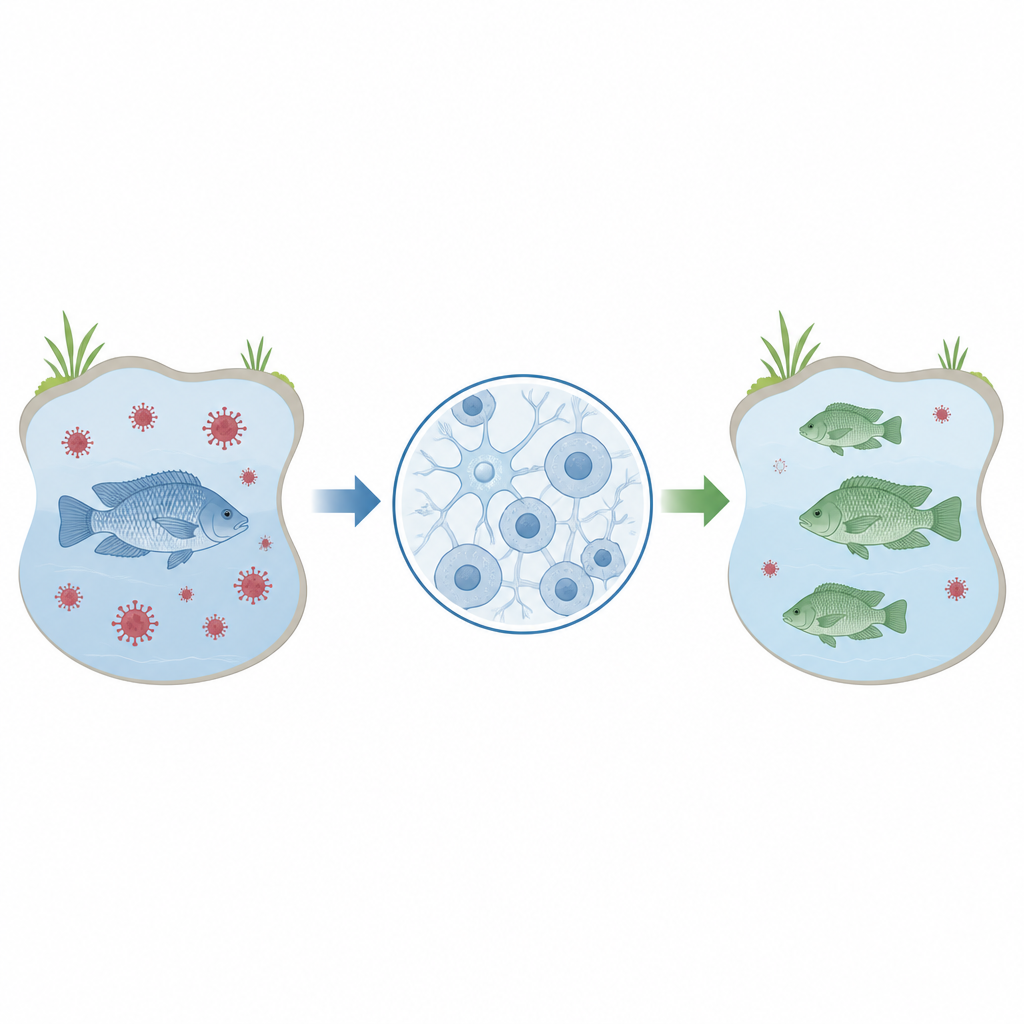
ضبط أداة التحرير
بدلاً من توصيل مكونات CRISPR على شكل حمض نووي قد يبقى في الخلايا ويثير مخاوف تتعلق بالسلامة، استخدم الفريق مجمعات جاهزة من البروتين والحمض النووي الريبي تُعرف بالريبونو بروتينات. دُفعت هذه المجمعات إلى خلايا OmB بواسطة نبضات كهربائية قصيرة في تقنية تُسمى التحفيز الكهربائي (electroporation). أولاً، استخدم العلماء جزيء تتبع فلوري لاختبار تركيبات مختلفة من الجهد، وطول النبضة والتركيز، باحثين عن شروط توصل الجزيء إلى جميع الخلايا تقريباً دون الإضرار ببقائها. وجدوا أن تركيز 2 ميكرومولار للتتبع وإعداد نبضة محدد أعطى امتصاصاً شبه كامل مع خلايا صحية.
اختبار وإثبات الطريقة
بعد ذلك، تساءل الفريق عما إذا كانت هذه الشروط يمكنها فعلاً تغيير الجينات. استخدموا نسخة من سلالة خلايا OmB تتوهج باللون الأخضر وصمموا جزيئات CRISPR لقطع جين البروتين الأخضر. تحت الإعدادات الكهربائية المحسّنة، تم تحرير نحو 80 في المئة من نسخ الجين، وبعد أسبوعين لم تتوهّج سوى نسبة صغيرة من الخلايا، مما يدل على أن الجين قد أُوقف بفعالية. ثم انتقل الباحثون إلى جينين طبيعيين في البلطي، اختيرت لأن تغييره لا يقتل الخلايا ولكنه يوفر قراءة واضحة. باستخدام نفس البروتوكول، حققوا معدلات تحرير تقارب 67 إلى 70 في المئة وتوقعات قوية لوقف وظيفة الجين.
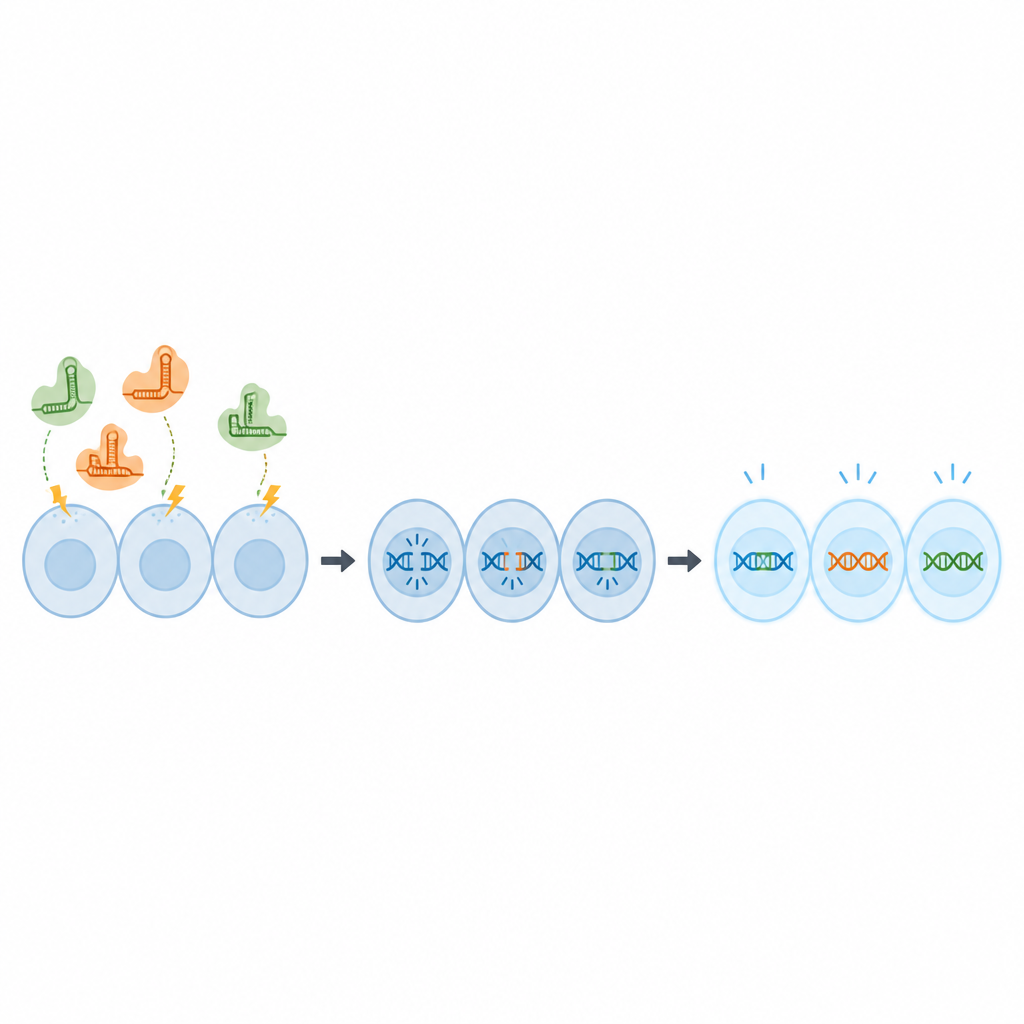
ما يعنيه هذا لصحة الأسماك في المستقبل
تقدم هذه الدراسة وصفة عملية لتحرير الجينات بكفاءة عالية في سلالة خلايا دماغ البلطي المستخدمة على نطاق واسع. من خلال إظهار أن مكونات CRISPR يمكن توصيلها بأمان وأنه يمكن تعطيل كل من الجينات الموسومة والطبيعية في معظم الخلايا، تحوّل الدراسة خلايا OmB إلى منصة اختبار قوية. يمكن للباحثين الآن بسهولة أكبر تشغيل أو إيقاف الجينات المرشحة لمعرفة كيف تؤثر في العدوى الفيروسية، واستجابات الإجهاد أو صفات أخرى. بينما لم تخلق هذه الدراسة بعد أسماكاً مقاومة للأمراض، فإنها توفر أداة أساسية ستساعد العلماء في تحديد التغييرات الجينية الأرجح لجعل البلطي المستزرع أكثر مرونة في المستقبل.
الاستشهاد: Wang, J., Bobrik, M., Pankaew, N. et al. Efficient genome editing in a Mozambique tilapia cell line using CAS ribonucleoprotein complexes. Sci Rep 16, 15125 (2026). https://doi.org/10.1038/s41598-026-42702-w
الكلمات المفتاحية: بلطي, الاستزراع المائي, كريسبر, أمراض الأسماك, تحرير الجينوم