Clear Sky Science · ru
Эффективное редактирование генома в клеточной линии мозамбикской тилапии с использованием комплексов РНК-белок CAS
Почему это исследование важно для рыб и продовольственной безопасности
Тилапия — распространенная рыба на обеденных столах по всему миру, особенно в регионах, где срочно нужен доступный и качественный белок. Однако рыбные фермы, разводящие тилапию, уязвимы к вирусным заболеваниям, таким как Tilapia lake virus, которые могут уничтожать стада и подрывать средства к существованию. В этом исследовании описан лабораторный метод быстрой и точной правки генов тилапии в клетках головного мозга, который закладывает основу для будущих работ по выведению рыб, более устойчивых к болезням, и поддержки глобальной продовольственной безопасности.
Рыбы на передовой продовольственной безопасности
Аквакультура уже обеспечивает примерно одну шестую животного белка, потребляемого в мире, и тилапия — одна из самых простых и распространенных в выращивании рыб. Она быстро растет, переносит высокую плотность посадки и в целом неприхотлива. Тем не менее традиционная селекция для улучшения признаков, таких как рост и устойчивость к болезням, медленна и ограничена природной вариабельностью в популяции. Редактирование генома дает возможность внести полезные генетические изменения за одно поколение, что особенно ценно для признаков, как устойчивость к серьезным вирусным инфекциям у промысловой рыбы.
Создание полезной клеточной модели
Исследователи сосредоточились на клеточной линии OmB, полученной из головного мозга мозамбикской тилапии. Известно, что эти клетки инфицируются Tilapia lake virus, что делает их практичной моделью для изучения взаимодействия вируса с хозяином. Прежде чем такие клетки можно будет широко использовать для тестирования генов, влияющих на инфекцию или устойчивость, ученым нужна надежная и эффективная методика точечной модификации генов и последующего измерения последствий. В этом исследовании поставлена задача отшлифовать пошаговый протокол для выполнения именно этого с помощью популярного инструмента редактирования генома CRISPR.
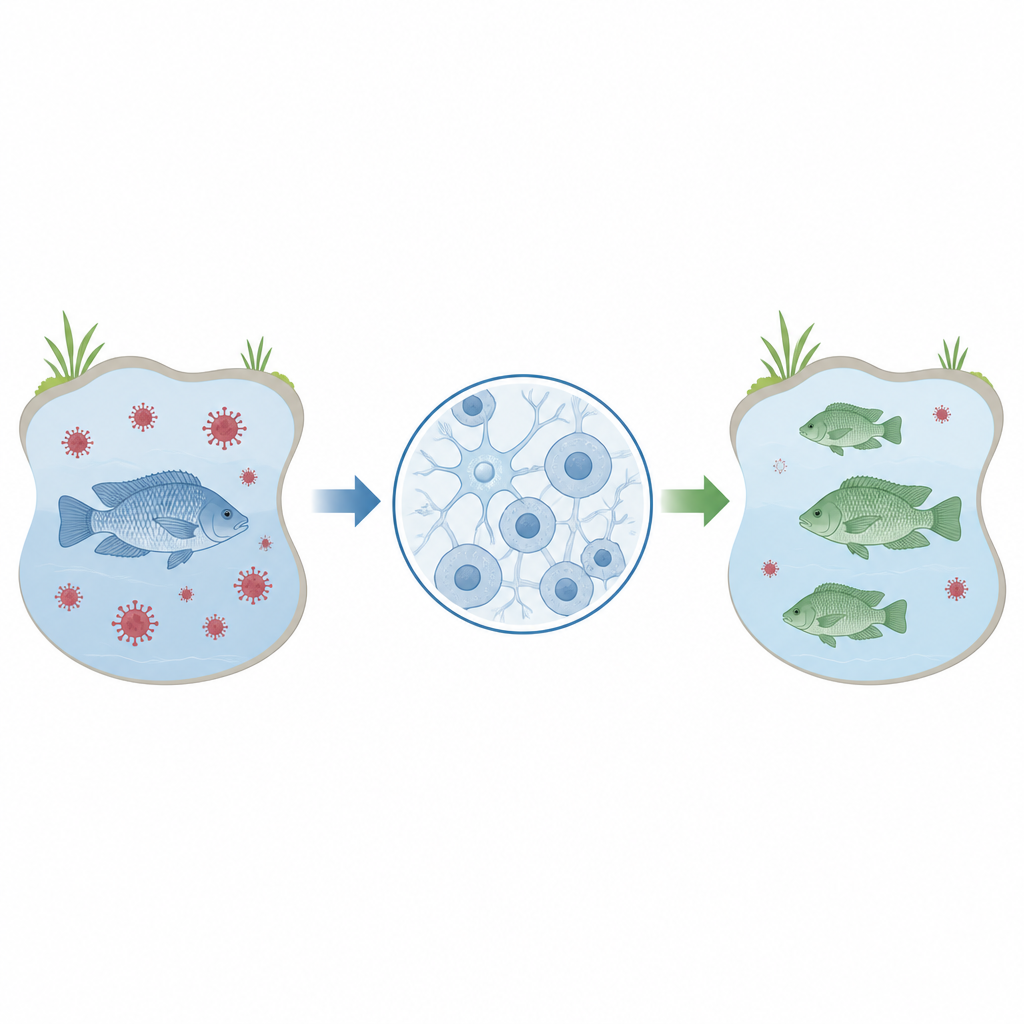
Тонкая настройка инструмента редактирования
Вместо доставки компонентов CRISPR в виде ДНК, которая может сохраняться в клетках и вызывать вопросы безопасности, команда использовала заранее собранные белково-РНКовые комплексы, известные как рибонуклеопротеины. Их вводили в клетки OmB короткими электрическими импульсами в технике, называемой электропорацией. Сначала ученые применили флуоресцентный маркер, чтобы протестировать различные комбинации напряжения, длительности импульса и концентрации, и выбрать условия, при которых маркер попадает почти во все клетки без ущерба для их выживаемости. Они обнаружили, что концентрация маркера 2 микромоля и определенные параметры импульса обеспечивали почти полное усвоение при сохранении здоровых клеток.
Тестирование и подтверждение метода
Далее команда проверила, могут ли эти условия действительно изменять гены. Они использовали вариант клеточной линии OmB, который светится зеленым, и спроектировали молекулы CRISPR для разрезания гена зеленого флуоресцентного белка. При оптимизированных электрических параметрах почти 80 процентов копий гена были отредактированы, а через две недели лишь небольшая доля клеток все еще светилась, что свидетельствует о эффективном выключении гена. Затем ученые перешли к двум нормальным генам тилапии, выбранным потому, что их изменение не убивает клетки, но дает четкий результат. При использовании того же протокола достигали уровней редактирования около 67–70 процентов и сильного предположительного нокаута функции гена.
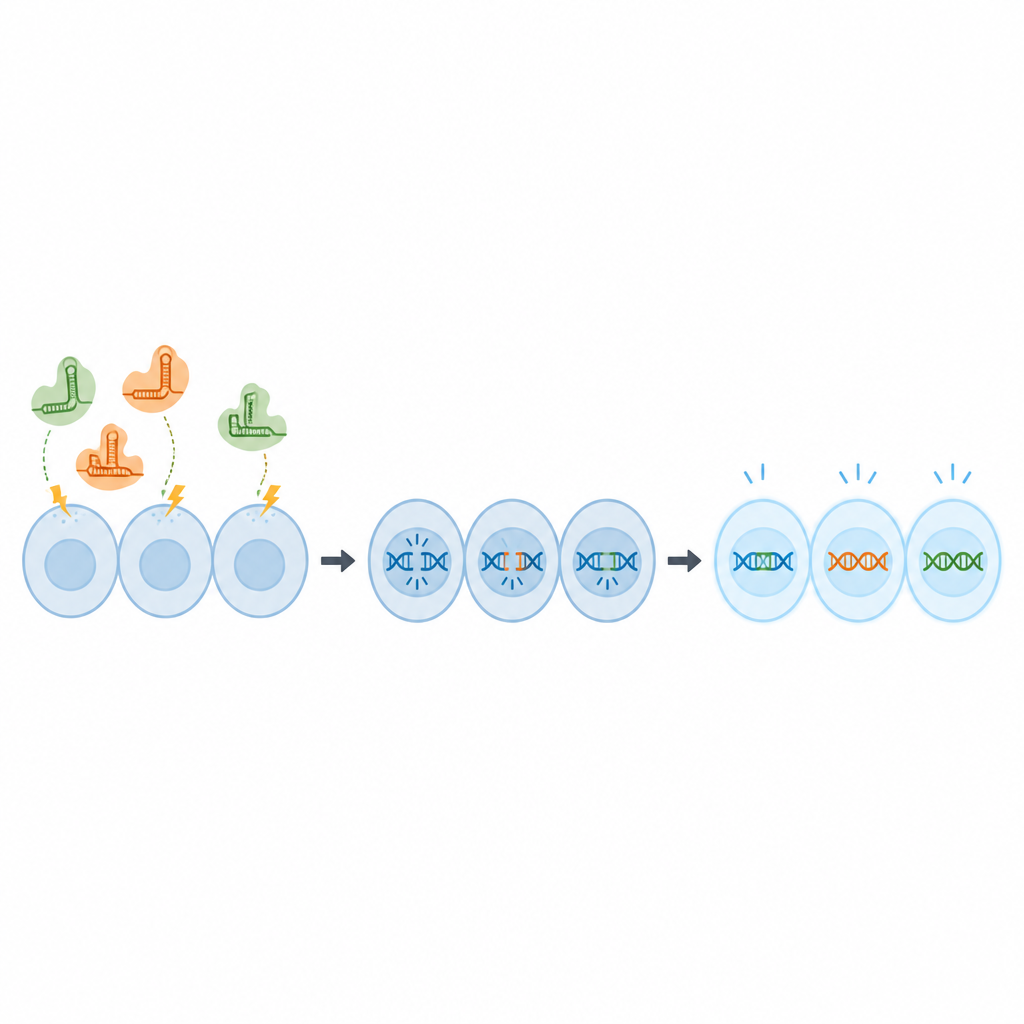
Что это означает для здоровья рыб в будущем
Работа предоставляет практическую инструкцию для высокоэффективного редактирования генов в широко используемой клеточной линии головного мозга тилапии OmB. Показав, что компоненты CRISPR можно безопасно доставить и что как маркерные, так и нативные гены можно нарушить в большинстве клеток, исследование превращает OmB в мощную тестовую платформу. Теперь ученым будет проще включать или выключать кандидаты-гены, чтобы увидеть, как они влияют на вирусную инфекцию, реакции на стресс и другие признаки. Хотя в этом исследовании еще не были получены рыбы, устойчивые к болезням, оно предоставляет ключевой инструмент, который поможет ученым выявить генетические изменения, наиболее вероятно повышающие устойчивость промысловой тилапии в будущем.
Цитирование: Wang, J., Bobrik, M., Pankaew, N. et al. Efficient genome editing in a Mozambique tilapia cell line using CAS ribonucleoprotein complexes. Sci Rep 16, 15125 (2026). https://doi.org/10.1038/s41598-026-42702-w
Ключевые слова: тилапия, аквакультура, CRISPR, болезни рыб, редактирование генома