Clear Sky Science · es
Edición genómica eficiente en una línea celular de tilapia de Mozambique mediante complejos ribonucleoproteicos CAS
Por qué este estudio importa para los peces y la alimentación
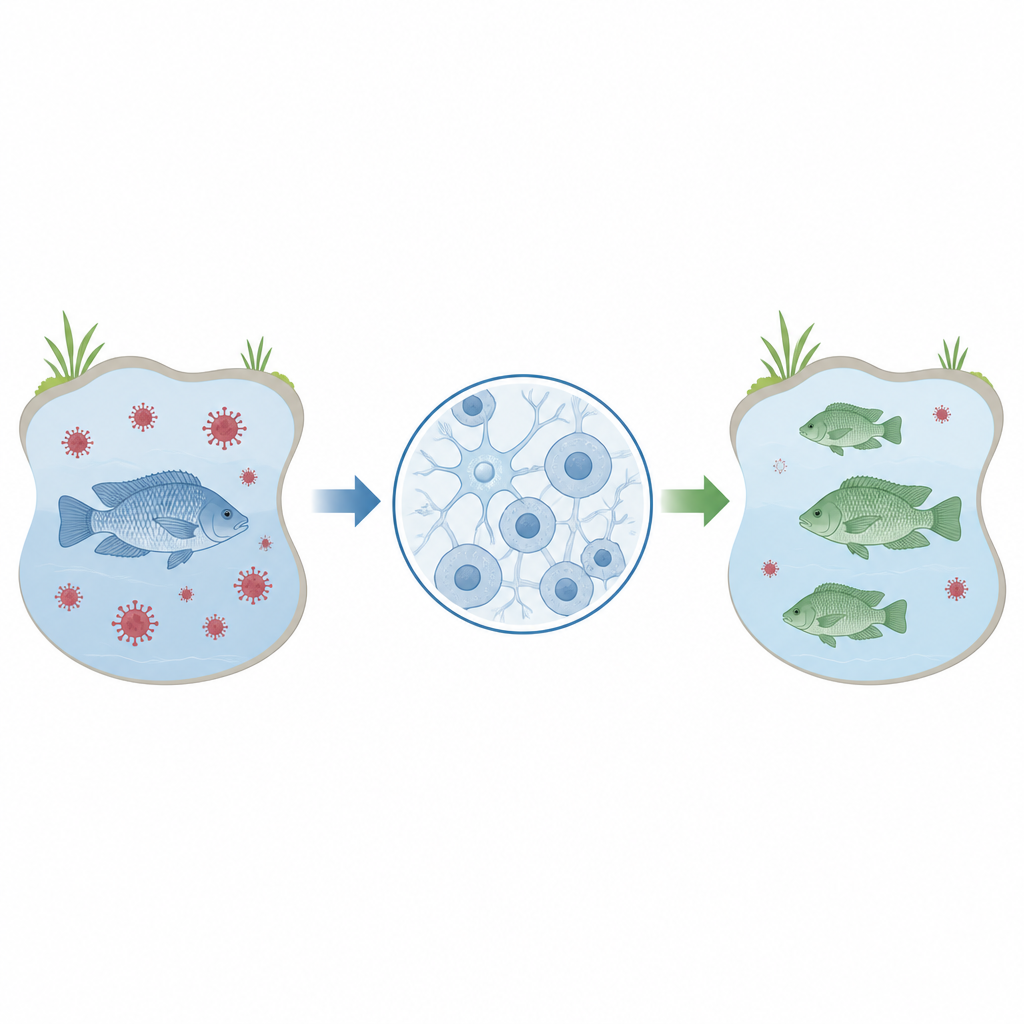
La tilapia es un pescado básico en los platos de todo el mundo, especialmente en regiones donde se necesita con urgencia proteína asequible y de calidad. Sin embargo, las granjas de tilapia son vulnerables a enfermedades virales como el Tilapia lake virus, que pueden diezmar existencias y amenazar medios de vida. Este estudio describe un método de laboratorio para editar rápida y precisamente genes de tilapia en células cerebrales, sentando las bases para trabajos futuros que permitan criar peces con mejor capacidad de resistir enfermedades y contribuir a la seguridad alimentaria global.
Los peces en la primera línea de la seguridad alimentaria
La acuicultura ya suministra aproximadamente una sexta parte de la proteína animal consumida a nivel mundial, y la tilapia está entre los peces más fáciles y comunes de cultivar. Crecen rápido, toleran estanques con alta densidad y son, en general, resistentes. Sin embargo, la mejora genética tradicional mediante selección para rasgos como crecimiento y resistencia a enfermedades es lenta y limitada por la variación natural presente en una población. La edición del genoma ofrece una forma de introducir cambios genéticos útiles en una sola generación, lo cual podría ser especialmente valioso para rasgos como la resistencia a infecciones virales graves en peces de cultivo.
Construyendo un modelo celular útil
Los investigadores se centraron en una línea celular llamada OmB, derivada del cerebro de la tilapia de Mozambique. Se sabe que estas células son infectables por el Tilapia lake virus, lo que las convierte en un sustituto práctico para estudiar cómo el virus interactúa con su huésped. Antes de que dichas células puedan usarse ampliamente para probar qué genes afectan la infección o la resistencia, los científicos necesitan una forma fiable y eficiente de modificar genes específicos en estas células y luego medir los efectos. Este estudio se propuso ajustar paso a paso un protocolo para hacer precisamente eso usando una herramienta de edición genética popular conocida como CRISPR.
Ajustando finamente la herramienta de edición
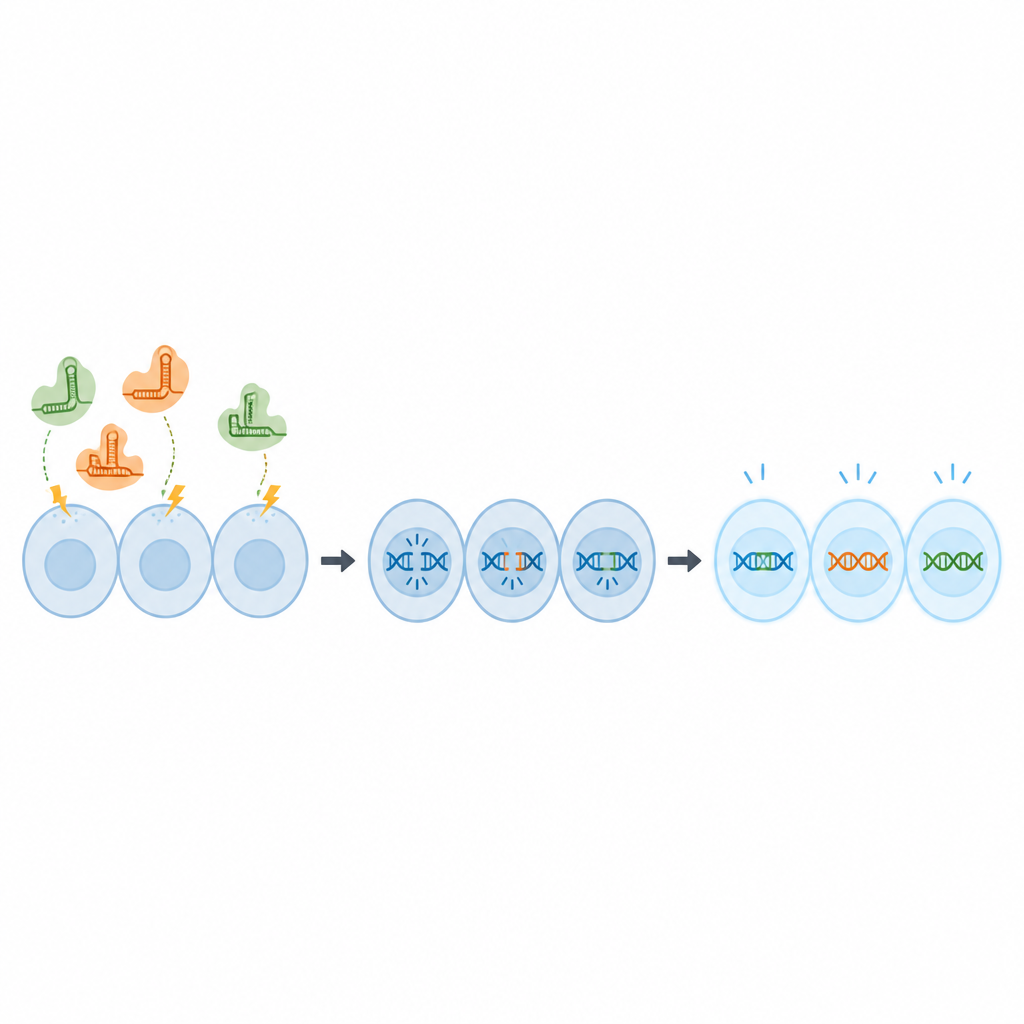
En lugar de entregar los componentes de CRISPR como ADN, que puede persistir en las células y plantear preocupaciones de seguridad, el equipo usó complejos preparados de proteína y ARN conocidos como ribonucleoproteínas. Estos se introdujeron en las células OmB mediante pulsos eléctricos cortos en una técnica llamada electroporación. Primero, los científicos emplearon una molécula trazadora fluorescente para probar diferentes combinaciones de voltaje, duración del pulso y concentración, buscando condiciones que llevaran el trazador a casi todas las células sin afectar su supervivencia. Encontraron que una concentración de 2 micromolar del trazador y un ajuste de pulso específico proporcionaban una captación casi completa con células saludables.
Probar y demostrar el método
A continuación, el equipo evaluó si esas condiciones podían realmente alterar genes. Usaron una versión de la línea celular OmB que emite fluorescencia verde y diseñaron moléculas CRISPR para cortar el gen de la proteína verde. Bajo los ajustes eléctricos optimizados, casi el 80 por ciento de las copias genéticas fueron editadas, y dos semanas después solo una pequeña fracción de las células seguía brillando, lo que demuestra que el gen se había desactivado con eficacia. Los científicos siguieron con dos genes tilapia nativos, elegidos porque su modificación no mata las células pero ofrece una lectura clara. Usando el mismo protocolo, lograron tasas de edición de alrededor del 67 al 70 por ciento y una fuerte predicción de anulación de la función génica.
Qué significa esto para la salud futura de los peces
El trabajo proporciona una receta práctica para la edición génica de alta eficiencia en una línea celular cerebral de tilapia ampliamente utilizada. Al demostrar que los componentes CRISPR pueden entregarse de forma segura y que tanto genes marcadores como nativos pueden interrumpirse en la mayoría de las células, el estudio convierte las células OmB en un banco de pruebas potente. Los investigadores ahora pueden activar o desactivar con mayor facilidad genes candidatos para ver cómo influyen en la infección viral, las respuestas al estrés u otros rasgos. Aunque este estudio aún no creó peces resistentes a enfermedades, proporciona una herramienta clave que ayudará a los científicos a identificar los cambios genéticos con más probabilidades de hacer a la tilapia de cultivo más resiliente en el futuro.
Cita: Wang, J., Bobrik, M., Pankaew, N. et al. Efficient genome editing in a Mozambique tilapia cell line using CAS ribonucleoprotein complexes. Sci Rep 16, 15125 (2026). https://doi.org/10.1038/s41598-026-42702-w
Palabras clave: tilapia, acuicultura, CRISPR, enfermedades de peces, edición del genoma