Clear Sky Science · pl
Wydajne edytowanie genomu w linii komórkowej tilapii mozambickiej z użyciem kompleksów rybonukleoprotein CAS
Dlaczego to badanie ma znaczenie dla ryb i żywności
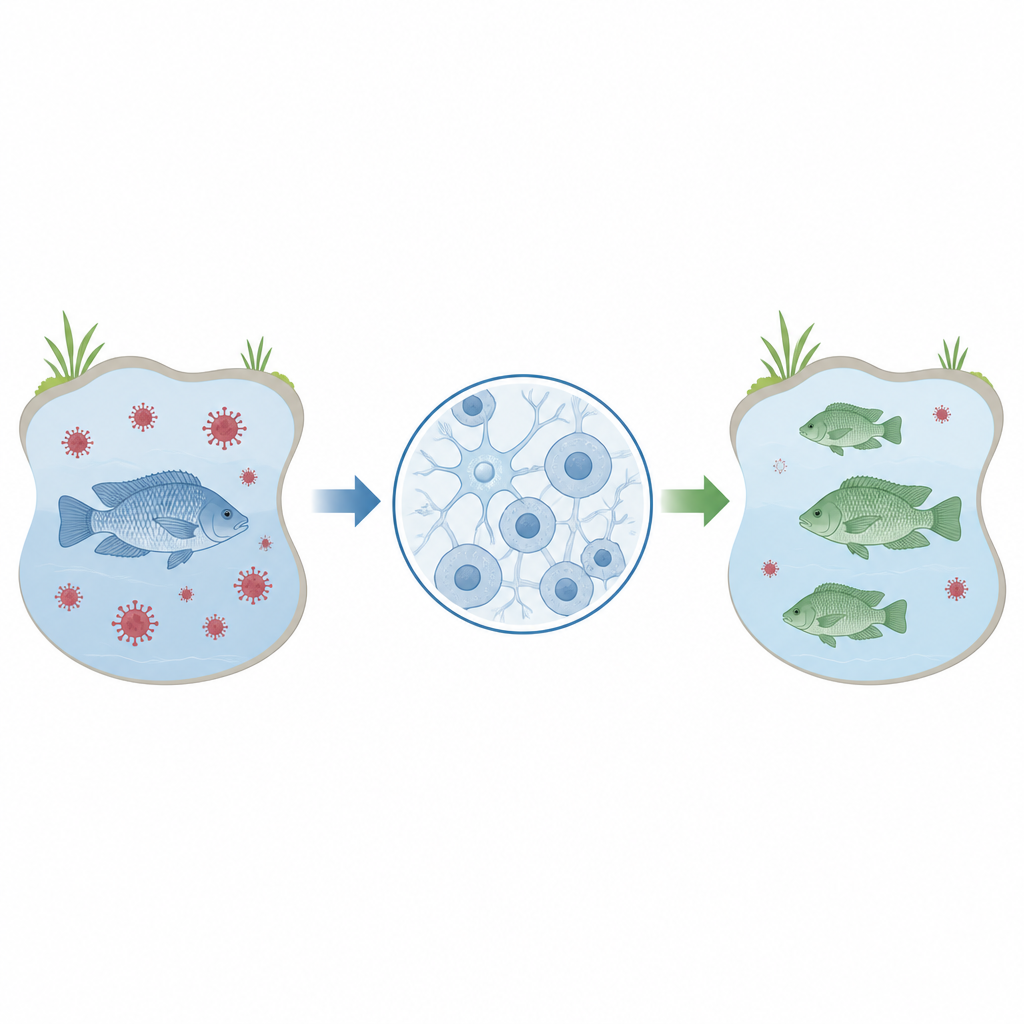
Tilapia to podstawowa ryba na stołach na całym świecie, zwłaszcza w regionach, gdzie pilnie potrzebne są przystępne i wysokiej jakości źródła białka. Hodowle tilapii są jednak podatne na choroby wirusowe, takie jak wirus jeziora Tilapia (Tilapia lake virus), które mogą zdziesiątkować stada i zagrażać środkom do życia. W tym badaniu opisano metodę laboratoryjną pozwalającą szybko i precyzyjnie edytować geny tilapii w komórkach mózgowych, co tworzy podstawy pod przyszłe prace nad hodowlą ryb odporniejszych na choroby i wspierających bezpieczeństwo żywnościowe.
Ryby na pierwszej linii bezpieczeństwa żywności
Akwakultura już dostarcza około jednej szóstej spożywanego globalnie białka zwierzęcego, a tilapie należą do najłatwiejszych i najczęściej hodowanych ryb. Rosną szybko, tolerują gęste obsady w stawach i są na ogół odporne. Tradycyjne selekcyjne krzyżowanie w celu poprawy cech, takich jak wzrost czy odporność na choroby, jest jednak powolne i ograniczone przez naturalną zmienność w populacji. Edycja genomu daje możliwość wprowadzenia przydatnych zmian genetycznych w jednym pokoleniu, co może być szczególnie ważne dla cech takich jak odporność na poważne infekcje wirusowe w hodowlanych populacjach ryb.
Budowanie użytecznego modelu komórkowego
Badacze skupili się na linii komórkowej zwanej OmB, pochodzącej z mózgu tilapii mozambickiej. Wiadomo, że te komórki są podatne na zakażenie wirusem jeziora Tilapia, co czyni je praktycznym modelem do badania interakcji wirusa z gospodarzem. Zanim takie komórki będą szeroko używane do testowania, które geny wpływają na zakażenie lub odporność, naukowcy potrzebują niezawodnego i efektywnego sposobu modyfikowania konkretnych genów w tych komórkach, a następnie mierzenia efektów. Celem tego badania było dopracowanie krok po kroku protokołu pozwalającego na wykonanie tego zadania za pomocą popularnego narzędzia do edycji genów znanego jako CRISPR.
Dostrojenie narzędzia edytującego
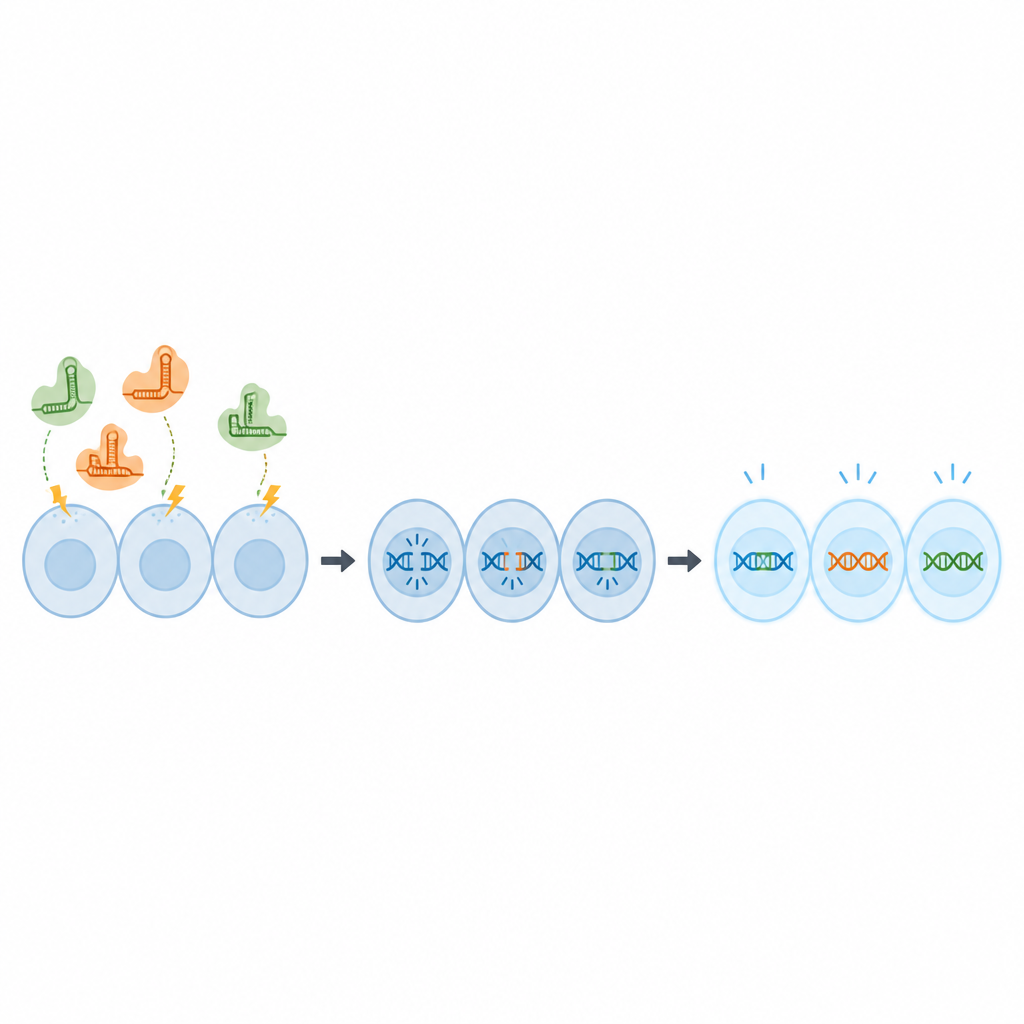
Zamiast dostarczać składniki CRISPR w postaci DNA, które może utrzymywać się w komórkach i budzić obawy bezpieczeństwa, zespół użył gotowych kompleksów białko–RNA, zwanych rybonukleoproteinami. Wprowadzono je do komórek OmB krótkimi impulsami elektrycznymi w technice zwanej elektroporacją. Najpierw naukowcy użyli fluorescencyjnego markera, by przetestować różne kombinacje napięcia, długości impulsu i stężenia, szukając warunków, które przeniosą znacznik do niemal wszystkich komórek, nie zabijając ich przy tym. Stwierdzili, że stężenie markera 2 mikromolowe i określone ustawienie impulsu zapewniało prawie kompletne pobranie przy zachowaniu dobrego przeżycia komórek.
Testowanie i weryfikacja metody
Dalej zespół sprawdził, czy te warunki rzeczywiście pozwalają zmieniać geny. Użyli wersji linii OmB świecącej na zielono i zaprojektowali molekuły CRISPR tak, by przecięły gen kodujący zielony białko fluorescencyjne. Przy zoptymalizowanych ustawieniach elektrycznych niemal 80 procent kopii genu zostało zmodyfikowanych, a po dwóch tygodniach tylko niewielka część komórek nadal świeciła, co pokazało skuteczne wyłączenie genu. Naukowcy przeszli następnie do dwóch natywnych genów tilapii, wybranych dlatego, że ich modyfikacja nie zabija komórek, a daje czytelny odczyt. Korzystając z tego samego protokołu, osiągnęli wskaźniki edycji na poziomie około 67–70 procent oraz silne przewidywane zniesienie funkcji genu.
Co to oznacza dla przyszłego zdrowia ryb
Praca dostarcza praktycznej receptury na wysokowydajną edycję genów w szeroko stosowanej linii komórek mózgowych tilapii. Pokazując, że składniki CRISPR można bezpiecznie dostarczyć i że zarówno geny znakowane, jak i natywne można zakłócić w większości komórek, badanie przekształca komórki OmB w potężne stanowisko testowe. Badacze mogą teraz łatwiej wyłączać lub aktywować kandydackie geny, aby sprawdzić, jak wpływają na zakażenia wirusowe, reakcje na stres czy inne cechy. Choć to badanie jeszcze nie stworzyło ryb odpornych na choroby, dostarcza kluczowe narzędzie, które pomoże naukowcom zidentyfikować zmiany genetyczne najbardziej prawdopodobne do zwiększenia odporności hodowlanych tilapii w przyszłości.
Cytowanie: Wang, J., Bobrik, M., Pankaew, N. et al. Efficient genome editing in a Mozambique tilapia cell line using CAS ribonucleoprotein complexes. Sci Rep 16, 15125 (2026). https://doi.org/10.1038/s41598-026-42702-w
Słowa kluczowe: tilapia, akwakultura, CRISPR, choroby ryb, edycja genomu