Clear Sky Science · de
Effiziente Genomeditierung in einer Mozambique-Tilapia-Zelllinie mithilfe von CAS-Ribonukleoproteinkomplexen
Warum diese Studie für Fisch und Ernährungssicherheit wichtig ist
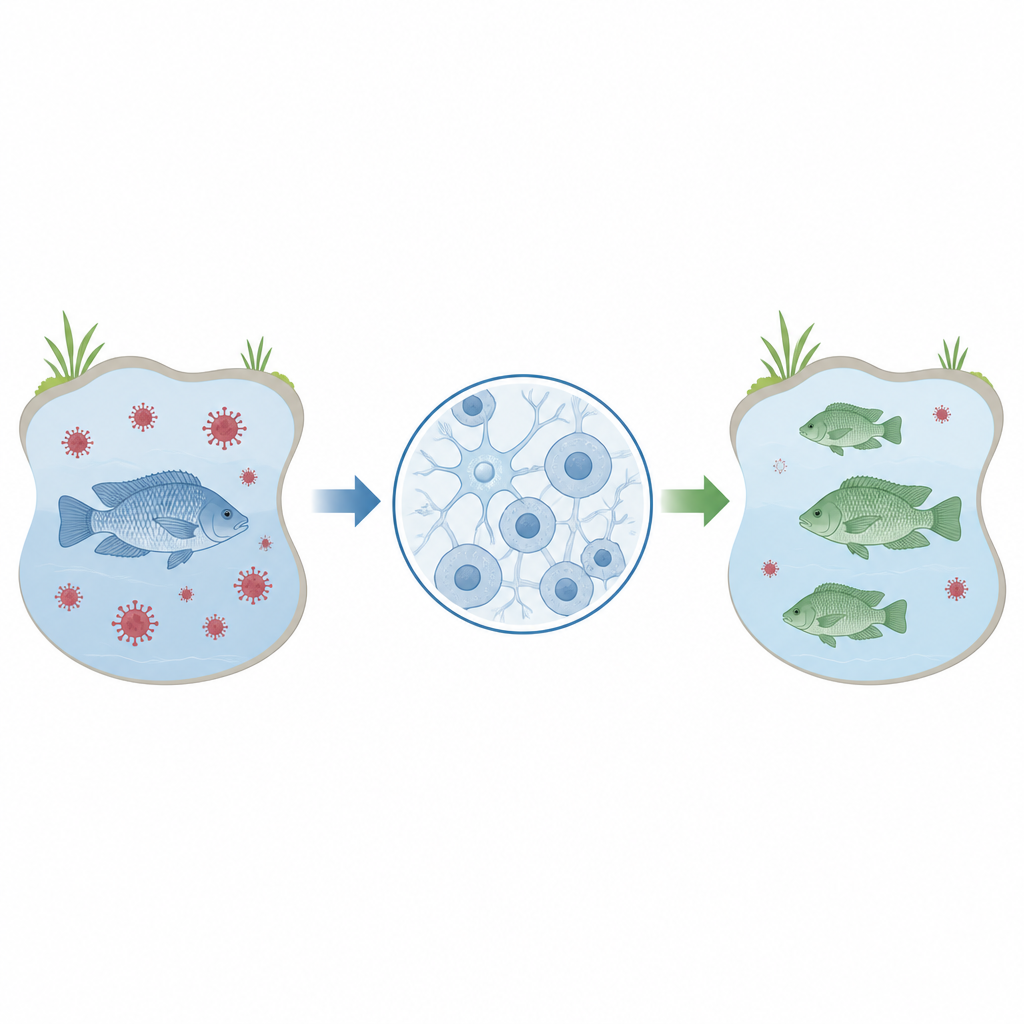
Tilapia ist weltweit ein Grundnahrungsmittel auf vielen Tellern, insbesondere in Regionen, in denen bezahlbares, hochwertiges Protein dringend benötigt wird. Gleichzeitig sind Tilapia-Farmen anfällig für Viruskrankheiten wie das Tilapia-Lake-Virus, das Bestände auslöschen und Existenzen bedrohen kann. Diese Studie beschreibt eine laborgestützte Methode, um Tilapia-Gene in Gehirnzellen schnell und präzise zu verändern und schafft damit die Grundlage für künftige Arbeiten, die darauf abzielen, Fische zu züchten, die besser gegen Krankheiten gewappnet sind und so die globale Ernährungssicherheit unterstützen.
Fische an der Front der Ernährungssicherheit
Die Aquakultur liefert bereits etwa ein Sechstel des weltweit verzehrten tierischen Proteins, und Tilapia gehören zu den am einfachsten und am häufigsten gezüchteten Fischen. Sie wachsen schnell, tolerieren dicht besetzte Teiche und sind allgemein robust. Traditionelle Zuchtmethoden zur Verbesserung von Merkmalen wie Wachstum und Krankheitsresistenz sind jedoch langsam und durch die natürliche Variabilität einer Population begrenzt. Genomeditierung bietet einen Weg, nützliche genetische Veränderungen in einer einzigen Generation einzuführen, was besonders wertvoll für Merkmale wie Resistenz gegenüber schweren Virusinfektionen in der Zuchtfischproduktion sein könnte.
Aufbau eines nützlichen Zellmodells
Die Forschenden konzentrierten sich auf eine Zelllinie namens OmB, die aus dem Gehirn der Mozambique-Tilapia stammt. Diese Zellen sind dafür bekannt, vom Tilapia-Lake-Virus infiziert zu werden, was sie zu einem praktischen Modell macht, um zu untersuchen, wie das Virus mit seinem Wirt interagiert. Bevor solche Zellen breit genutzt werden können, um zu testen, welche Gene Infektion oder Resistenz beeinflussen, benötigen Wissenschaftler eine zuverlässige, effiziente Methode, um gezielt Gene in diesen Zellen zu verändern und anschließend die Folgen zu messen. Diese Studie zielte darauf ab, ein schrittweises Protokoll genau dafür mit einem verbreiteten Gen-Editierungswerkzeug namens CRISPR zu optimieren.
Feinabstimmung des Editierungswerkzeugs
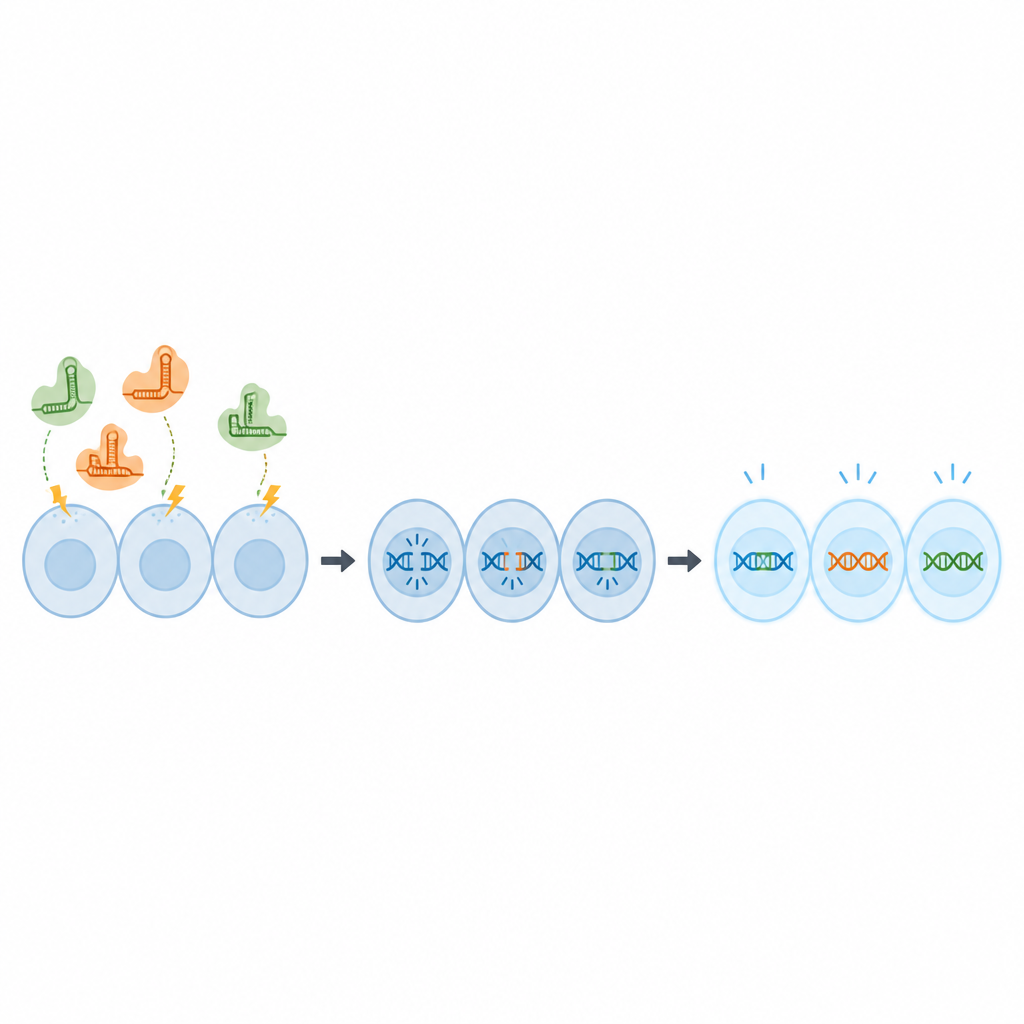
Anstatt CRISPR-Komponenten als DNA zu verabreichen, die in Zellen verbleiben und Sicherheitsbedenken aufwerfen kann, verwendete das Team fertige Protein‑RNA‑Komplexe, sogenannte Ribonukleoproteine. Diese wurden mittels kurzer elektrischer Pulse in OmB‑Zellen eingebracht — eine Technik namens Elektroporation. Zuerst testeten die Wissenschaftler mit einem fluoreszierenden Tracer verschiedene Kombinationen aus Spannung, Pulsdauer und Konzentration, um Bedingungen zu finden, die den Tracer in nahezu alle Zellen beförderten, ohne deren Überleben zu beeinträchtigen. Sie stellten fest, dass eine Tracer-Konzentration von 2 Mikromolar und eine bestimmte Puls-Einstellung nahezu vollständige Aufnahme bei gesunden Zellen ermöglichte.
Testen und Nachweisen der Methode
Im nächsten Schritt überprüfte das Team, ob diese Bedingungen tatsächlich Gene verändern können. Sie verwendeten eine Variante der OmB-Zelllinie, die grün leuchtet, und entwarfen CRISPR-Moleküle, um das Gen für das grüne Protein zu schneiden. Unter den optimierten elektrischen Einstellungen wurden fast 80 Prozent der Genkopien editiert, und zwei Wochen später leuchtete nur noch ein kleiner Bruchteil der Zellen, was zeigte, dass das Gen effektiv abgeschaltet worden war. Die Forschenden gingen anschließend zu zwei normalen Tilapia-Genen über, die ausgewählt wurden, weil ihre Veränderung die Zellen nicht tötet, aber eine klare Auslese ermöglicht. Mit demselben Protokoll erreichten sie Editierraten von etwa 67 bis 70 Prozent und eine starke vorhergesagte Funktionsausfallrate der Gene.
Was das für die künftige Fischgesundheit bedeutet
Die Arbeit liefert ein praktisches Rezept für hoch effiziente Genomeditierung in einer weit verbreiteten Tilapia-Gehirnzelllinie. Indem gezeigt wurde, dass CRISPR-Komponenten sicher eingebracht werden können und sowohl Marker- als auch native Gene in den meisten Zellen gestört werden können, verwandelt die Studie OmB-Zellen in ein leistungsfähiges Testsystem. Forschende können nun Kandidatengene einfacher ein- oder ausschalten, um zu untersuchen, wie sie Infektionen, Stressreaktionen oder andere Merkmale beeinflussen. Zwar hat diese Studie noch keine krankheitsresistenten Fische erzeugt, doch sie stellt ein wichtiges Werkzeug bereit, das Wissenschaftlerinnen und Wissenschaftlern helfen wird, die genetischen Veränderungen zu identifizieren, die am wahrscheinlichsten machen, dass Zuchttilapia künftig widerstandsfähiger werden.
Zitation: Wang, J., Bobrik, M., Pankaew, N. et al. Efficient genome editing in a Mozambique tilapia cell line using CAS ribonucleoprotein complexes. Sci Rep 16, 15125 (2026). https://doi.org/10.1038/s41598-026-42702-w
Schlüsselwörter: tilapia, Aquakultur, CRISPR, Fischkrankheit, Genomeditierung