Clear Sky Science · nl
Efficiënte genbewerking in een Mozambikaanse tilapia-celijn met behulp van CAS ribonucleoproteïnecomplexen
Waarom deze studie belangrijk is voor vis en voedsel
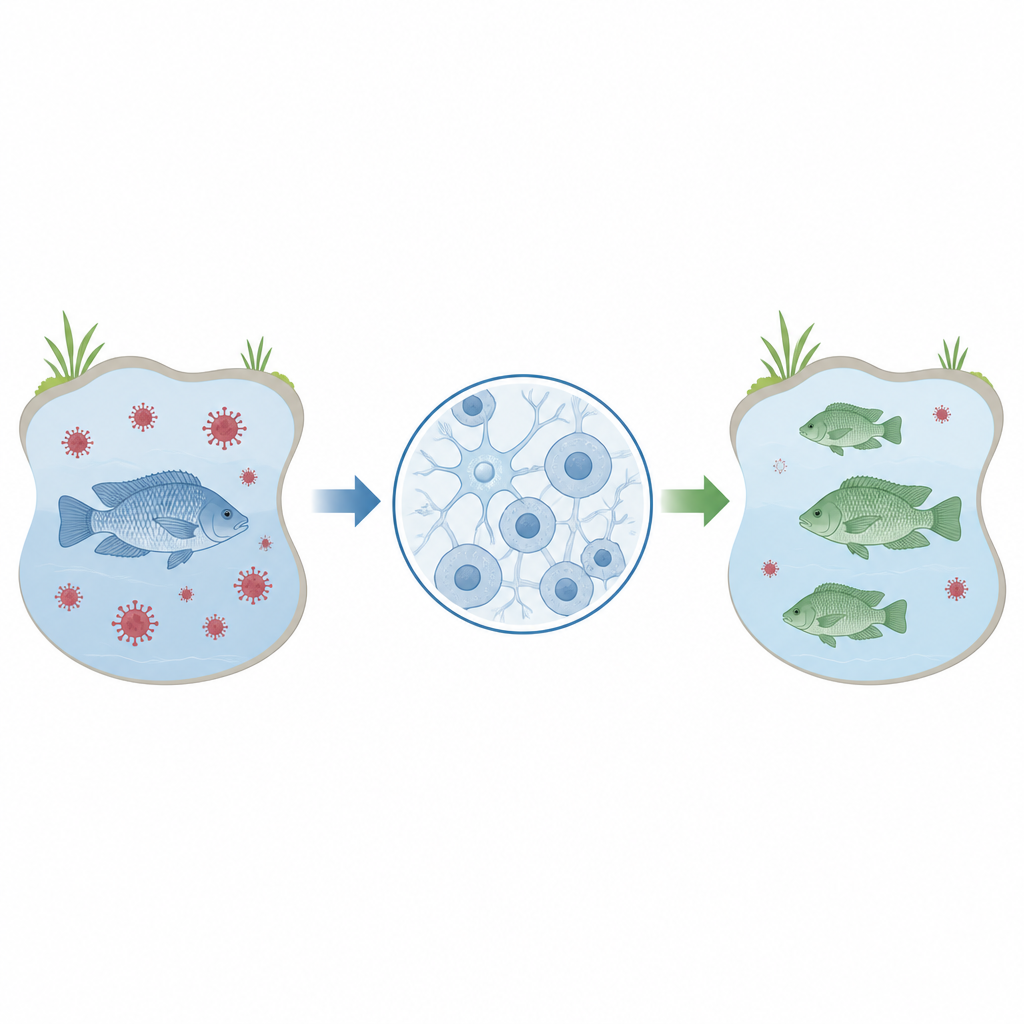
Tilapia is een veelgegeten vis op bordjes wereldwijd, vooral in regio’s waar betaalbaar, eiwitrijk voedsel hard nodig is. Toch zijn tilapiabedrijven kwetsbaar voor virale ziekteverwekkers zoals Tilapia lake virus, die voor grote sterfte en economische schade kunnen zorgen. Deze studie beschrijft een labmethode om snel en nauwkeurig tilapiagenen in hersencellen te bewerken, en legt daarmee de basis voor toekomstig werk om vissen te kweken die beter tegen ziekte kunnen en zo de voedselzekerheid ondersteunen.
Vissen in de frontlinie van voedselzekerheid
Aquacultuur levert al ongeveer een zesde van het dierlijke eiwit dat wereldwijd wordt gegeten, en tilapia’s behoren tot de gemakkelijkst en meest voorkomende te kweken vissoorten. Ze groeien snel, verdragen dichte populaties in vijvers en zijn over het algemeen robuust. Traditionele selectieve fokkerij om eigenschappen als groei en ziektebestendigheid te verbeteren is echter traag en beperkt door de natuurlijke variatie in een kweekstam. Genbewerking biedt een manier om nuttige genetische veranderingen in één generatie in te voeren, wat vooral waardevol kan zijn voor eigenschappen zoals resistentie tegen ernstige virale infecties bij gekweekte vissen.
Het bouwen van een bruikbaar celmodel
De onderzoekers richtten zich op een celijn genaamd OmB, afkomstig uit de hersenen van Mozambikaanse tilapia. Deze cellen kunnen worden geïnfecteerd door Tilapia lake virus, wat ze praktisch maakt om te bestuderen hoe het virus met zijn gastheer omgaat. Voordat zulke cellen breed kunnen worden ingezet om te testen welke genen invloed hebben op infectie of resistentie, hebben wetenschappers een betrouwbare, efficiënte manier nodig om specifieke genen in deze cellen aan te passen en vervolgens te meten wat er gebeurt. Deze studie had als doel een stapsgewijs protocol te verfijnen om precies dat te doen met behulp van een veelgebruikt genbewerkinstrument, bekend als CRISPR.
De bewerkingstool verfijnen
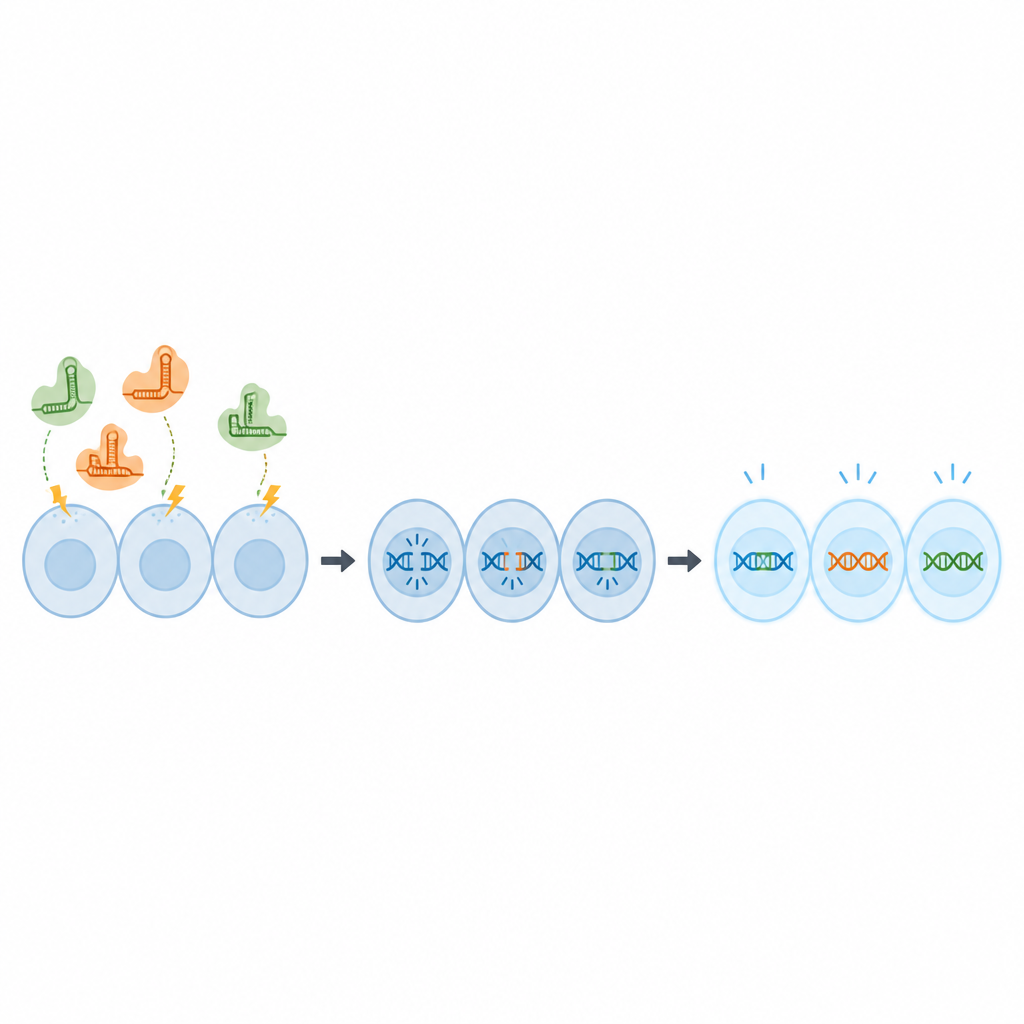
In plaats van CRISPR-componenten als DNA af te leveren — wat in cellen kan achterblijven en veiligheidsvragen oproept — gebruikte het team kant-en-klare eiwit-RNA-complexen, bekend als ribonucleoproteïnen. Deze werden met korte elektrische pulsen in OmB-cellen gebracht via een techniek die electroporatie heet. Eerst gebruikten de wetenschappers een fluorescerende tracermolecuul om verschillende combinaties van spanning, pulslengte en concentratie te testen, op zoek naar instellingen die de tracer in bijna alle cellen brachten zonder hun overleving te schaden. Ze vonden dat een tracerconcentratie van 2 micromolair en een specifieke pulsinstelling vrijwel volledige opname gaf met gezonde cellen.
De methode testen en aantonen
Vervolgens vroegen de onderzoekers of deze condities daadwerkelijk genen konden veranderen. Ze gebruikten een versie van de OmB-celijn die groen oplichtte en ontwierpen CRISPR-moleculen om het gen voor het groene eiwit te knippen. Onder de geoptimaliseerde elektrische instellingen werden bijna 80 procent van de genkopieën bewerkt, en twee weken later straalde nog maar een klein deel van de cellen groen, wat aantoont dat het gen effectief was uitgeschakeld. De wetenschappers gingen toen verder met twee normale tilapiagenen, geselecteerd omdat wijziging daarvan de cellen niet doodt maar wel een duidelijk resultaat oplevert. Met hetzelfde protocol behaalden ze bewerkingspercentages van ongeveer 67 tot 70 procent en sterke voorspelde uitval (knockout) van genfunctie.
Wat dit betekent voor toekomstige visgezondheid
Het werk levert een praktisch recept voor zeer efficiënte genbewerking in een veelgebruikte tilapia-hersencelijn. Door aan te tonen dat CRISPR-componenten veilig kunnen worden afgeleverd en dat zowel marker- als inheemse genen in de meeste cellen kunnen worden verstoord, verandert de studie OmB-cellen in een krachtig testplatform. Onderzoekers kunnen nu gemakkelijker kandidaatgenen aan- of uitzetten om te zien hoe ze virale infectie, stressreacties of andere eigenschappen beïnvloeden. Hoewel deze studie nog geen ziektebestendige vissen heeft geproduceerd, biedt ze een belangrijk hulpmiddel dat onderzoekers zal helpen de genetische veranderingen te identificeren die waarschijnlijk het meest bijdragen aan robuustere gekweekte tilapia in de toekomst.
Bronvermelding: Wang, J., Bobrik, M., Pankaew, N. et al. Efficient genome editing in a Mozambique tilapia cell line using CAS ribonucleoprotein complexes. Sci Rep 16, 15125 (2026). https://doi.org/10.1038/s41598-026-42702-w
Trefwoorden: tilapia, aquacultuur, CRISPR, visziekte, genbewerking