Clear Sky Science · it
Modifica efficace del genoma in una linea cellulare di tilapia del Mozambico usando complessi ribonucleoproteici CAS
Perché questo studio è importante per il pesce e per il cibo
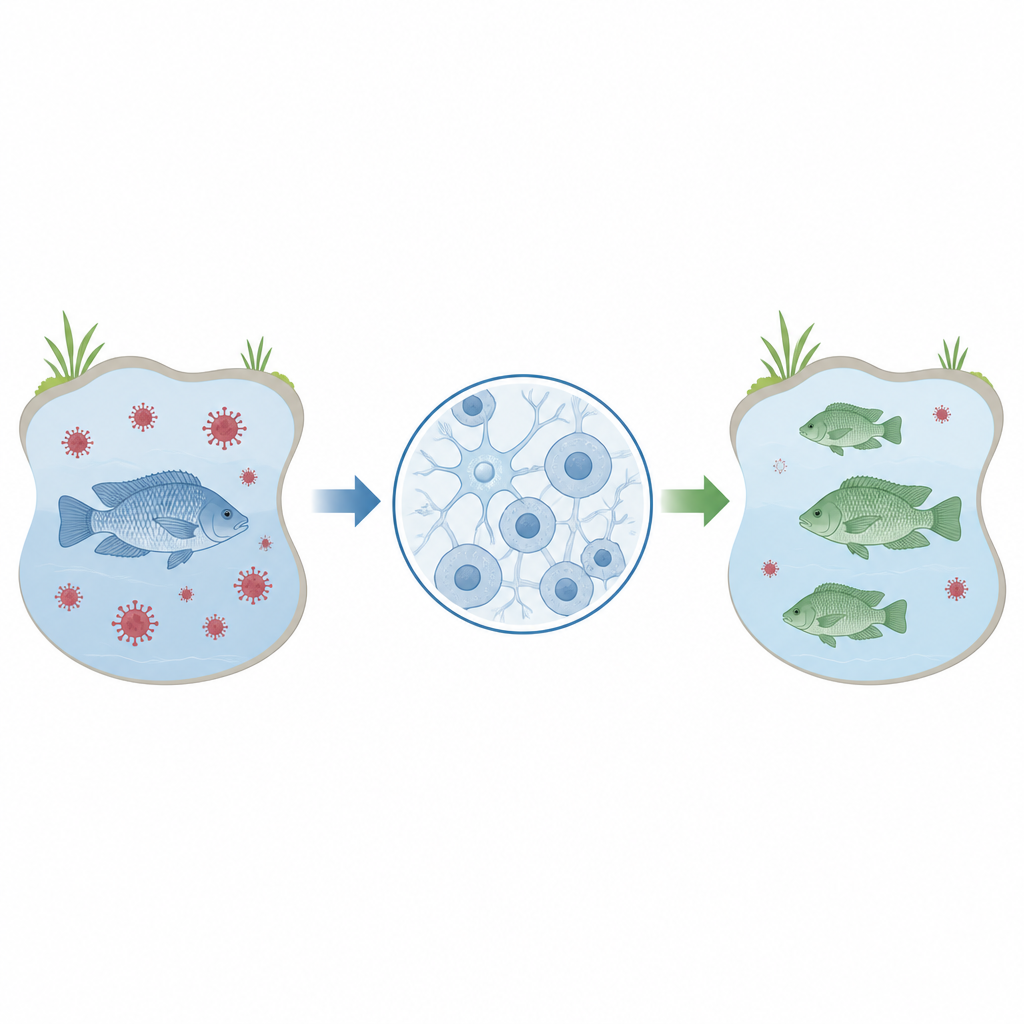
La tilapia è un pesce fondamentale sulle tavole di tutto il mondo, soprattutto in regioni dove è urgente disporre di proteine di qualità a basso costo. Tuttavia gli allevamenti di tilapia sono vulnerabili a malattie virali come il Tilapia lake virus, che possono decimare gli stock e minacciare i mezzi di sussistenza. Questo studio descrive un metodo in vitro per modificare rapidamente e con precisione i geni della tilapia in cellule cerebrali, gettando le basi per lavori futuri volti a selezionare pesci più resistenti alle malattie e a sostenere la sicurezza alimentare globale.
I pesci in prima linea per la sicurezza alimentare
L’acquacoltura fornisce già circa un sesto delle proteine animali consumate a livello globale, e la tilapia è tra i pesci più facili e comuni da allevare. Cresce rapidamente, tollera stagni affollati ed è generalmente robusta. Tuttavia, l’allevamento selettivo tradizionale per migliorare tratti come crescita e resistenza alle malattie è lento e limitato dalla variazione naturale presente nello stock. La modifica del genoma offre un modo per introdurre cambiamenti genetici utili in una singola generazione, il che potrebbe essere particolarmente utile per tratti come la resistenza a infezioni virali gravi negli allevamenti.
Costruire un modello cellulare utile
I ricercatori si sono concentrati su una linea cellulare chiamata OmB, derivata dal cervello della tilapia del Mozambico. Queste cellule sono note per essere infettate dal Tilapia lake virus, il che le rende un sostituto pratico per studiare come il virus interagisce con l’ospite. Prima che tali cellule possano essere ampiamente usate per testare quali geni influenzano l’infezione o la resistenza, gli scienziati hanno bisogno di un modo affidabile ed efficiente per modificare geni specifici in queste cellule e poi misurare gli effetti. Questo studio si è proposto di mettere a punto un protocollo passo dopo passo per fare esattamente questo usando uno strumento di editing genico diffuso noto come CRISPR.
Ottimizzare lo strumento di editing
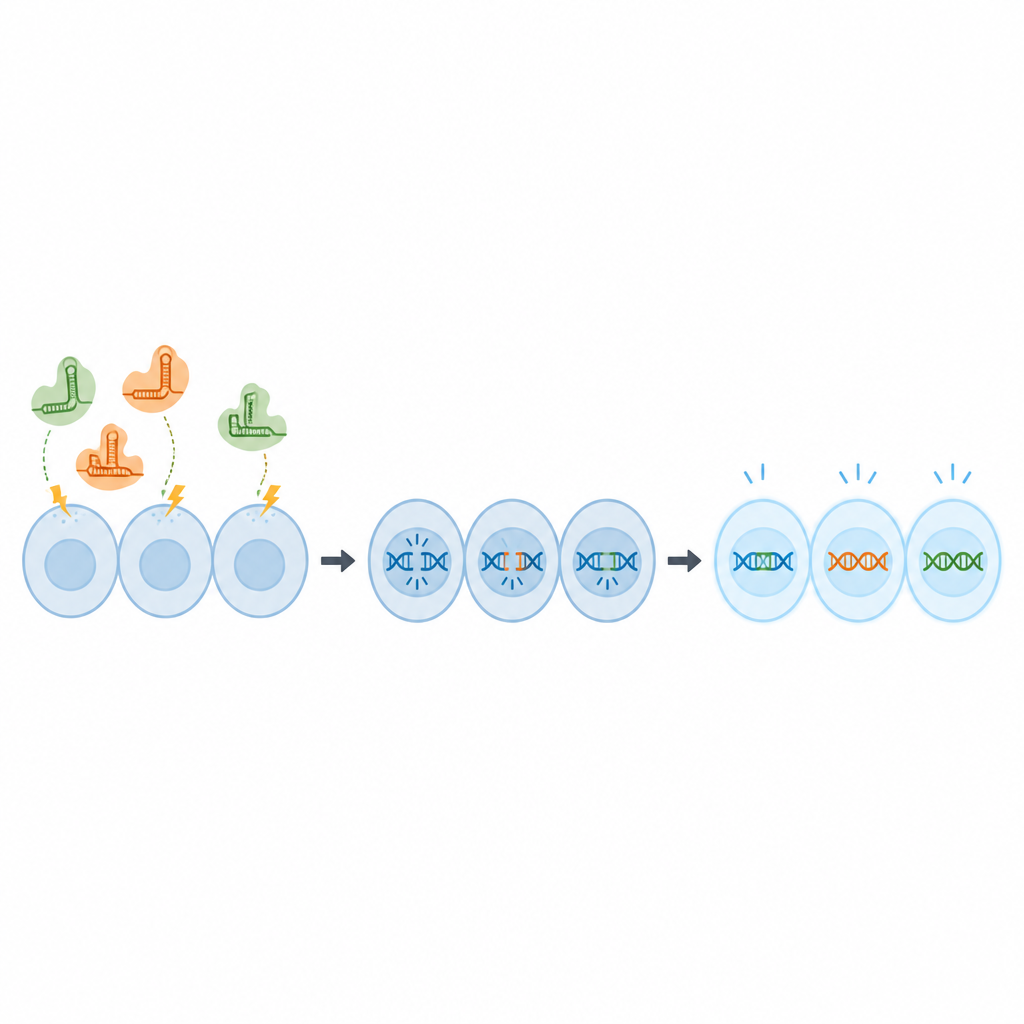
Invece di somministrare componenti CRISPR come DNA, che può persistere nelle cellule e sollevare preoccupazioni di sicurezza, il team ha usato complessi proteina-RNA pronti all’uso noti come ribonucleoproteine. Questi sono stati introdotti nelle cellule OmB mediante brevi impulsi elettrici in una tecnica chiamata elettroporazione. Per prima cosa, gli scienziati hanno usato una molecola tracciante fluorescente per testare diverse combinazioni di tensione, durata dell’impulso e concentrazione, cercando condizioni che portassero il tracciante nella quasi totalità delle cellule senza compromettere la loro sopravvivenza. Hanno trovato che una concentrazione di 2 micromolari del tracciante e un’impostazione di impulso specifica garantivano un’assunzione quasi completa con cellule in buona salute.
Testare e dimostrare il metodo
Successivamente il team ha verificato se queste condizioni potessero effettivamente modificare i geni. Hanno usato una versione della linea cellulare OmB che emetteva fluorescenza verde e hanno progettato molecole CRISPR per tagliare il gene della proteina verde. Con le impostazioni elettriche ottimizzate, quasi l’80 percento delle copie geniche è stato modificato, e due settimane dopo solo una piccola frazione di cellule continuava a brillare, dimostrando che il gene era stato efficacemente spento. I ricercatori hanno poi proseguito con due geni normali della tilapia, scelti perché la loro alterazione non uccide le cellule ma fornisce un chiaro riscontro. Usando lo stesso protocollo, hanno ottenuto tassi di editing di circa il 67-70 percento e una forte previsione di knockout della funzione genica.
Cosa significa per la salute dei pesci in futuro
Il lavoro fornisce una ricetta pratica per l’editing genico ad alta efficienza in una linea cellulare cerebrale di tilapia ampiamente usata. Dimostrando che i componenti CRISPR possono essere consegnati in sicurezza e che sia i geni marcatore sia quelli nativi possono essere interrotti nella maggior parte delle cellule, lo studio trasforma le cellule OmB in un potente banco di prova. I ricercatori possono ora spegnere o attivare più facilmente geni candidati per vedere come influenzano l’infezione virale, le risposte allo stress o altri tratti. Sebbene questo studio non abbia ancora creato tilapie resistenti alle malattie, fornisce uno strumento chiave che aiuterà gli scienziati a identificare i cambiamenti genetici più probabili per rendere gli allevamenti di tilapia più resilienti in futuro.
Citazione: Wang, J., Bobrik, M., Pankaew, N. et al. Efficient genome editing in a Mozambique tilapia cell line using CAS ribonucleoprotein complexes. Sci Rep 16, 15125 (2026). https://doi.org/10.1038/s41598-026-42702-w
Parole chiave: tilapia, acquacoltura, CRISPR, malattie dei pesci, modifica del genoma