Clear Sky Science · zh
表观遗传调节剂地西他滨与二甲双胍协同诱导胃癌细胞凋亡,凸显联合治疗的潜力
本研究为何重要
胃癌是全球致死率较高的癌症之一,部分原因在于肿瘤常对标准化疗产生耐药。本研究探讨将两种已获批准的药物——一种用于血液疾病、另一种用于糖尿病——配对使用,是否能协同促使胃癌细胞走向自我毁灭,从而为未来更安全、更有效的治疗组合提供线索。
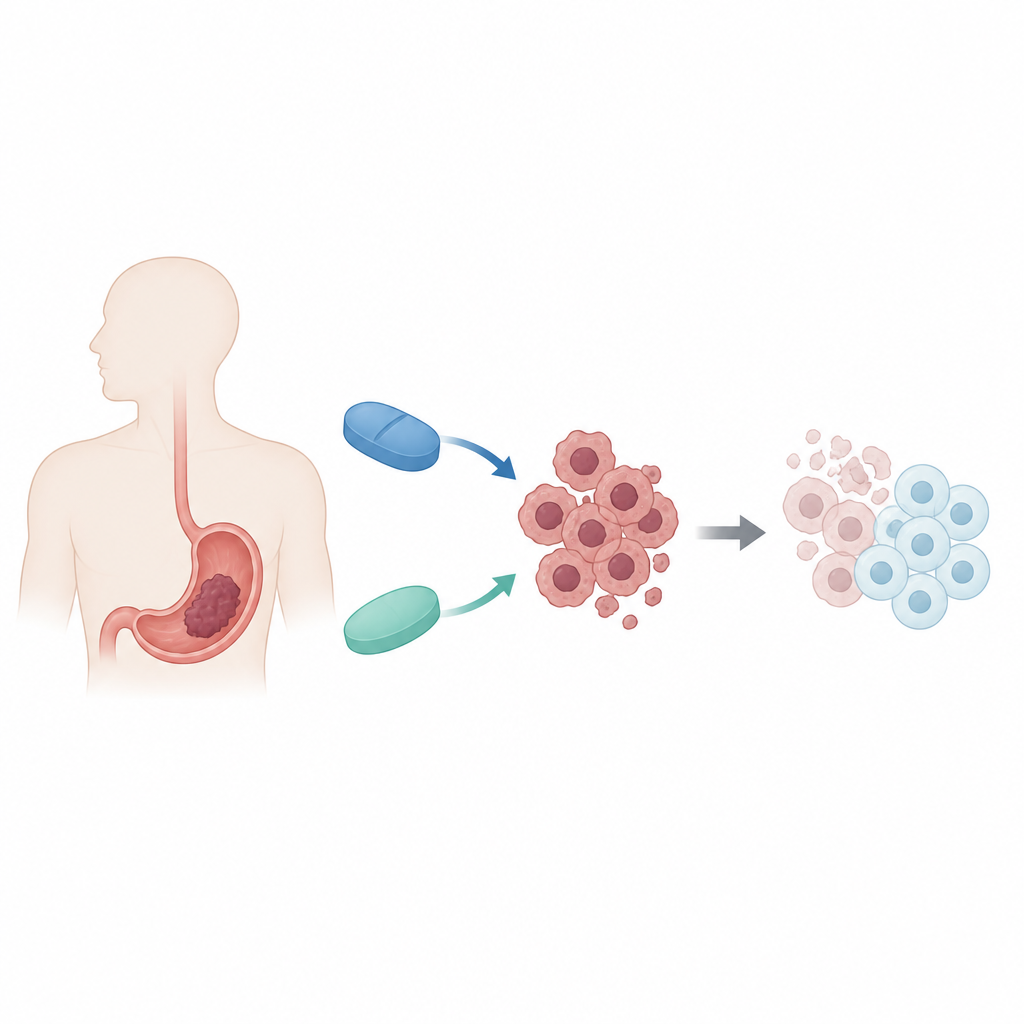
两种熟悉的药物,新颖的组合
研究人员关注的是两种主要作用各异的药物。地西他滨用于治疗某些骨髓相关恶性肿瘤,通过放松DNA上的化学标记来解除对保护性基因的沉默。二甲双胍是常用的降糖药,能改变细胞的能量代谢并激活细胞内的“燃料表”。两者单独均显示出一定的抗肿瘤活性,但在胃癌等实体瘤中效果有限。研究团队提出疑问:在人体胃癌细胞中将两者联用,是否可以同时利用肿瘤在基因调控和代谢方面的脆弱点。
评估对癌细胞存活的影响
研究者使用名为 MKN45 的人胃癌细胞系,先在数天内给出不同剂量的单药处理,再用固定剂量的药物组合。通过标准的比色法检测存活细胞数。一种用于评估药物相互作用的数学方法显示,联合用药降低了抑制细胞生长所需的剂量,并且在低至中等细胞杀伤水平下两药呈协同作用。换言之,两药合用的效果优于各自效应之和,同时可用较低剂量,尤其是降低二甲双胍的用量。
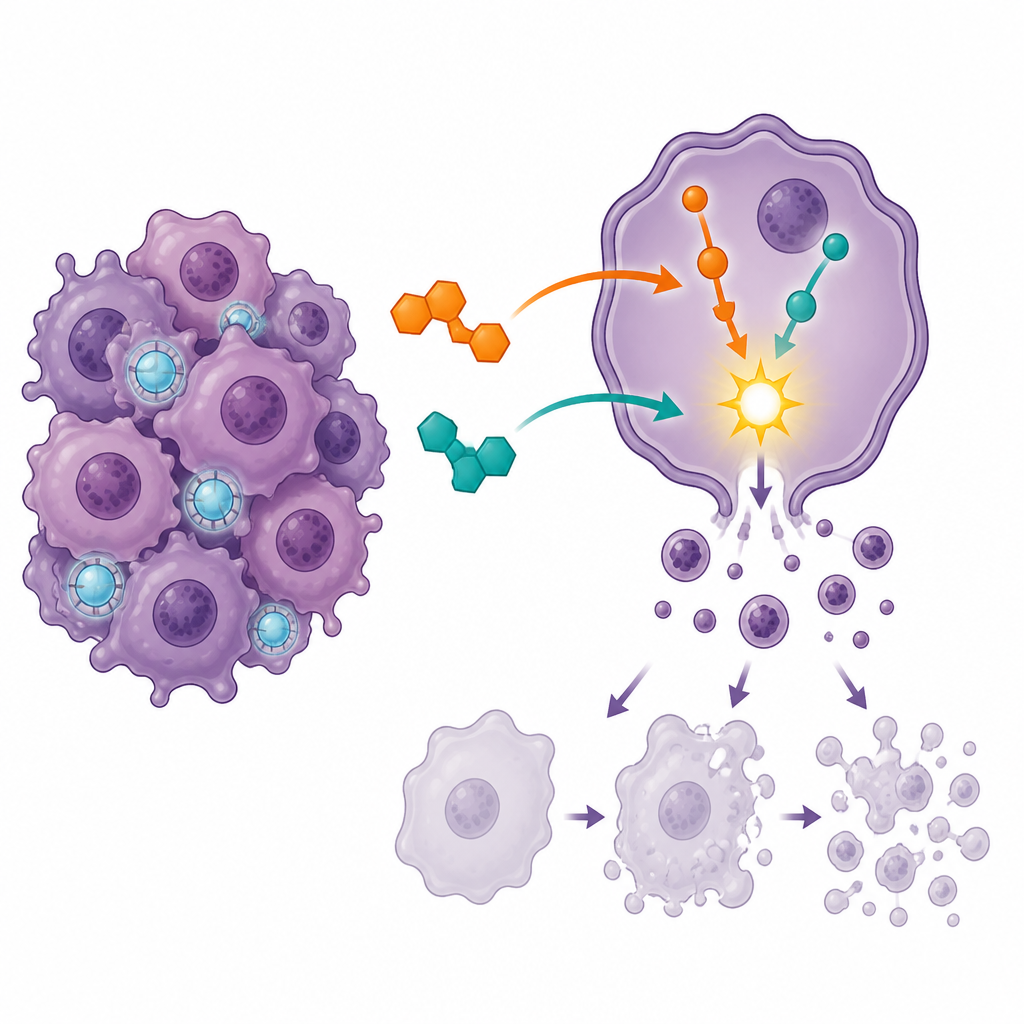
诱导细胞自杀并阻断细胞分裂
为观察药物对癌细胞的具体影响,团队使用流式细胞术,这一技术可区分存活细胞与处于不同程序性死亡阶段的细胞。单药处理均使更多细胞倾向于死亡,但联合用药导致晚期凋亡显著增加,完全存活细胞的比例下降。同时,大多数细胞在细胞周期的关键检查点 G2/M 阶段被迫暂停,该阶段是细胞准备分裂之时。这个在分裂阶段形成的严重“交通堵塞”表明,联合治疗将细胞困在一个脆弱时刻,从而更可能走向受控的自我毁灭,而不是继续增殖。
开启细胞内的死亡程序
研究人员随后检测了多种作为生存与死亡内部开关的基因表达水平。联合用药下,促凋亡基因如 BAX 及两种参与降解细胞成分的半胱天冬酶的表达上调,而通常帮助细胞抵抗死亡的 BCL2 表达下调。BAX 与 BCL2 之间的平衡明显向细胞自杀倾斜。另一个与自噬回收过程相关的基因 ATG7 也选择性上调,暗示在治疗下受控的细胞内部分解和清理可能与凋亡协同作用。基于计算的网络与通路分析证实,受影响的主要生物学主题包括凋亡通路、与 p53 蛋白相关的应激信号,以及与对标准铂类化疗药物耐药相关的路径。
这对未来治疗可能意味着什么
通俗地说,这项工作表明地西他滨和二甲双胍联用时,比单独使用任一药物更能使胃癌细胞停止分裂并激活其内在的自毁机制。通过同时针对错误的基因控制与异常的能量利用,这对药物似乎按下了癌细胞赖以生存和抵抗治疗的多个“关闭”开关。尽管目前的发现基于实验室培养的一种癌细胞类型,但它们提示,将表观遗传学药物与代谢调节药物联合使用可能有助于克服侵袭性胃癌的治疗耐药,并为在更多细胞模型乃至动物实验中测试该策略提供了有力依据。
引用: AlAli, M., Latifi-Navid, S. & Khakzad, M.R. Synergistic induction of apoptosis by the epigenetic modulator decitabine and metformin in gastric cancer cells highlights the potential for combination therapy. Sci Rep 16, 14951 (2026). https://doi.org/10.1038/s41598-026-42417-y
关键词: 胃癌, 地西他滨, 二甲双胍, 凋亡, 联合治疗