Clear Sky Science · sv
Synergistisk induktion av apoptos av den epigenetiska modulatorn decitabin och metformin i mags cancerceller belyser potentialen för kombinationsterapi
Varför denna studie är viktig
Magsäckscancer är en av de dödligaste cancerformerna globalt, delvis eftersom tumörer ofta är motståndskraftiga mot standardkemoterapi. Denna studie undersöker om paret av två redan godkända läkemedel—ett för blodsjukdomar och ett för diabetes—kan fungera tillsammans för att driva magsäcksceller mot självförstörelse, vilket potentiellt pekar på säkrare och mer effektiva behandlingskombinationer i framtiden.
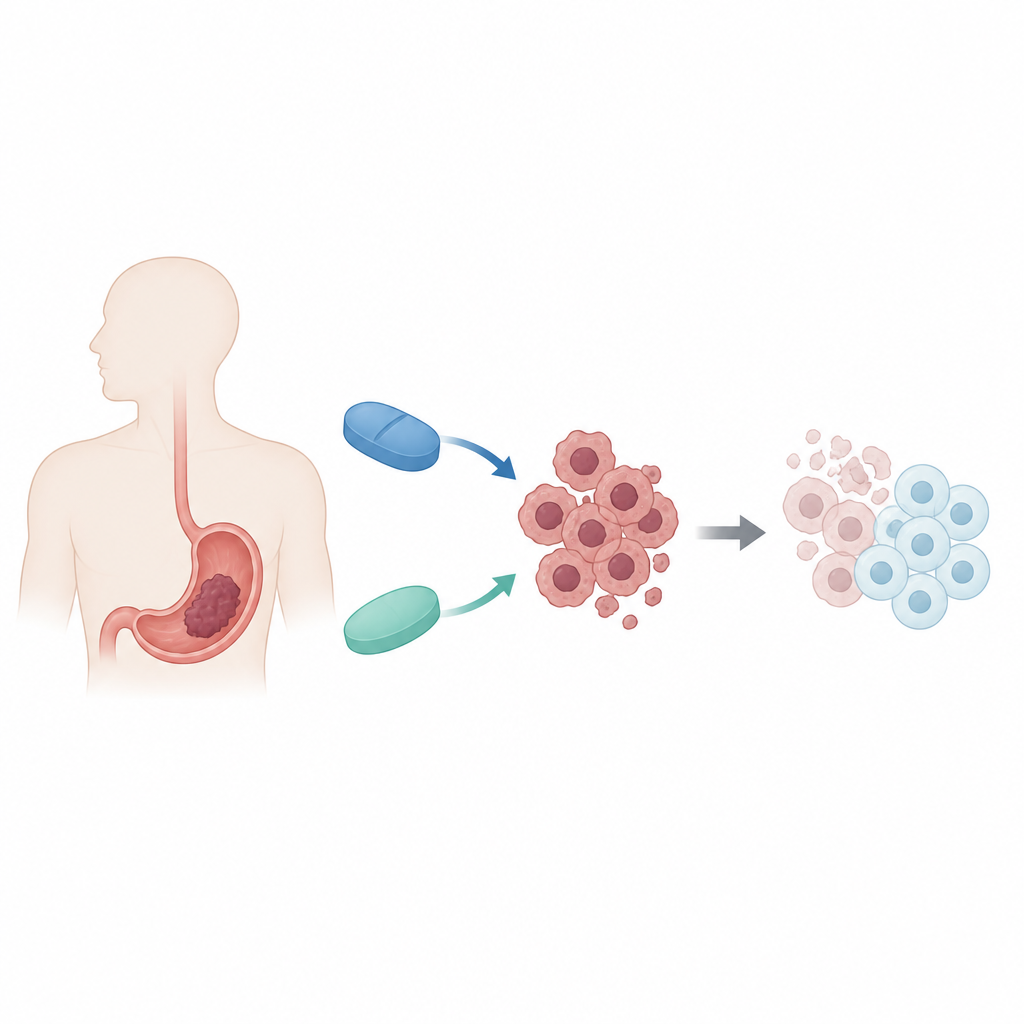
Två bekanta läkemedel, ett nytt partnerskap
Forskarlaget koncentrerade sig på två läkemedel med mycket olika huvuduppgifter. Decitabin används för att behandla vissa benmärgscancerformer genom att luckra upp kemiska märkningar på DNA som släcker skyddande gener. Metformin är ett vanligt diabetesläkemedel som förändrar hur celler hanterar energi och aktiverar en cellulär ”bränslemätare.” Båda har visat anticanceraktivitet var för sig, men bara måttliga effekter i solida tumörer som magsäckscancer. Forskarna undrade om användning av dem tillsammans i humana magsäcksceller skulle kunna utnyttja tumörens svagheter i både genkontroll och metabolism samtidigt.
Test av effekten på cancercellers överlevnad
Med hjälp av en human magsäckscellinje kallad MKN45 exponerade forskarna först celler för en rad doser av varje läkemedel ensamt under flera dagar, och sedan för fasta dospar av de två läkemedlen tillsammans. De mätte hur många celler som förblev levande med ett standardiserat färgbaserat labbtest. En matematisk metod som utvärderar hur läkemedel interagerar visade att kombinationen minskade den dos som krävdes för att hämma celltillväxt och att de två läkemedlen agerade synergistiskt vid låga till måttliga dödlighetsnivåer. Med andra ord var de tillsammans mer effektiva än vad som kunde förväntas av att bara lägga ihop deras individuella effekter, samtidigt som lägre doser kunde användas, särskilt av metformin.
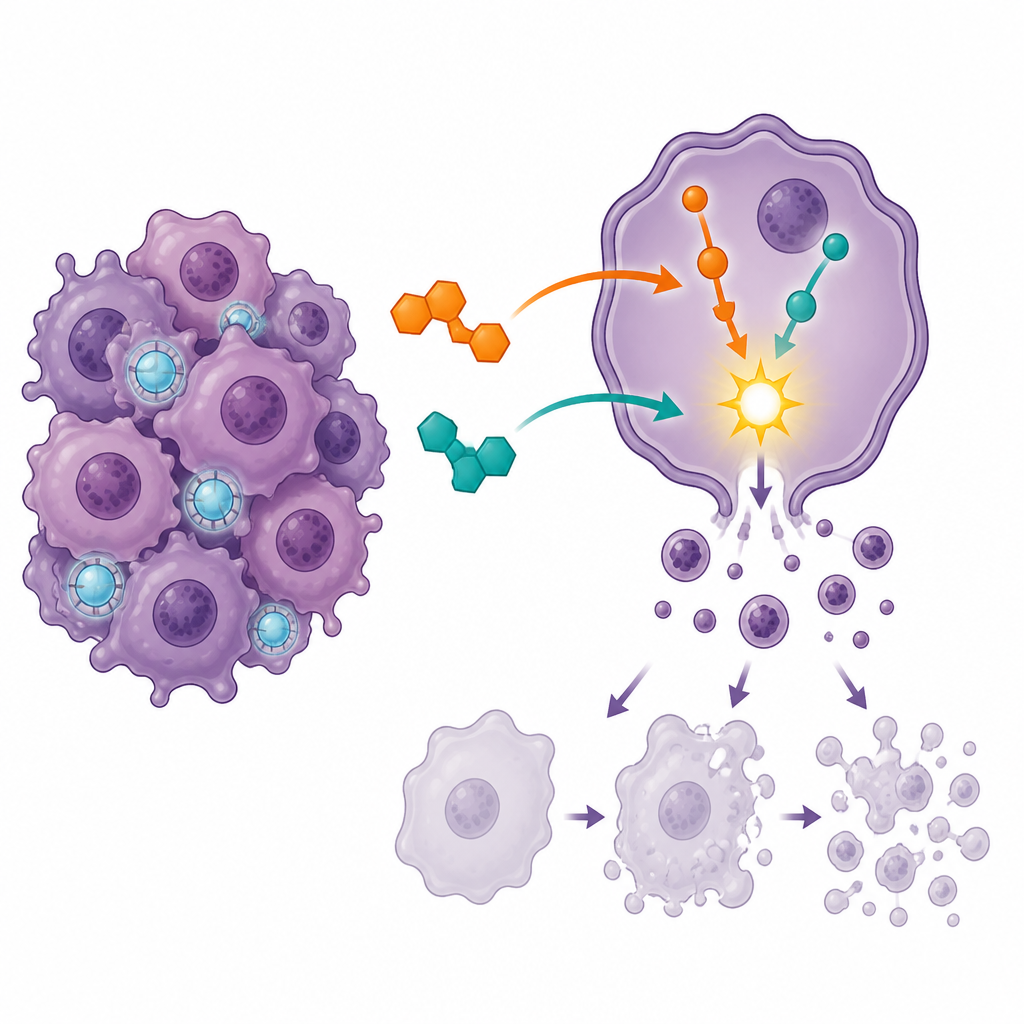
Utlösning av celldöd och stopp av celldelning
För att se hur läkemedlen påverkade cancercellerna använde teamet flödescytometri, en teknik som kan särskilja levande celler från dem i olika stadier av programmerad celldöd, eller apoptos. Var och en av läkemedlen försiggick att fler celler gick mot död, men kombinationen orsakade en mycket större ökning av sena stadier av apoptos och minskade andelen fullständigt livskraftiga celler. Samtidigt tvingades de flesta celler att pausa vid en viktig kontrollpunkt i cellcykeln känd som G2/M, där celler normalt förbereder sig för delning. Denna starka trafikstockning vid delningsstadiet tyder på att den kombinerade behandlingen fångar celler i ett sårbart ögonblick, varefter de är mer benägna att genomgå kontrollerad självförstörelse istället för att fortsätta multiplicera sig.
Aktivering av dödsprogram inuti cellen
Forskarna tittade sedan på aktivitetsnivåer för flera gener som fungerar som interna strömbrytare för överlevnad och död. Vid läkemedelskombinationen ökade uttrycket av gener som främjar apoptos, såsom BAX och två kaspaser som sönderdelar cellulära komponenter, medan BCL2, en gen som normalt hjälper celler att motstå död, minskade. Balansen mellan BAX och BCL2 försköts kraftigt till förmån för celldöd. En annan gen, ATG7, som hjälper till att hantera en återvinningsprocess kallad autofagi, ökade också selektivt, vilket antyder att kontrollerad nedbrytning och städning inuti cellen kan samverka med apoptos under behandlingen. Datorbaserade nätverks- och vägledningsanalyser bekräftade att de huvudsakliga biologiska teman som påverkades var apoptosvägar, stressignaler kopplade till p53-proteinet och vägar relaterade till motstånd mot standard kemoterapier baserade på platina.
Vad detta kan innebära för framtida behandlingar
Enkelt uttryckt visar detta arbete att decitabin och metformin, när de används tillsammans, gör magsäcksceller mer benägna att sluta dela sig och att aktivera sin inbyggda självdestruktionsmaskineri än när något av läkemedlen används ensam. Genom att gemensamt rikta in sig på felaktig genkontroll och onormal energianvändning verkar paret trycka på flera ”av”-knappar som cancern litar på för att överleva och motstå behandling. Även om fynden hittills kommer från en celltyp odlad i laboratoriet, antyder de att kombinationer av epigenetiska och metabola läkemedel kan hjälpa till att övervinna behandlingsresistens i aggressiva magsäckscancerformer, och de ger ett starkt skäl att testa denna strategi i ytterligare cellmodeller och så småningom i djurstudier.
Citering: AlAli, M., Latifi-Navid, S. & Khakzad, M.R. Synergistic induction of apoptosis by the epigenetic modulator decitabine and metformin in gastric cancer cells highlights the potential for combination therapy. Sci Rep 16, 14951 (2026). https://doi.org/10.1038/s41598-026-42417-y
Nyckelord: magsäckscancer, decitabin, metformin, apoptos, kombinationsterapi