Clear Sky Science · ja
エピジェネティック修飾剤デシタビンとメトホルミンが胃がん細胞で相乗的にアポトーシスを誘導することは併用療法の可能性を示唆する
この研究が重要な理由
胃がんは世界的に致死性の高いがんの一つであり、その一因は腫瘍が標準化学療法にしばしば抵抗することにあります。本研究は、血液疾患治療薬と糖尿病治療薬という既承認の二つの薬剤を組み合わせることで、胃がん細胞を自己破壊へと追い込めるかを検討し、将来的により安全で効果的な治療の組み合わせを示唆し得るかを探っています。
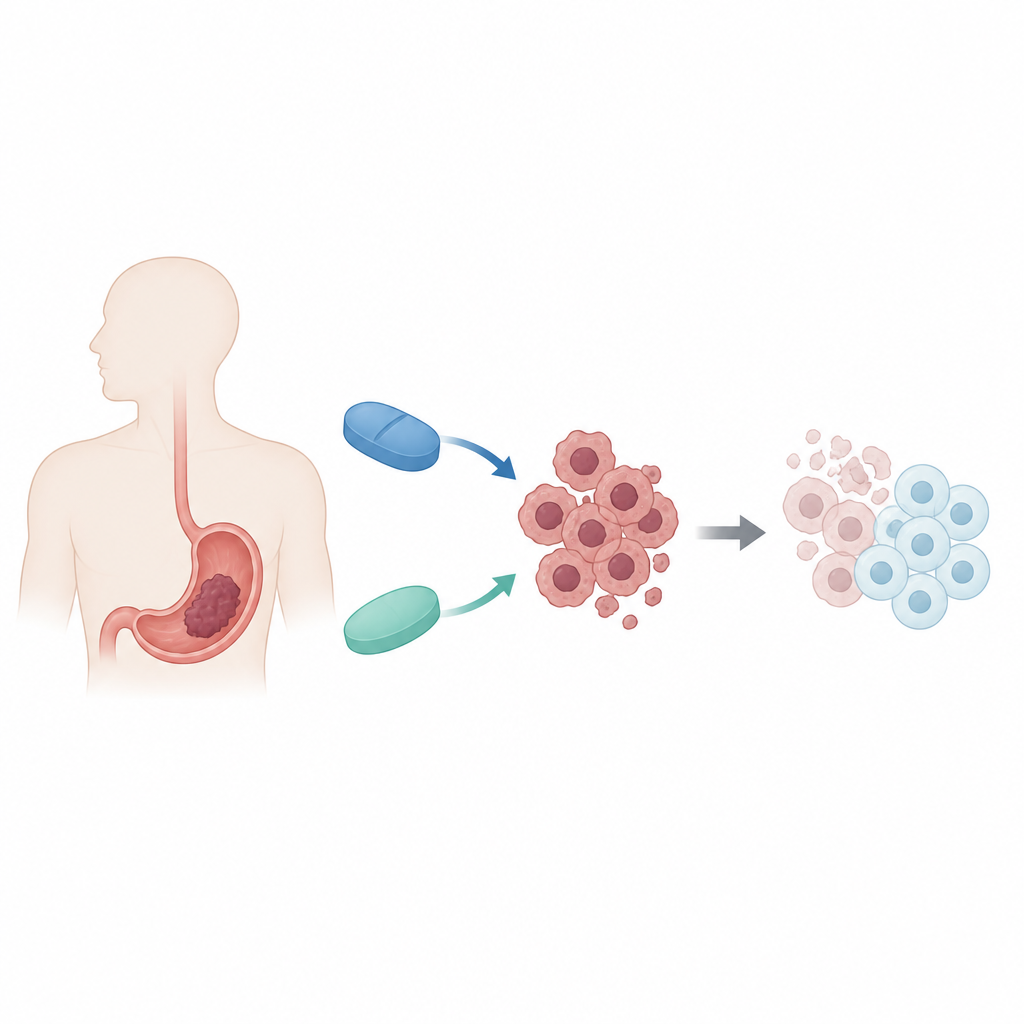
馴染みのある二つの薬、新たな協力関係
研究者たちは主作用が大きく異なる二つの薬に着目しました。デシタビンはDNA上の遺伝子を沈黙させる化学的タグを緩めることで一部の骨髄系がんを治療する薬です。メトホルミンは細胞のエネルギー代謝を変え、細胞の「燃料計」を活性化する一般的な糖尿病薬です。両者は単独で抗がん作用を示すことがありますが、胃がんのような固形腫瘍では効果は限定的でした。研究チームは、これらをヒト胃がん細胞で同時に用いることで、遺伝子制御と代謝という腫瘍の弱点を同時に突けるかを検討しました。
がん細胞の生存への影響を検証
研究ではヒト胃がん細胞株MKN45を用い、まず各薬剤を単独で数日間にわたり濃度を変えて曝露し、その後、固定用量で二剤を併用しました。細胞生存率は標準的な色素反応による実験で測定されました。薬物相互作用を評価する数学的手法により、併用は細胞増殖抑制に必要な用量を低減させ、低〜中程度の細胞死レベルでは二剤が相乗的に作用することが示されました。つまり、併用は単純にそれぞれの効果を足した以上の効果を示し、とくにメトホルミンの用量を下げられる可能性があることを示しています。
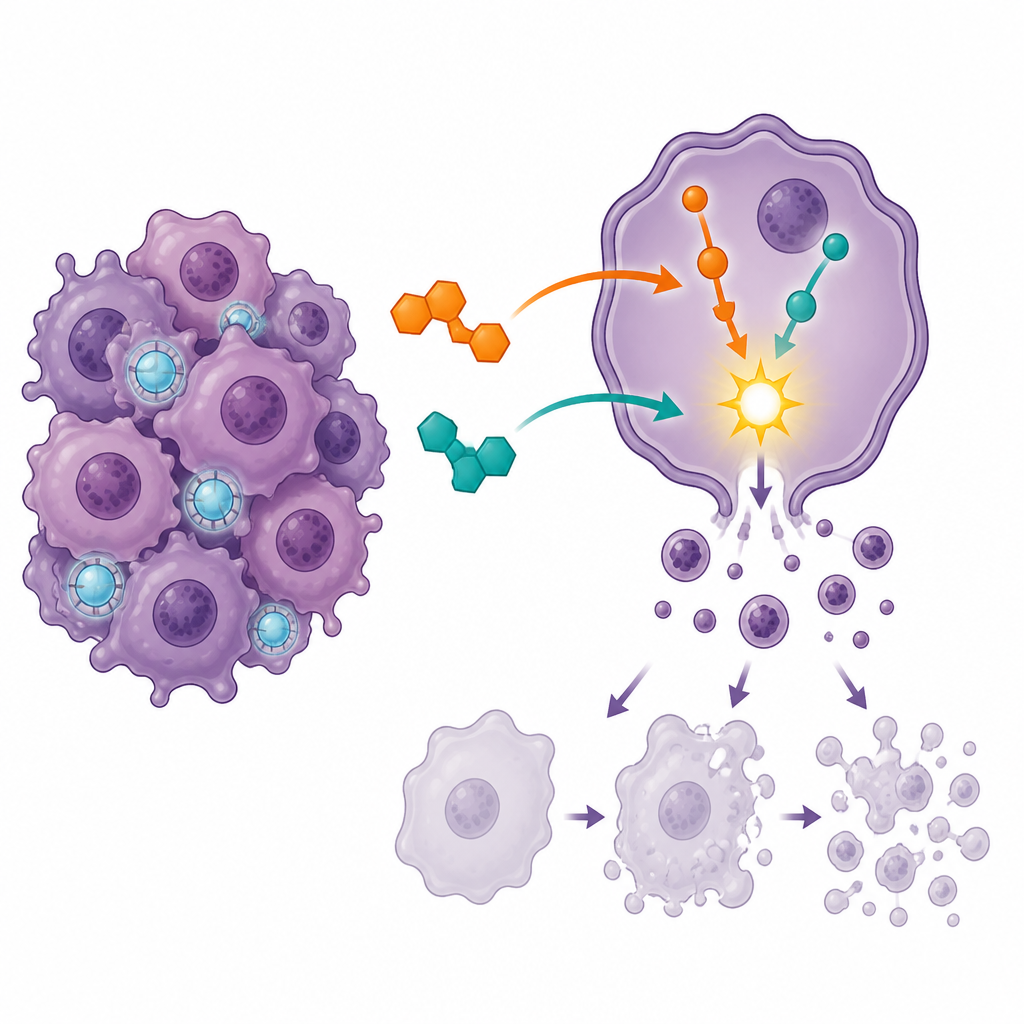
細胞自殺の誘導と細胞分裂の停止
薬剤ががん細胞にどのような影響を与えているかを調べるため、研究チームはフローサイトメトリーを用いて生存細胞とプログラムされた細胞死(アポトーシス)の各段階にある細胞を区別しました。各薬剤は単独でも死に向かう細胞を増やしましたが、併用では後期アポトーシスの増加がより顕著で、完全に生存している細胞の割合が減りました。同時に、多くの細胞がG2/Mとして知られる細胞周期の重要なチェックポイントで停止させられ、分裂準備段階での渋滞が生じました。この分裂段階での強い停滞は、併用治療が細胞を脆弱な瞬間に閉じ込め、その後増殖を続けるよりも制御された自己破壊を起こしやすくしていることを示唆します。
細胞内の死のプログラムをオンにする
次に研究者たちは、生存と死の内部スイッチとして働くいくつかの遺伝子の活性レベルを調べました。併用で、BAXや細胞成分を切断する二つのカスパーゼなどアポトーシス促進遺伝子の発現が上昇し、細胞死に抵抗する働きのあるBCL2は抑えられました。BAXとBCL2のバランスは細胞自殺側に大きく傾きました。さらに、オートファジーと呼ばれるリサイクル過程を管理するATG7も選択的に増加し、処理された分解と細胞内のクリーンアップがアポトーシスと協調して働く可能性が示唆されます。コンピュータによるネットワークおよび経路解析は、影響を受けた主な生物学的テーマがアポトーシス経路、p53に関連するストレスシグナル、および白金系化学療法薬に対する抵抗に結びつく経路であることを確認しました。
将来の治療への示唆
簡潔に言えば、本研究はデシタビンとメトホルミンの併用が、いずれか単独よりも胃がん細胞を分裂停止へと導き、内在する自己破壊機構を活性化しやすくすることを示しています。遺伝子制御の欠陥と異常なエネルギー利用を同時に標的にすることで、がんが生き延びるためや治療抵抗に寄与する複数の“オフ”スイッチを同時に押しているように見えます。これまでの成果は培養下の一種のがん細胞に基づくものであるものの、エピジェネティック薬と代謝薬の併用が侵攻性の高い胃がんの治療抵抗を克服する助けとなる可能性を示唆しており、追加の細胞モデルや最終的には動物実験でこの戦略を検証する強い根拠を提供します。
引用: AlAli, M., Latifi-Navid, S. & Khakzad, M.R. Synergistic induction of apoptosis by the epigenetic modulator decitabine and metformin in gastric cancer cells highlights the potential for combination therapy. Sci Rep 16, 14951 (2026). https://doi.org/10.1038/s41598-026-42417-y
キーワード: 胃がん, デシタビン, メトホルミン, アポトーシス, 併用療法