Clear Sky Science · tr
Epigenetik düzenleyici decitabine ve metformin’in mide kanseri hücrelerinde apoptozu sinerjik olarak indüklemesi, kombinasyon tedavisi olasılığını vurguluyor
Bu çalışma neden önemli
Mide kanseri, kısmen tümörlerin standart kemoterapiye sıkça direnç göstermesi nedeniyle dünya çapında en ölümcül kanserlerden biridir. Bu çalışma, kan hastalıkları için onaylı bir ilaç ile diyabet için kullanılan başka bir onaylı ilacı bir araya getirmenin, mide kanseri hücrelerini kendi kendini yok etme yönüne itip itmeyeceğini araştırıyor; bu da gelecekte daha güvenli ve daha etkili tedavi kombinasyonlarına işaret edebilir.
İki tanıdık ilaç, yeni bir ortaklık
Araştırmacılar, birincil görevleri birbirinden çok farklı olan iki ilaca odaklandı. Decitabine, DNA üzerindeki hücresel koruyucu genleri susturan kimyasal işaretleri gevşeterek belirli kemik iliği kanserlerini tedavi etmek için kullanılır. Metformin ise hücrelerin enerji yönetimini değiştiren ve hücresel bir “yakıt göstergesini” aktive eden yaygın bir diyabet ilacıdır. Her ikisi de tek başına antikanser etkiler göstermiş olsa da, mide kanseri gibi katı tümörlerde etkileri sınırlı olmuştur. Araştırma ekibi, insan mide kanseri hücrelerinde bu iki ilacı birlikte kullanmanın, tümörün hem gen kontrolü hem de metabolizmadaki zayıf noktalarından aynı anda yararlanıp yararlanamayacağını sordu.
Kanser hücresi canlılığı üzerindeki etkiyi test etme
MKN45 adlı insan mide kanseri hücre hattını kullanarak, bilim insanları önce hücreleri her bir ilacın çeşitli dozlarına birkaç gün boyunca maruz bıraktılar, ardından iki ilacın sabit doz kombinasyonlarına uyguladılar. Kalan canlı hücre sayısını ölçmek için standart renk bazlı laboratuvar testi kullandılar. İlaç etkileşimlerini değerlendiren bir matematiksel yöntem, kombinasyonun hücre büyümesini yavaşlatmak için gereken dozu azalttığını ve iki ilacın düşük ila orta öldürücü seviyelerde sinerjistik davrandığını gösterdi. Başka bir deyişle, birlikte kullanıldıklarında, bireysel etkilerinin basit toplamından beklenenden daha etkiliydiler ve özellikle metformin dozlarının düşürülmesine olanak tanıdılar.
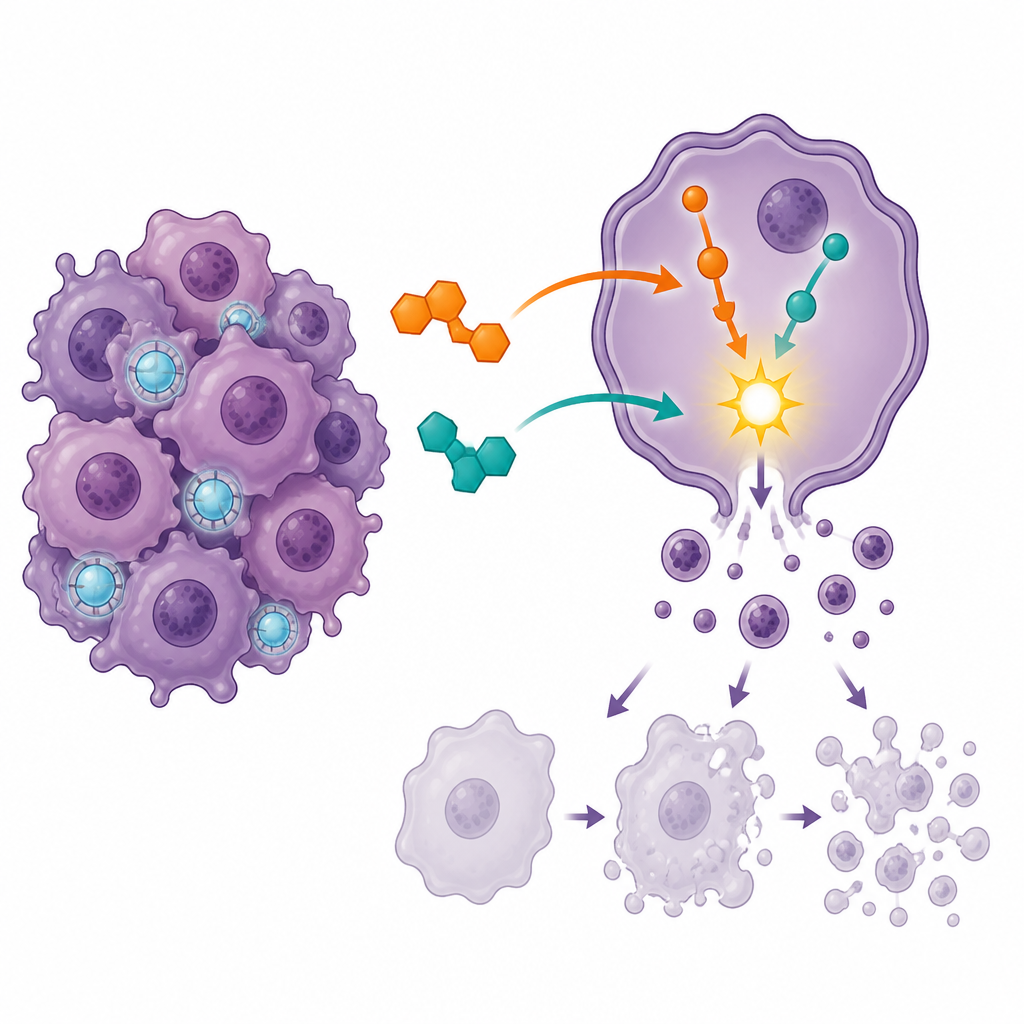
Hücre intiharı tetikleme ve hücre bölünmesini durdurma
İlaçların kanser hücrelerini nasıl etkilediğini görmek için ekip, canlı hücreleri programlı hücre ölümü olan apoptozun farklı aşamalarındaki hücrelerden ayırt edebilen akım sitometrisi tekniğini kullandı. Her bir ilaç tek başına daha fazla hücreyi ölüme doğru itti, ancak kombinasyon geç evre apoptozda çok daha büyük bir artışa neden oldu ve tamamen canlı hücrelerin oranını azalttı. Aynı zamanda hücrelerin çoğu, hücre döngüsünün hücrelerin normalde bölünmeye hazırlandığı G2/M adlı kritik bir kontrol noktasında durmak zorunda kaldı. Bölünme aşamasında oluşan bu güçlü tıkanıklık, birleşik tedavinin hücreleri savunmasız bir anda yakalayıp, çoğalmaya devam etmeleri yerine kontrollü kendi kendini yok etme sürecine girmelerini kolaylaştırdığını düşündürüyor.
Hücre içindeki ölüm programlarını açma
Bilim insanları daha sonra hayatta kalma ve ölüm için iç anahtar görevi gören birkaç genin aktivite düzeylerine baktı. İlaç kombinasyonuyla, BAX ve hücresel bileşenleri parçalayan iki kaspaz gibi apoptozu teşvik eden genlerin düzeyleri yükselirken, hücrelerin normalde ölümü direnmesine yardımcı olan BCL2 geni aşağıya çekildi. BAX ile BCL2 arasındaki denge keskin bir şekilde hücre intiharını destekleyecek yönde kaydı. Hücre içindeki geri dönüşüm sürecine (otofaji) yardımcı olan ATG7 adlı başka bir gen de seçici olarak artmıştı; bu, kontrollü iç parçalanma ve temizliğin tedavi altında apoptozla iş birliği yapabileceğine işaret ediyor. Bilgisayar tabanlı ağ ve yol analizleri, etkilenen ana biyolojik temaların apoptoz yolları, p53 proteiniyle bağlantılı stres sinyalleri ve standart platin bazlı kemoterapi ilaçlarına karşı dirençle ilişkili yollar olduğunu doğruladı.
Gelecekteki tedaviler için ne anlama gelebilir
Basitçe söylemek gerekirse, bu çalışma decitabine ve metformin birlikte kullanıldığında mide kanseri hücrelerini tek başlarına kullanıldıklarından daha fazla bölünmeyi durdurmaya ve yerleşik kendi kendini yok etme mekanizmalarını aktive etmeye yatkın hale getirdiğini gösteriyor. Hatalı gen kontrolü ve anormal enerji kullanımını birlikte hedefleyerek, çift tümörün hayatta kalmak ve tedaviye direnç göstermek için dayandığı birden fazla “kapama” anahtarına aynı anda baskı uyguluyor gibi görünüyor. Bulgular şu ana kadar laboratuvarda büyütülen tek bir hücre tipinden elde edilse de, epigenetik ve metabolik ilaçların kombinasyonunun agresif mide kanserlerinde tedavi direncini aşmaya yardımcı olabileceğini öne sürüyor ve bu stratejinin ek hücre modellerinde ve nihayetinde hayvan çalışmalarında test edilmesi için güçlü bir gerekçe sunuyor.
Atıf: AlAli, M., Latifi-Navid, S. & Khakzad, M.R. Synergistic induction of apoptosis by the epigenetic modulator decitabine and metformin in gastric cancer cells highlights the potential for combination therapy. Sci Rep 16, 14951 (2026). https://doi.org/10.1038/s41598-026-42417-y
Anahtar kelimeler: mide kanseri, decitabine, metformin, apoptoz, kombinasyon tedavisi