Clear Sky Science · ar
التحفيز التآزري للموت المبرمج بواسطة المعدل اللاجيني ديسيتابين والميتفورمين في خلايا سرطان المعدة يبرز إمكانات العلاج المركب
لماذا تهم هذه الدراسة
سرطان المعدة من أخطر السرطانات عالمياً، ويرجع ذلك جزئياً إلى أن الأورام غالباً ما تقاوم العلاج الكيميائي القياسي. تستقصي هذه الدراسة ما إذا كان الجمع بين دوائين معتمدين بالفعل — أحدهما لأمراض الدم والآخر لمرض السكري — يمكن أن يعملان معاً لدفع خلايا سرطان المعدة نحو التدمير الذاتي، مما قد يشير إلى تراكيب علاجية أكثر أماناً وفعالية في المستقبل.
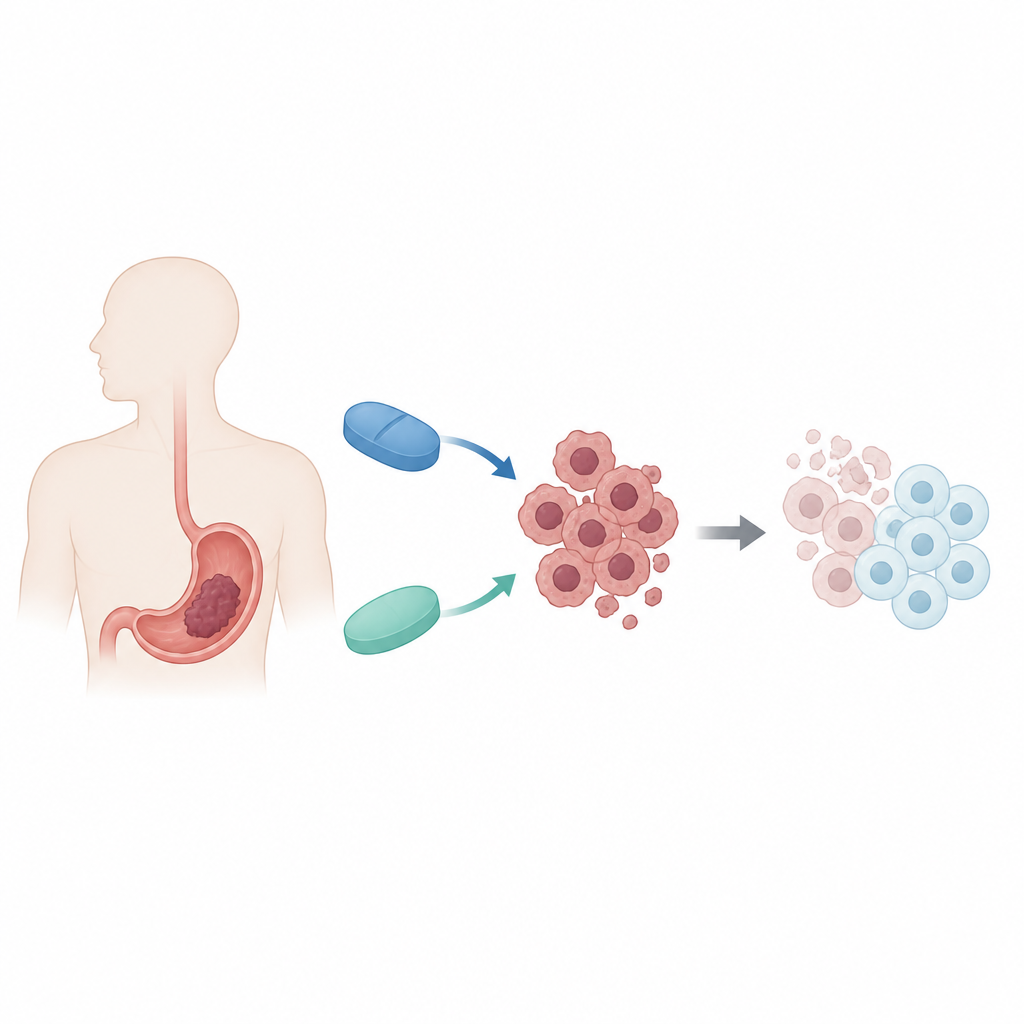
دواءان مألوفان، شراكة جديدة
ركّز الباحثون على دوائين لهما وظائف أساسية مختلفة تماماً. يُستخدم ديسيتابين لعلاج بعض سرطانات نخاع العظام عن طريق تخفيف العلامات الكيميائية على الحمض النووي التي تكبت الجينات الوقائية. الميتفورمين دواء شائع للسكري يغير كيفية معالجة الخلايا للطاقة وينشط "مؤشر الوقود" الخلوي. كلاهما أظهر نشاطاً مضاداً للسرطان بمفرده، لكن تأثيراتهما على الأورام الصلبة مثل سرطان المعدة كانت متواضعة. تساءل الفريق عما إذا كان استخدامهما معاً في خلايا سرطان المعدة البشرية قد يستغل نقاط الضعف في التحكم الجيني والتمثيل الغذائي في الوقت نفسه.
اختبار التأثير على بقاء الخلايا السرطانية
باستخدام خط خلايا سرطان المعدة البشري المسمى MKN45، تعرّض العلماء أولاً لمجموعة من جرعات كل دواء بمفرده على مدار عدة أيام، ثم لأزواج بجرعات ثابتة من الدوائين معاً. قاسوا عدد الخلايا الحية المتبقية باستخدام اختبار مخبري لوني قياسي. أظهرت طريقة رياضية تقيم تداخل الأدوية أن الجمع قلل الجرعة اللازمة لإبطاء نمو الخلايا وأن الدوائين تصرفا بتآزر عند مستويات قتالية منخفضة إلى متوسطة. بعبارة أخرى، معاً كانا أكثر فعالية مما يُتوقع من جمع تأثيراتهما الفردية، مع السماح بجرعات أقل، خصوصاً للميتفورمين.
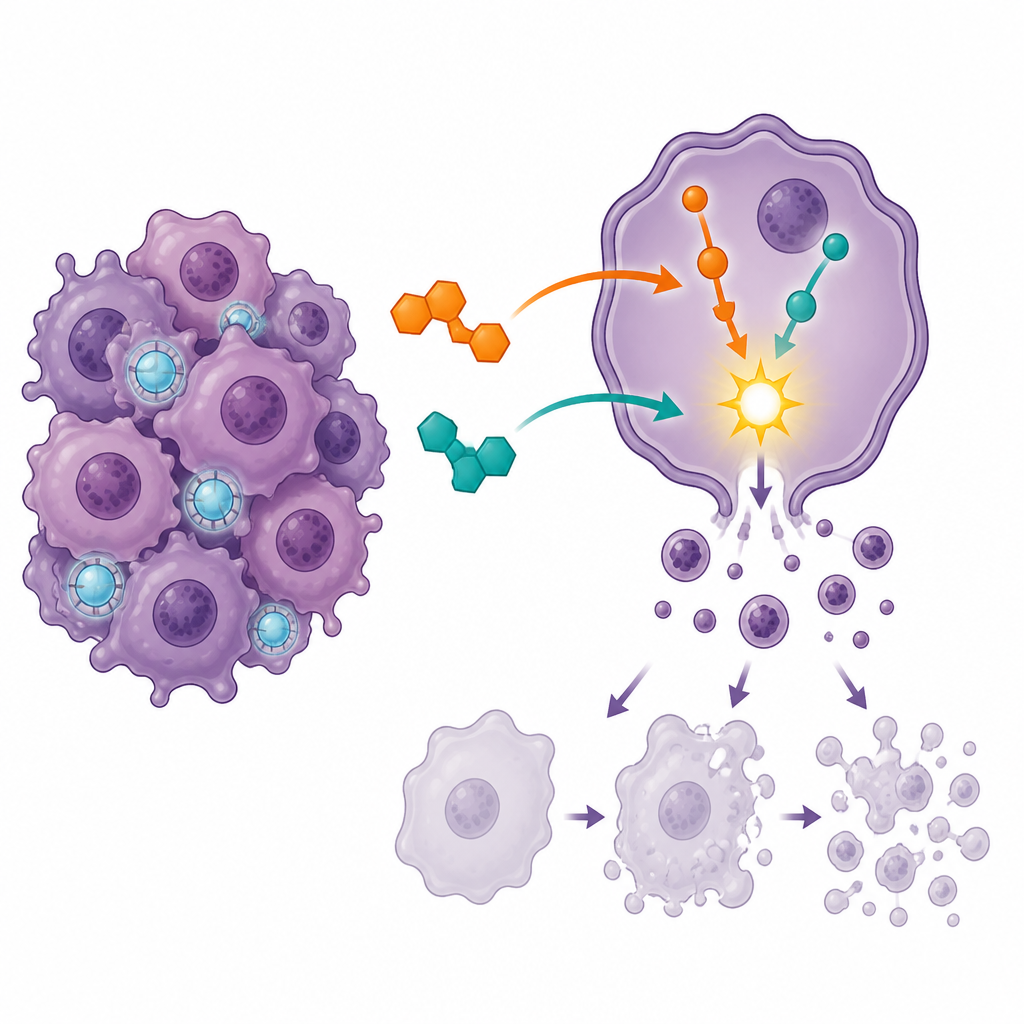
تحفيز الانتحار الخلوي وإيقاف انقسام الخلايا
لمعرفة كيف تؤثر الأدوية على الخلايا السرطانية، استخدم الفريق مقياس التدفق الخلوي، وهي تقنية تميز الخلايا الحية عن تلك في مراحل مختلفة من الموت المبرمج أو الاستماتة. كل دواء بمفرده دفع عدداً أكبر من الخلايا نحو الموت، لكن المزيج تسبب في قفزة أكبر بكثير في الاستماتة المتأخرة وخفض نسبة الخلايا القابلة للحياة تماماً. في الوقت نفسه، أُجبرت معظم الخلايا على التوقف عند نقطة تفتيش رئيسية في دورة الخلية تُعرف بمرحلة G2/M، حيث تستعد الخلايا عادة للانقسام. هذا الاختناق القوي عند مرحلة الانقسام يشير إلى أن العلاج المشترك يحبس الخلايا في لحظة هشة، وبعدها تكون أكثر ميلاً للدخول في عملية التدمير الذاتي المنظمة بدلاً من الاستمرار في التكاثر.
تشغيل برامج الموت داخل الخلية
ثم فحص العلماء مستويات نشاط عدة جينات تعمل كمفاتيح داخلية للنجاة والموت. مع التوليفة الدوائية، ارتفعت مستويات الجينات التي تعزز الموت المبرمج، مثل BAX ونوعين من الكاسبيز اللذين يقسمان مكونات الخلية، بينما انخفضت مستويات BCL2، الجين الذي يساعد الخلايا عادة على مقاومة الموت. تحولت المعادلة بين BAX وBCL2 بشكل حاد لصالح الانتحار الخلوي. كما زاد تعبير جين آخر، ATG7، الذي يساعد في عملية إعادة التدوير المسماة الالتهاب الذاتي (autophagy)، ما يوحي بأن التحلل المنظم والتنظيف داخل الخلية قد يتعاونا مع الاستماتة أثناء العلاج. أكدت تحليلات شبكات ومسارات حاسوبية أن المواضيع البيولوجية الرئيسة المتأثرة كانت مسارات الاستماتة، إشارات الإجهاد المرتبطة ببروتين p53، والطرق المرتبطة بالمقاومة ضد أدوية العلاج الكيميائي القائمة على البلاتين.
ماذا قد يعني هذا للعلاجات المستقبلية
بعبارة بسيطة، تُظهر هذه الدراسة أن ديسيتابين والميتفورمين، عند استخدامهما معاً، يجعلان خلايا سرطان المعدة أكثر عرضة للتوقف عن الانقسام وتنشيط آليات التدمير الذاتي المدمجة مقارنةً بكل دواء بمفرده. من خلال استهداف التحكم الجيني المختل واستخدام الطاقة الشاذ بشكل مشترك، يبدو أن الزوج يضغط على عدة "مفاتيح إيقاف" تعتمد عليها السرطان للبقاء والمقاومة. رغم أن النتائج حتى الآن مستمدة من نوع واحد من خلايا السرطان المزروعة في المختبر، فإنها تشير إلى أن الجمع بين أدوية مؤثرة على العلامات اللاجينية والأيض قد يساعد في التغلب على مقاومة العلاج في سرطانات المعدة العدوانية، وتوفر مبرراً قوياً لاختبار هذه الاستراتيجية في نماذج خلوية إضافية ولاحقاً في دراسات حيوانية.
الاستشهاد: AlAli, M., Latifi-Navid, S. & Khakzad, M.R. Synergistic induction of apoptosis by the epigenetic modulator decitabine and metformin in gastric cancer cells highlights the potential for combination therapy. Sci Rep 16, 14951 (2026). https://doi.org/10.1038/s41598-026-42417-y
الكلمات المفتاحية: سرطان المعدة, ديسيتابين, ميتفورمين, الموت المبرمج, العلاج المركب