Clear Sky Science · it
Induzione sinergica dell'apoptosi dal modulatore epigenetico decitabina e dalla metformina nelle cellule del cancro gastrico evidenzia il potenziale della terapia combinata
Perché questo studio è importante
Il cancro dello stomaco è tra i tumori più letali a livello globale, in parte perché i tumori spesso resistono alla chemioterapia standard. Questo studio esplora se l’accoppiamento di due farmaci già approvati — uno per disturbi ematologici e uno per il diabete — possa agire in sinergia per spingere le cellule tumorali gastriche verso l’autodistruzione, indicando potenzialmente combinazioni terapeutiche più sicure ed efficaci in futuro.
Due farmaci familiari, una nuova collaborazione
I ricercatori si sono concentrati su due medicinali con ruoli primari molto diversi. La decitabina è usata per trattare alcuni tumori del midollo osseo sciogliendo i segni chimici sul DNA che silenziano geni protettivi. La metformina è un farmaco comune per il diabete che modifica il modo in cui le cellule gestiscono l’energia e attiva un “contagiri” cellulare del carburante. Entrambi hanno dimostrato attività anticancro da soli, ma effetti modesti sui tumori solidi come il cancro gastrico. Il gruppo ha chiesto se usarli insieme in cellule umane di cancro gastrico potesse sfruttare i punti deboli del tumore sia nel controllo genico sia nel metabolismo contemporaneamente.
Valutare l’impatto sulla sopravvivenza delle cellule tumorali
Utilizzando una linea cellulare umana di cancro gastrico chiamata MKN45, gli scienziati hanno prima esposto le cellule a una gamma di dosi di ciascun farmaco da soli per diversi giorni, quindi a coppie a dose fissa dei due farmaci insieme. Hanno misurato quante cellule restavano vive usando un test di laboratorio colorimetrico standard. Un metodo matematico che valuta come interagiscono i farmaci ha mostrato che la combinazione ha ridotto la dose necessaria per rallentare la crescita cellulare e che i due farmaci si comportavano in modo sinergico a livelli di uccisione da bassi a moderati. In altre parole, insieme erano più efficaci di quanto ci si sarebbe aspettati dalla semplice somma dei loro effetti individuali, permettendo dosi più basse, in particolare di metformina.
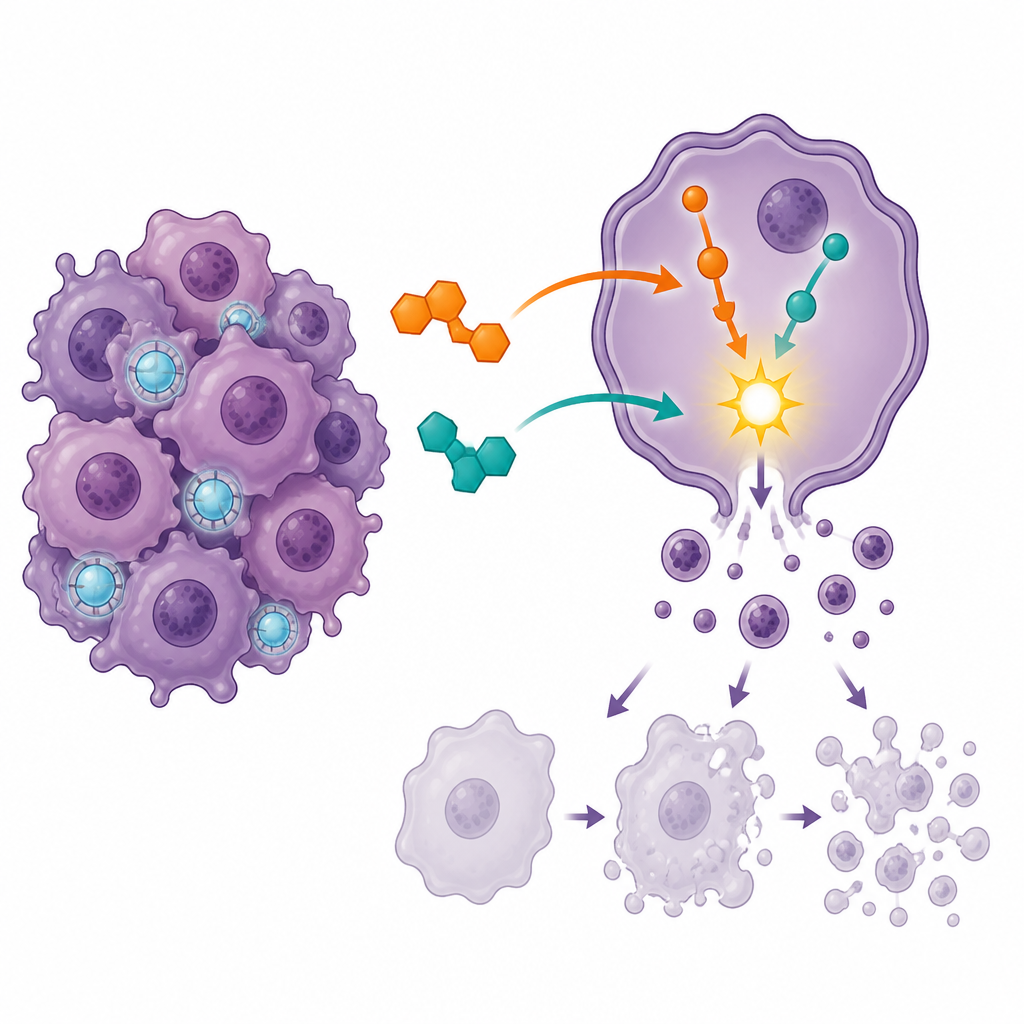
Scatenare il suicidio cellulare e fermare la divisione
Per capire come i farmaci influivano sulle cellule tumorali, il team ha usato la citometria a flusso, una tecnica che distingue le cellule vive da quelle nelle diverse fasi della morte programmata, o apoptosi. Ciascun farmaco da solo ha spinto più cellule verso la morte, ma la combinazione ha causato un aumento molto più marcato dell’apoptosi in fase avanzata e ha ridotto la frazione di cellule completamente vitali. Allo stesso tempo, la maggior parte delle cellule è stata costretta a fermarsi a un punto di controllo chiave del ciclo cellulare noto come G2/M, dove normalmente le cellule si preparano a dividere. Questo forte ingorgo nella fase di divisione suggerisce che il trattamento combinato intrappola le cellule in un momento vulnerabile, dopo il quale è più probabile che subiscano l’autodistruzione controllata piuttosto che continuare a moltiplicarsi.
Attivare i programmi di morte all’interno della cellula
Gli scienziati hanno quindi analizzato i livelli di attività di diversi geni che agiscono come interruttori interni per sopravvivenza e morte. Con la combinazione farmacologica, i geni che promuovono l’apoptosi, come BAX e due caspasi che degradano componenti cellulari, erano aumentati, mentre BCL2, un gene che normalmente aiuta le cellule a resistere alla morte, era ridotto. L’equilibrio tra BAX e BCL2 si è spostato nettamente a favore del suicidio cellulare. Un altro gene, ATG7, che partecipa a un processo di riciclo chiamato autofagia, è stato anch’esso incrementato in modo selettivo, suggerendo che la degradazione e la pulizia controllata all’interno della cellula possono cooperare con l’apoptosi durante il trattamento. Analisi di rete e di via basate su computer hanno confermato che i principali temi biologici interessati erano le vie dell’apoptosi, i segnali di stress legati alla proteina p53 e le rotte associate alla resistenza ai chemioterapici a base di platino.
Cosa potrebbe significare per i trattamenti futuri
In termini semplici, questo lavoro mostra che decitabina e metformina, usate insieme, rendono le cellule del cancro gastrico più propense a interrompere la divisione e ad attivare i meccanismi interni di autodistruzione rispetto all’uso di ciascun farmaco singolarmente. Mirando congiuntamente al controllo genico difettoso e all’uso anomalo dell’energia, la coppia sembra premere su più “interruttori di spegnimento” di cui il tumore si serve per sopravvivere e resistere al trattamento. Sebbene i risultati finora provengano da un solo tipo di cellula tumorale coltivata in laboratorio, suggeriscono che la combinazione di farmaci epigenetici e metabolici potrebbe aiutare a superare la resistenza ai trattamenti nei gastrici aggressivi e forniscono una solida base per testare questa strategia in ulteriori modelli cellulari e, successivamente, in studi animali.
Citazione: AlAli, M., Latifi-Navid, S. & Khakzad, M.R. Synergistic induction of apoptosis by the epigenetic modulator decitabine and metformin in gastric cancer cells highlights the potential for combination therapy. Sci Rep 16, 14951 (2026). https://doi.org/10.1038/s41598-026-42417-y
Parole chiave: cancro gastrico, decitabina, metformina, apoptosi, terapia combinata