Clear Sky Science · fr
Induction synergique de l’apoptose par le modulateur épigénétique décitabine et la metformine dans des cellules de cancer gastrique souligne le potentiel d’une thérapie combinée
Pourquoi cette étude compte
Le cancer de l’estomac figure parmi les cancers les plus meurtriers dans le monde, en partie parce que les tumeurs résistent souvent à la chimiothérapie standard. Cette étude examine si l’association de deux médicaments déjà approuvés — l’un pour des troubles sanguins et l’autre pour le diabète — peut agir de concert pour pousser les cellules du cancer gastrique vers l’autodestruction, ouvrant potentiellement la voie à des combinaisons de traitement plus sûres et plus efficaces à l’avenir.
Deux médicaments familiers, un nouveau partenariat
Les chercheurs se sont focalisés sur deux médicaments dont les indications principales sont très différentes. La décitabine est utilisée pour traiter certains cancers de la moelle osseuse en assouplissant les marques chimiques sur l’ADN qui inhibent des gènes protecteurs. La metformine est un médicament courant contre le diabète qui modifie la gestion de l’énergie par les cellules et active un « indicateur de carburant » cellulaire. Chacun a montré une activité anticancéreuse isolément, mais des effets modestes sur les tumeurs solides comme le cancer gastrique. L’équipe a testé si leur utilisation conjointe dans des cellules humaines de cancer gastrique pourrait exploiter simultanément les points faibles de la tumeur en matière de contrôle des gènes et de métabolisme.
Évaluer l’impact sur la survie des cellules cancéreuses
En utilisant une lignée cellulaire humaine de cancer de l’estomac appelée MKN45, les scientifiques ont d’abord exposé les cellules à une gamme de doses de chaque médicament seul pendant plusieurs jours, puis à des paires de doses fixes des deux médicaments ensemble. Ils ont mesuré le nombre de cellules encore vivantes à l’aide d’un test de laboratoire colorimétrique standard. Une méthode mathématique évaluant les interactions médicamenteuses a montré que la combinaison réduisait la dose nécessaire pour ralentir la croissance cellulaire et que les deux médicaments se comportaient de façon synergique à des niveaux de mortalité faibles à modérés. Autrement dit, ensemble ils étaient plus efficaces que la somme de leurs effets individuels, tout en permettant d’utiliser des doses plus faibles, en particulier de metformine.
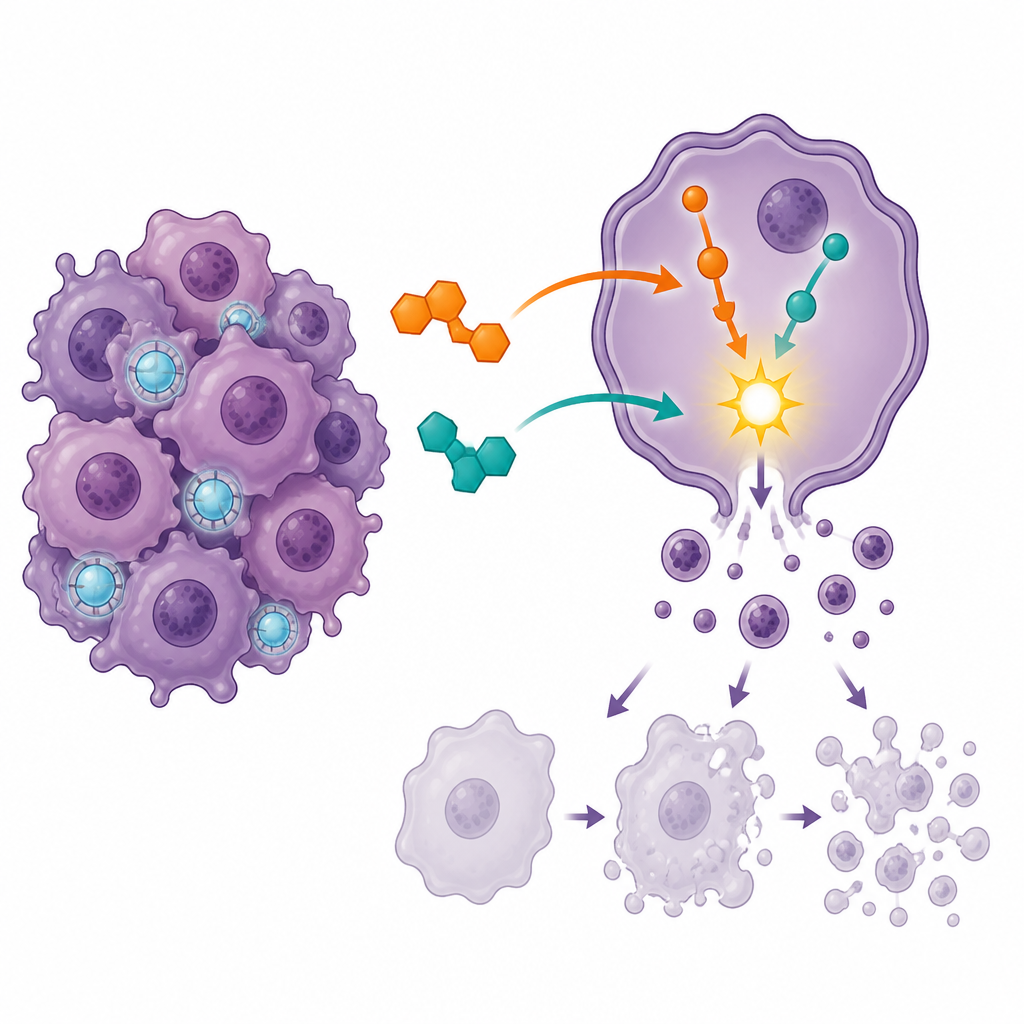
Déclencher le suicide cellulaire et arrêter la division
Pour comprendre comment les médicaments affectaient les cellules cancéreuses, l’équipe a utilisé la cytométrie en flux, une technique capable de distinguer les cellules vivantes de celles en différents stades de mort programmée, ou apoptose. Chaque médicament seul a poussé un nombre plus élevé de cellules vers la mort, mais la combinaison a provoqué une augmentation bien plus marquée de l’apoptose en phase avancée et a réduit la fraction de cellules pleinement viables. Parallèlement, la majorité des cellules ont été contraintes de s’arrêter à un point de contrôle clé du cycle cellulaire connu sous le nom de G2/M, où les cellules se préparent normalement à se diviser. Cet important embouteillage au stade de la division suggère que le traitement combiné piège les cellules à un moment vulnérable, après quoi elles sont plus susceptibles de subir une autodestruction contrôlée plutôt que de continuer à se multiplier.
Activation des programmes de mort à l’intérieur de la cellule
Les scientifiques ont ensuite examiné les niveaux d’expression de plusieurs gènes qui servent de commutateurs internes pour la survie et la mort. Avec la combinaison médicamenteuse, les gènes qui favorisent l’apoptose, tels que BAX et deux caspases qui dégradent les composants cellulaires, ont été up‑régulés, tandis que BCL2, un gène qui aide normalement les cellules à résister à la mort, a été down‑régulé. L’équilibre entre BAX et BCL2 s’est déplacé nettement en faveur du suicide cellulaire. Un autre gène, ATG7, qui participe à la gestion d’un processus de recyclage appelé autophagie, a également été augmenté de façon sélective, suggérant que la dégradation et le nettoyage contrôlés à l’intérieur de la cellule peuvent coopérer avec l’apoptose lors du traitement. Des analyses informatiques de réseaux et de voies ont confirmé que les principaux thèmes biologiques affectés étaient les voies d’apoptose, les signaux de stress liés à la protéine p53 et les voies associées à la résistance aux médicaments de chimiothérapie à base de platine.
Ce que cela pourrait signifier pour les traitements futurs
En termes simples, ce travail montre que la décitabine et la metformine, utilisées ensemble, rendent les cellules du cancer gastrique plus susceptibles d’arrêter de se diviser et d’activer leur mécanisme d’autodestruction qu’avec l’un ou l’autre médicament seul. En ciblant conjointement le contrôle génétique défaillant et l’utilisation anormale de l’énergie, le duo semble actionner plusieurs « interrupteurs off » dont la tumeur dépend pour survivre et résister au traitement. Bien que les résultats proviennent pour l’instant d’un seul type de cellules cultivées en laboratoire, ils suggèrent que la combinaison de médicaments épigénétiques et métaboliques pourrait aider à surmonter la résistance aux traitements dans les cancers gastriques agressifs, et fournissent une justification solide pour tester cette stratégie dans d’autres modèles cellulaires puis, éventuellement, chez l’animal.
Citation: AlAli, M., Latifi-Navid, S. & Khakzad, M.R. Synergistic induction of apoptosis by the epigenetic modulator decitabine and metformin in gastric cancer cells highlights the potential for combination therapy. Sci Rep 16, 14951 (2026). https://doi.org/10.1038/s41598-026-42417-y
Mots-clés: cancer gastrique, décitabine, metformine, apoptose, thérapie combinée