Clear Sky Science · ru
Синергетическое индуцирование апоптоза эпигенетическим модификатором децитабином и метформином в клетках рака желудка подчёркивает потенциал комбинированной терапии
Почему это исследование важно
Рак желудка — один из самых смертельных видов рака в мире, отчасти потому, что опухоли часто устойчивы к стандартной химиотерапии. В этом исследовании проверяют, смогут ли два уже одобренных препарата — один для заболеваний крови и один для диабета — совместно работать над тем, чтобы подтолкнуть клетки рака желудка к саморазрушению, что потенциально может указать на более безопасные и эффективные варианты лечения в будущем.
Два привычных препарата, новое партнёрство
Исследователи сосредоточились на двух лекарствах с очень разными основными задачами. Децитабин применяется при некоторых злокачественных болезнях костного мозга, он ослабляет химические метки на ДНК, которые делают неактивными защитные гены. Метформин — широко используемое средство при диабете, которое меняет способы получения клеткой энергии и активирует клеточный «датчик топлива». Оба препарата в одиночку демонстрировали противоопухолевую активность, но их эффекты в солидных опухолях, таких как рак желудка, были скромными. Команда поставила вопрос, не позволит ли их совместное применение в клетках человеческого рака желудка одновременно затронуть слабые места опухоли в контроле генов и метаболизме.
Проверка влияния на выживаемость клеток рака
Используя клеточную линию человеческого рака желудка MKN45, учёные сначала обрабатывали клетки диапазоном доз каждого препарата по отдельности на протяжении нескольких дней, а затем фиксированными парами доз обоих препаратов вместе. Они измеряли число живых клеток с помощью стандартного колориметрического лабораторного теста. Математический метод для оценки взаимодействия препаратов показал, что комбинация снижала дозу, необходимую для торможения роста клеток, и что два препарата вели себя синергически при низком и умеренном уровне гибели клеток. Иными словами, вместе они оказывали более сильный эффект, чем простое суммирование индивидуальных действий, при этом позволяя использовать более низкие дозы, особенно метформина.
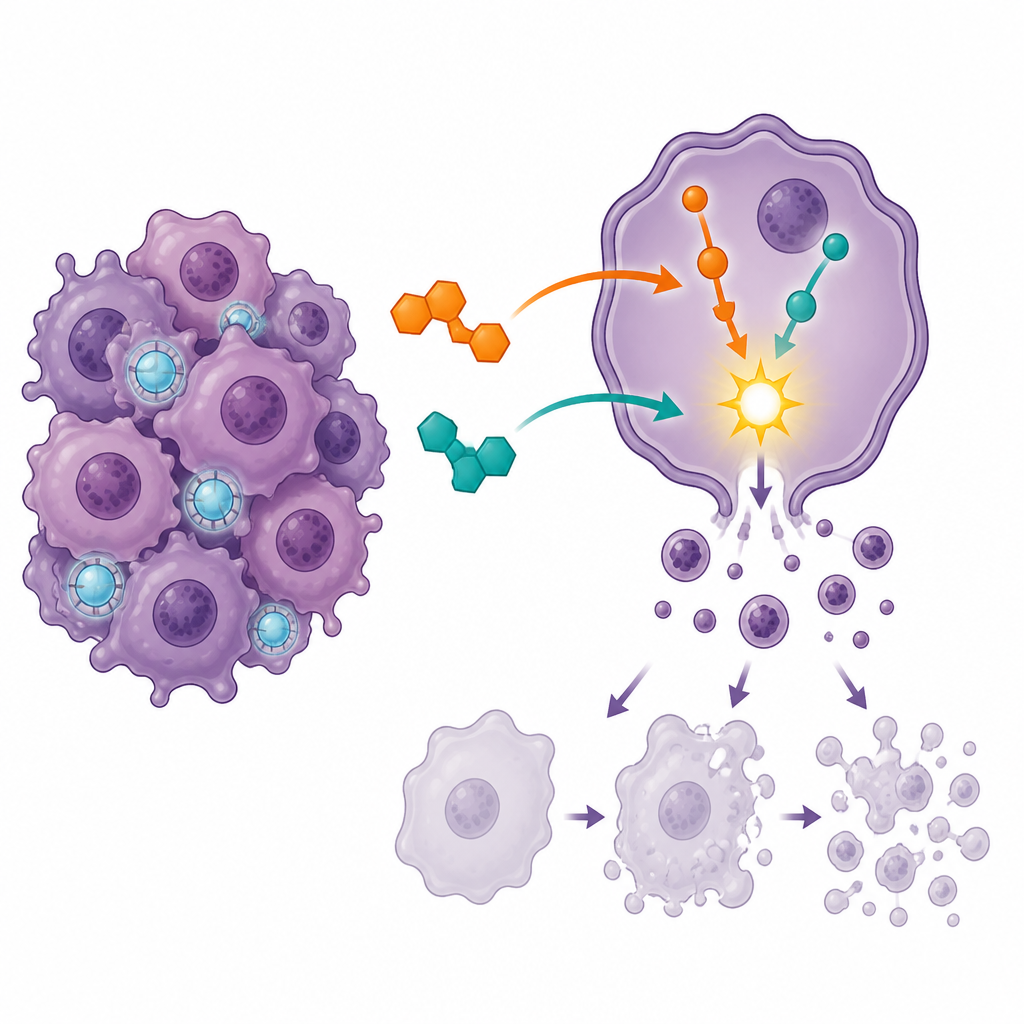
Запуск клеточного самоубийства и остановка деления
Чтобы понять, как препараты влияют на раковые клетки, команда использовала проточная цитометрию — метод, позволяющий различать живые клетки и клетки на разных стадиях программируемой гибели, или апоптоза. Каждый препарат по‑отдельности сдвигал больше клеток в сторону смерти, но комбинация вызывала гораздо более заметный рост доли клеток на поздних стадиях апоптоза и уменьшала долю полностью жизнеспособных клеток. Одновременно большинство клеток оказывались задержаны в ключевой контрольной точке клеточного цикла, известной как G2/M, где клетки обычно готовятся к делению. Эта сильная «пробка» на стадии деления указывает на то, что комбинированное лечение захватывает клетки в уязвимый момент, после чего они с большей вероятностью пойдут по пути контролируемого саморазрушения, а не продолжат размножаться.
Активация программ смерти внутри клетки
Затем учёные изучили уровни активности нескольких генов, выступающих внутренними переключателями выживания и смерти. При комбинированной терапии усиливалась экспрессия генов, способствующих апоптозу, таких как BAX и двух каспаз, расщепляющих компоненты клетки, тогда как BCL2, ген, который обычно помогает клеткам противостоять смерти, подавлялся. Баланс между BAX и BCL2 резко сместился в пользу клеточного самоубийства. Другой ген, ATG7, участвующий в управлении процессом рециклинга — аутофагией, также был выборочно повышен, что указывает на то, что контролируемый распад и уборка внутри клетки могут взаимодействовать с апоптозом при лечении. Компьютерный анализ сетей и путей подтвердил, что основные затронутые биологические темы — это пути апоптоза, стрессовые сигналы, связанные с белком p53, и маршруты, связанные с устойчивостью к стандартным препаратам на основе платины.
Что это может значить для будущих лечений
Проще говоря, результаты показывают, что децитабин и метформин в сочетании делают клетки рака желудка более склонными прекратить деление и включить встроенные механизмы саморазрушения, чем при применении любого из препаратов по отдельности. Совместно воздействуя на нарушенный контроль генов и аномальный обмен энергией, пара, похоже, нажимает несколько «выключателей», на которые опирается рак для выживания и устойчивости к лечению. Хотя полученные данные пока относятся к одному типу клеток, выращенных в лаборатории, они свидетельствуют о том, что комбинирование эпигенетических и метаболических препаратов может помочь преодолеть устойчивость к лечению в агрессивных формах рака желудка и дают веские основания для проверки этой стратегии в дополнительных клеточных моделях и, в конечном итоге, в экспериментах на животных.
Цитирование: AlAli, M., Latifi-Navid, S. & Khakzad, M.R. Synergistic induction of apoptosis by the epigenetic modulator decitabine and metformin in gastric cancer cells highlights the potential for combination therapy. Sci Rep 16, 14951 (2026). https://doi.org/10.1038/s41598-026-42417-y
Ключевые слова: рак желудка, децитабин, метформин, апоптоз, комбинированная терапия