Clear Sky Science · nl
Synergetische inductie van apoptose door de epigenetische modulator decitabine en metformine in maagkankercellen benadrukt de potentie van combinatietherapie
Waarom deze studie ertoe doet
Maagkanker behoort wereldwijd tot de dodelijkste vormen van kanker, deels omdat tumoren vaak resistent zijn tegen standaardchemotherapie. Deze studie onderzoekt of het combineren van twee reeds goedgekeurde middelen — één voor bloedziekten en één voor diabetes — samen maagkankercellen kan aanzetten tot zelfdestructie, wat mogelijk wijst op veiligere en effectievere behandelcombinaties in de toekomst.
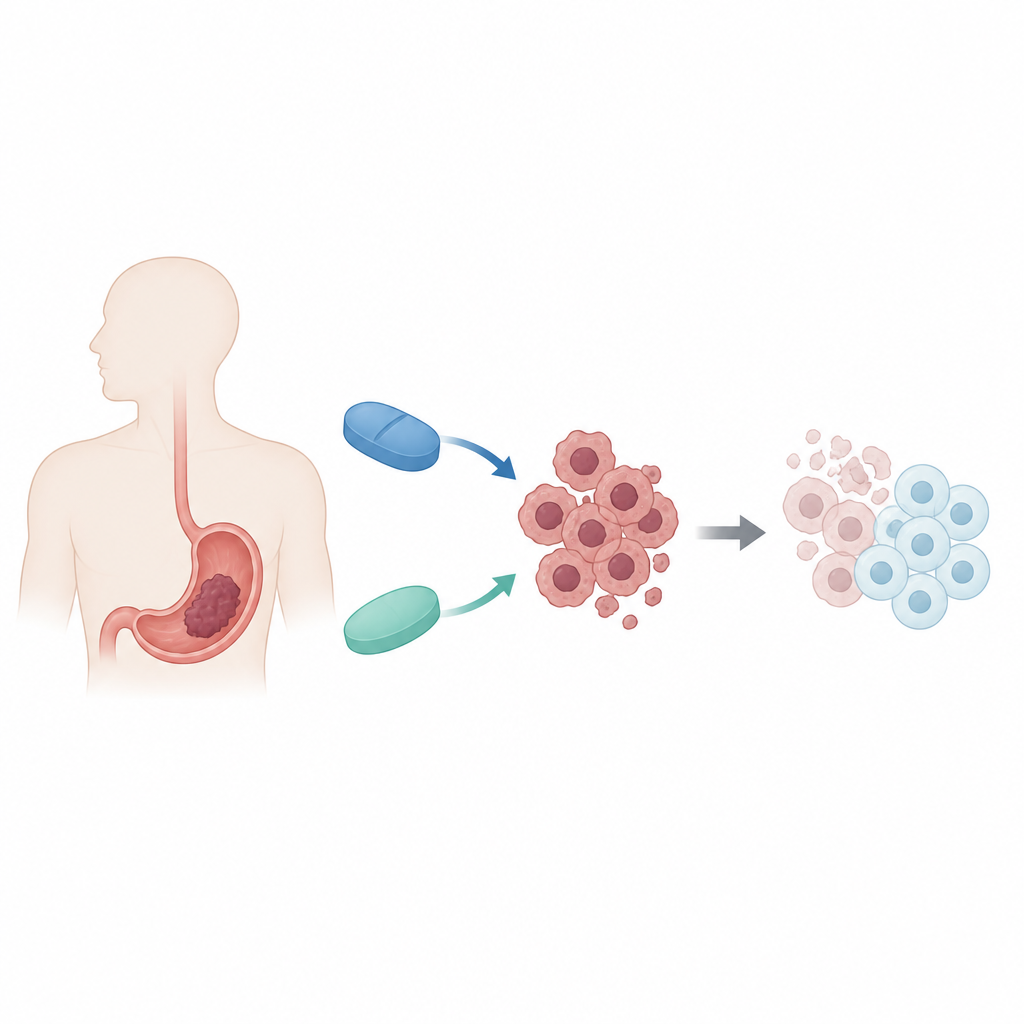
Twee vertrouwde medicijnen, een nieuw partnerschap
De onderzoekers concentreerden zich op twee geneesmiddelen met heel verschillende primaire functies. Decitabine wordt gebruikt voor bepaalde beenmergkankers door chemische labels op DNA losser te maken die beschermende genen stilleggen. Metformine is een veelgebruikt diabetesmiddel dat de manier waarop cellen energie gebruiken verandert en een cellulair “brandstofmeter”-pad activeert. Beide hebben op zichzelf anti-kankeractiviteit laten zien, maar slechts bescheiden effecten in solide tumoren zoals maagkanker. Het team vroeg zich af of ze samen in humane maagkankercellen de zwakke plekken van de tumor in zowel genregulatie als metabolisme tegelijk zouden kunnen benutten.
Het effect op overleving van kankercellen testen
Met een humane maagkankercellijn genaamd MKN45 brachten de wetenschappers de cellen eerst meerdere dagen bloot aan een reeks concentraties van elk geneesmiddel afzonderlijk, en daarna aan vaste dosisparen van de twee middelen samen. Ze maten hoeveel cellen leefden met een standaard kleurgebaseerde laboratoriumtest. Een wiskundige methode voor het evalueren van geneesmiddelinteracties liet zien dat de combinatie de benodigde dosis om celgroei te remmen verlaagde en dat de twee middelen synergetisch werkten bij lage tot matige niveaus van celdood. Met andere woorden: samen waren ze effectiever dan verwacht op basis van een simpele optelsom van hun individuele effecten, terwijl lagere doses mogelijk waren, vooral van metformine.
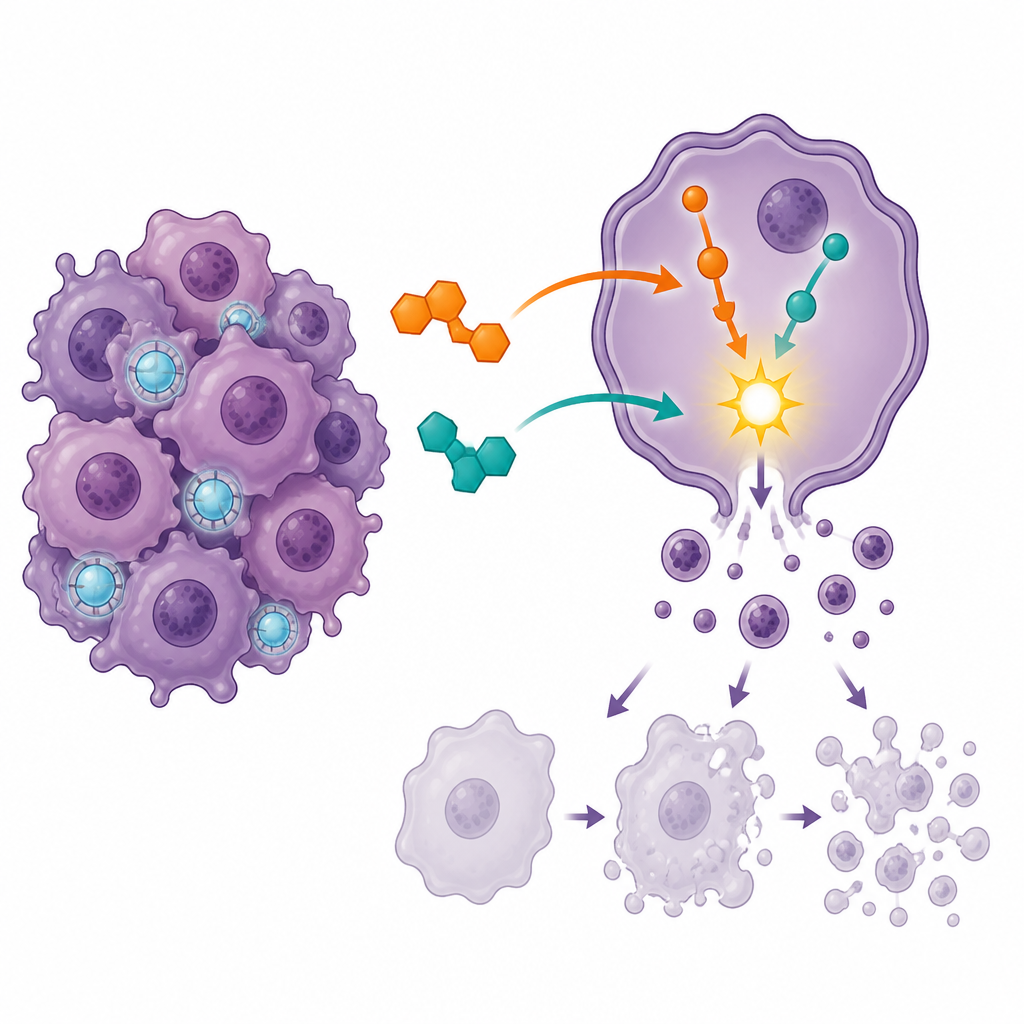
Celzelfmoord activeren en celdeling stoppen
Om te zien hoe de middelen de kankercellen beïnvloedden, gebruikten de onderzoekers flowcytometrie, een techniek die levende cellen kan onderscheiden van cellen in verschillende stadia van geprogrammeerde celdood, of apoptose. Elk middel op zichzelf duwde meer cellen richting celdood, maar de combinatie veroorzaakte een veel sterkere toename van late apoptose en verminderde het aandeel volledig levensvatbare cellen. Tegelijkertijd werden de meeste cellen gedwongen te pauzeren bij een cruciaal controlepunt van de celcyclus dat bekendstaat als G2/M, waar cellen zich normaal voorbereiden om te delen. Deze sterke opstopping bij de delingsfase suggereert dat de gecombineerde behandeling cellen op een kwetsbaar moment vastzet, waarna ze eerder gecontroleerde zelfvernietiging ondergaan dan verder te delen.
Interne doodsprogramma’s inschakelen
De wetenschappers bekeken vervolgens de activiteit van meerdere genen die als interne schakelaars voor overleving en dood fungeren. Bij de combinatiebehandeling werden genen die apoptose bevorderen, zoals BAX en twee caspases die cellulaire componenten afbreken, omhooggebracht, terwijl BCL2, een gen dat cellen normaal helpt weerstand tegen dood te bieden, werd omlaaggebracht. De balans tussen BAX en BCL2 schoof scherp in het voordeel van celdood. Een ander gen, ATG7, dat een rol speelt in een recyclingproces genaamd autofagie, werd ook selectief verhoogd, wat suggereert dat gecontroleerde afbraak en opruiming binnen de cel mogelijk samenwerken met apoptose onder behandeling. Computergebaseerde netwerk- en padanalyses bevestigden dat de belangrijkste biologische thema’s die werden beïnvloed apoptosepaden, stresssignalen gekoppeld aan het p53-eiwit en routes gerelateerd aan resistentie tegen standaard platinumgebaseerde chemotherapieën waren.
Wat dit kan betekenen voor toekomstige behandelingen
Simpel gezegd laat dit werk zien dat decitabine en metformine, wanneer ze samen worden gebruikt, maagkankercellen eerder doen stoppen met delen en hun ingebouwde zelfvernietigingsmechanismen activeren dan wanneer elk medicijn afzonderlijk wordt toegepast. Door gezamenlijk foutieve genregulatie en abnormaal energiegebruik aan te pakken, lijkt het paar meerdere “uit”-schakelaars in te drukken waarop de kanker vertrouwt om te overleven en treatment te weerstaan. Hoewel de bevindingen tot nu toe afkomstig zijn van één type kankercel gekweekt in het laboratorium, suggereren ze dat het combineren van epigenetische en metabole middelen kan helpen behandelresistentie in agressieve maagkankers te overwinnen, en geven ze een sterke rationale om deze strategie in aanvullende cellulaire modellen en uiteindelijk in dierstudies te testen.
Bronvermelding: AlAli, M., Latifi-Navid, S. & Khakzad, M.R. Synergistic induction of apoptosis by the epigenetic modulator decitabine and metformin in gastric cancer cells highlights the potential for combination therapy. Sci Rep 16, 14951 (2026). https://doi.org/10.1038/s41598-026-42417-y
Trefwoorden: maagkanker, decitabine, metformine, apoptose, combinatietherapie