Clear Sky Science · pl
Synergistyczne wywołanie apoptozy przez modyfikator epigenetyczny dekwitabina i metforminę w komórkach raka żołądka — implikacje dla terapii skojarzonej
Dlaczego to badanie ma znaczenie
Rak żołądka należy do jednych z najbardziej śmiertelnych nowotworów na świecie, częściowo dlatego, że guzy często wykazują oporność na standardową chemioterapię. W tym badaniu sprawdzono, czy zestawienie dwóch już zatwierdzonych leków — jednego stosowanego w chorobach krwi i drugiego w cukrzycy — może wspólnie skłonić komórki raka żołądka do samodestrukcji, co potencjalnie wskazuje na bezpieczniejsze i skuteczniejsze kombinacje terapeutyczne w przyszłości.
Dwa znane leki, nowe partnerstwo
Naukowcy skoncentrowali się na dwóch lekach o bardzo różnych podstawowych zadaniach. Dekwitabina stosowana jest w leczeniu wybranych nowotworów szpiku poprzez rozluźnianie chemicznych znaczników na DNA, które wyciszają geny ochronne. Metformina to powszechny lek przeciwcukrzycowy, który zmienia sposób gospodarowania energią w komórce i aktywuje wewnętrzny „wskaźnik paliwa”. Oba wykazały samodzielnie aktywność przeciwnowotworową, lecz efekty w guzach litych, takich jak rak żołądka, były umiarkowane. Zespół postawił pytanie, czy ich jednoczesne stosowanie w ludzkich komórkach raka żołądka może jednocześnie wykorzystać słabe punkty guza w kontroli genów i metabolizmie.
Badanie wpływu na przeżywalność komórek nowotworowych
Z użyciem ludzkiej linii komórkowej raka żołądka MKN45 naukowcy najpierw poddali komórki działaniu różnych dawek każdego leku osobno przez kilka dni, a następnie stałym parom dawek obu leków razem. Mierzono liczbę żywych komórek za pomocą standardowego kolorymetrycznego testu laboratoryjnego. Matematyczna metoda oceniająca interakcje leków wykazała, że kombinacja zmniejszała dawkę potrzebną do spowolnienia wzrostu komórek oraz że dwa leki działały synergistycznie przy niskich do umiarkowanych poziomach zabijania. Innymi słowy, razem były bardziej skuteczne, niż wynikałoby to z prostego dodania ich indywidualnych efektów, pozwalając jednocześnie na niższe dawki, zwłaszcza metforminy.
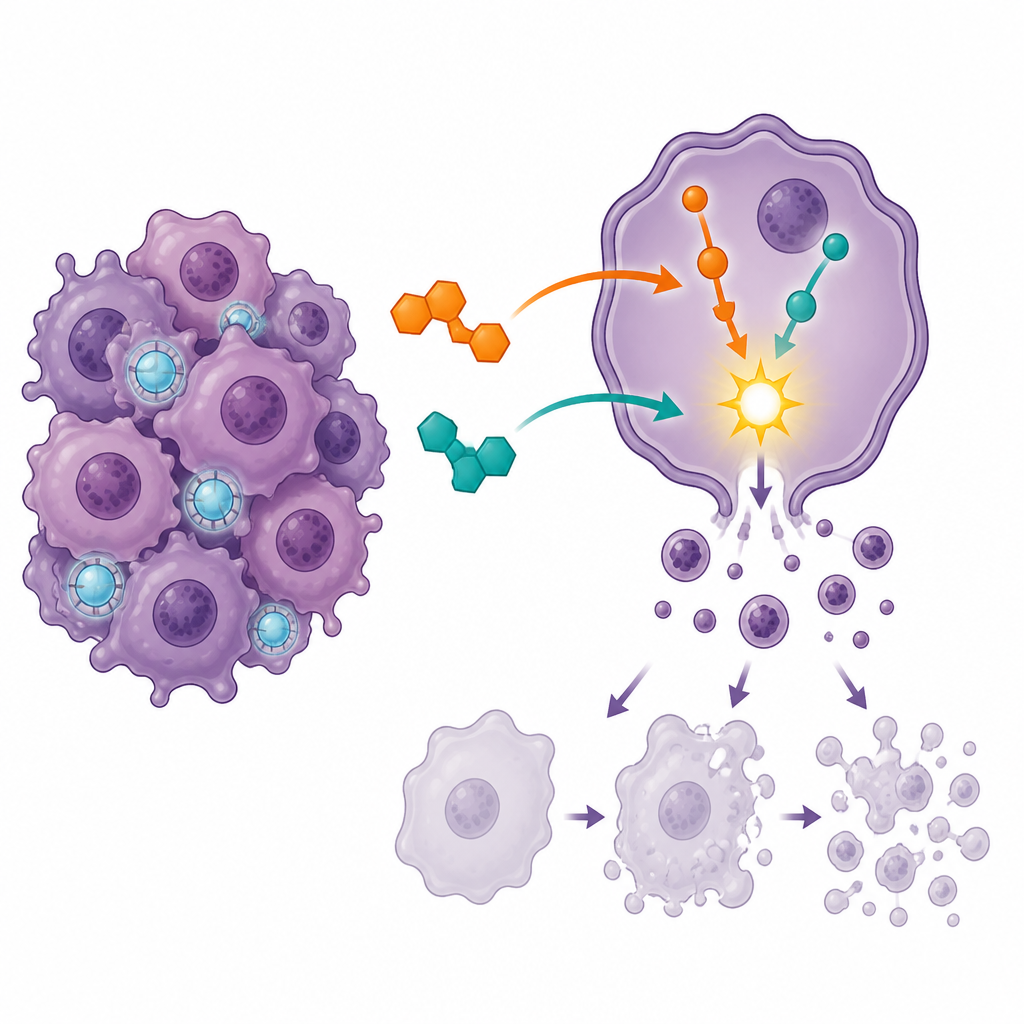
Wywoływanie samobójstwa komórkowego i zatrzymywanie podziałów
Aby sprawdzić, jak leki wpływają na komórki nowotworowe, zespół użył cytometrii przepływowej — techniki pozwalającej odróżnić komórki żywe od tych znajdujących się w różnych stadiach kontrolowanej śmierci komórkowej, czyli apoptozy. Każdy lek z osobna skłaniał więcej komórek ku śmierci, ale kombinacja spowodowała znacznie większy wzrost liczby komórek w zaawansowanej apoptozie i zmniejszyła odsetek w pełni żywotnych komórek. Jednocześnie większość komórek była zatrzymana w kluczowym punkcie kontrolnym cyklu komórkowego znanym jako faza G2/M, gdzie komórki przygotowują się do podziału. Ten mocny „korek” na etapie podziału sugeruje, że leczenie skojarzone blokuje komórki w newralgicznym momencie, po którym są bardziej skłonne do kontrolowanej samodestrukcji zamiast dalszego mnożenia.
Włączanie programów śmierci wewnątrz komórki
Następnie naukowcy przeanalizowali poziomy aktywności kilku genów działających jako wewnętrzne przełączniki przeżycia i śmierci. W wyniku terapii skojarzonej zwiększyła się ekspresja genów promujących apoptozę, takich jak BAX i dwóch kaspaz, które rozkładają składniki komórkowe, podczas gdy BCL2 — gen zwykle pomagający komórkom opierać się śmierci — został stłumiony. Równowaga między BAX a BCL2 przesunęła się zdecydowanie na korzyść „samobójstwa” komórkowego. Inny gen, ATG7, uczestniczący w procesie recyklingu komórkowego zwanego autofagią, również został selektywnie zwiększony, co sugeruje, że kontrolowany rozkład i porządkowanie wewnątrz komórki może współpracować z apoptozą podczas leczenia. Analizy sieciowe i ścieżkowe wspomagane komputerowo potwierdziły, że główne zmienione motywy biologiczne to szlaki apoptozy, sygnały stresowe związane z białkiem p53 oraz szlaki powiązane z opornością na standardowe leki chemioterapeutyczne oparte na platynie.
Co to może oznaczać dla przyszłych terapii
Mówiąc prosto, praca ta pokazuje, że dekwitabina i metformina stosowane razem zwiększają prawdopodobieństwo, że komórki raka żołądka przestaną się dzielić i aktywują swój wewnętrzny mechanizm samodestrukcji w większym stopniu niż przy użyciu któregokolwiek leku osobno. Poprzez jednoczesne celowanie w wadliwą kontrolę genów i nieprawidłowe wykorzystanie energii, para ta wydaje się naciskać na wiele „wyłączników”, od których zależy przetrwanie i oporność nowotworu. Chociaż wyniki pochodzą jak dotąd z jednego typu komórek hodowanych w laboratorium, sugerują, że łączenie leków epigenetycznych i metabolicznych może pomóc pokonać oporność leczniczą w agresywnych rakach żołądka i dostarcza mocnych przesłanek do testowania tej strategii w dodatkowych modelach komórkowych, a w dalszej kolejności w badaniach na zwierzętach.
Cytowanie: AlAli, M., Latifi-Navid, S. & Khakzad, M.R. Synergistic induction of apoptosis by the epigenetic modulator decitabine and metformin in gastric cancer cells highlights the potential for combination therapy. Sci Rep 16, 14951 (2026). https://doi.org/10.1038/s41598-026-42417-y
Słowa kluczowe: rak żołądka, dekwitabina, metformina, apoptoza, terapia skojarzona