Clear Sky Science · es
Inducción sinérgica de la apoptosis por el modulador epigenético decitabina y la metformina en células de cáncer gástrico subraya el potencial de la terapia combinada
Por qué este estudio importa
El cáncer de estómago es uno de los más mortales a nivel mundial, en parte porque los tumores a menudo resisten la quimioterapia estándar. Este estudio explora si emparejar dos fármacos ya aprobados —uno para trastornos sanguíneos y otro para la diabetes— puede actuar de forma conjunta para impulsar a las células del cáncer gástrico hacia la autodestrucción, señalando potencialmente combinaciones de tratamiento más seguras y efectivas en el futuro.
Dos fármacos familiares, una nueva alianza
Los investigadores se centraron en dos medicinas con funciones primarias muy distintas. La decitabina se usa para tratar ciertos cánceres de médula ósea al aflojar las marcas químicas en el ADN que silencian genes protectores. La metformina es un fármaco común contra la diabetes que altera cómo las células manejan la energía y activa un “indicador de combustible” celular. Ambos han mostrado actividad anticancerígena por sí solos, pero con efectos modestos en tumores sólidos como el gástrico. El equipo preguntó si usarlos juntos en células humanas de cáncer gástrico podría explotar las debilidades del tumor tanto en el control génico como en el metabolismo al mismo tiempo.
Probando el impacto sobre la supervivencia celular
Usando una línea celular humana de cáncer de estómago llamada MKN45, los científicos primero expusieron las células a una gama de dosis de cada fármaco por separado durante varios días, y luego a pares de dosis fijas de ambos fármacos juntos. Midieron cuántas células permanecían vivas usando una prueba de laboratorio colorimétrica estándar. Un método matemático que evalúa cómo interactúan los fármacos mostró que la combinación redujo la dosis necesaria para frenar el crecimiento celular y que los dos fármacos se comportaron de forma sinérgica en niveles bajos a moderados de mortalidad. En otras palabras, juntos fueron más efectivos de lo esperado por la suma de sus efectos individuales, permitiendo además dosis más bajas, especialmente de metformina.
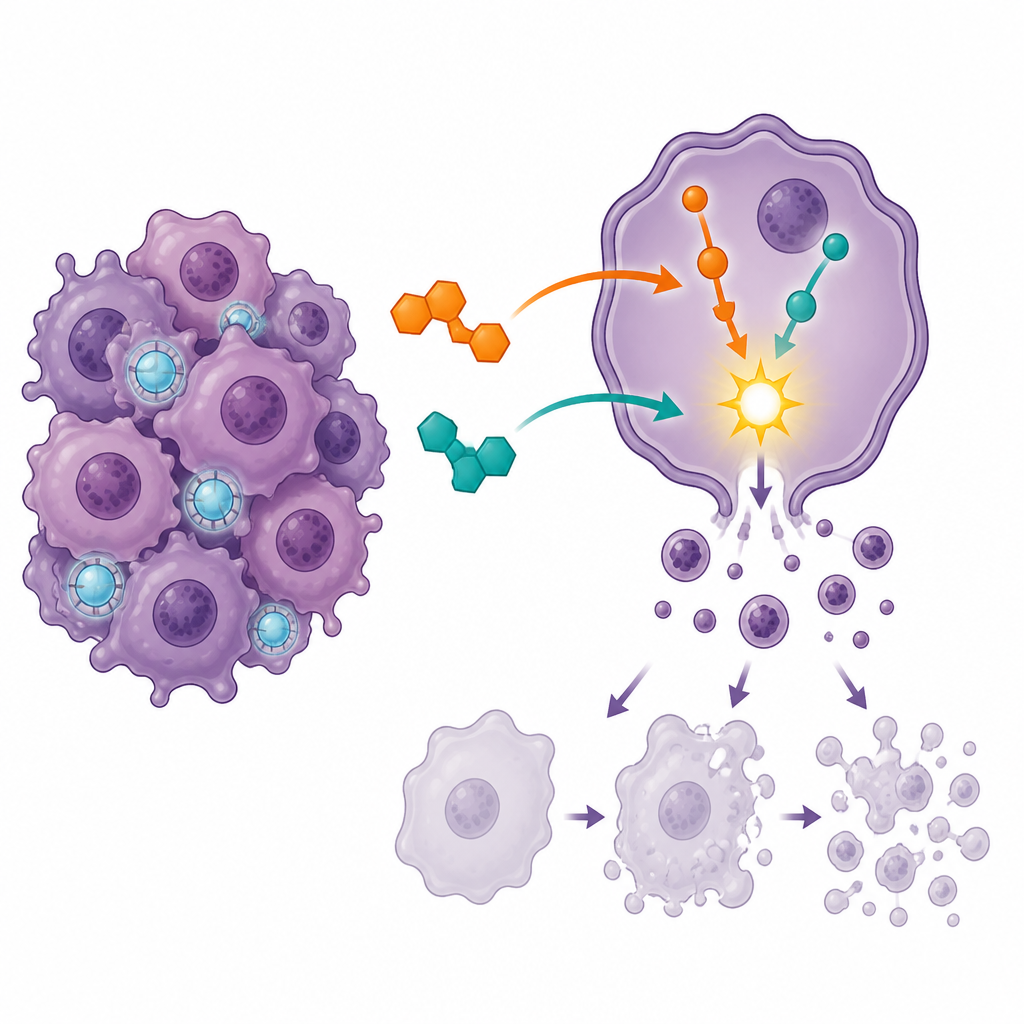
Provocando suicidio celular y deteniendo la división
Para ver cómo los fármacos estaban afectando a las células cancerosas, el equipo usó citometría de flujo, una técnica que puede distinguir células vivas de aquellas en distintas etapas de muerte programada, o apoptosis. Cada fármaco por separado empujó a más células hacia la muerte, pero la combinación provocó un salto mucho mayor en la apoptosis en fase tardía y redujo la fracción de células completamente viables. Al mismo tiempo, la mayoría de las células se vieron obligadas a detenerse en un punto de control clave del ciclo celular conocido como G2/M, donde las células normalmente se preparan para dividirse. Este fuerte atasco en la etapa de división sugiere que el tratamiento combinado atrapa a las células en un momento vulnerable, tras lo cual es más probable que experimenten autodestrucción controlada en lugar de seguir multiplicándose.
Activando los programas de muerte dentro de la célula
Los científicos analizaron luego los niveles de actividad de varios genes que actúan como interruptores internos de supervivencia y muerte. Con la combinación de fármacos, los genes que promueven la apoptosis, como BAX y dos caspasas que descomponen componentes celulares, se activaron, mientras que BCL2, un gen que normalmente ayuda a las células a resistir la muerte, se inhibió. El equilibrio entre BAX y BCL2 cambió drásticamente a favor del suicidio celular. Otro gen, ATG7, que participa en un proceso de reciclaje llamado autofagia, también se incrementó selectivamente, lo que insinúa que la degradación y limpieza controlada dentro de la célula puede cooperar con la apoptosis bajo el tratamiento. Análisis computacionales de redes y vías confirmaron que los principales temas biológicos afectados fueron las vías de apoptosis, las señales de estrés vinculadas a la proteína p53 y las rutas asociadas con la resistencia a fármacos quimioterapéuticos estándar basados en platino.
Qué podría significar esto para tratamientos futuros
En términos simples, este trabajo muestra que la decitabina y la metformina, cuando se usan juntas, hacen que las células de cáncer gástrico sean más propensas a dejar de dividirse y a activar su maquinaria interna de autodestrucción que cuando cualquiera de los fármacos se usa por separado. Al dirigirse conjuntamente al control génico defectuoso y al uso anómalo de la energía, la pareja parece presionar múltiples “interruptores de apagado” que el cáncer utiliza para sobrevivir y resistir el tratamiento. Aunque los hallazgos hasta ahora provienen de un tipo de célula cancerosa cultivada en el laboratorio, sugieren que combinar fármacos epigenéticos y metabólicos podría ayudar a superar la resistencia al tratamiento en cánceres gástricos agresivos, y proporcionan una base sólida para probar esta estrategia en modelos celulares adicionales y, eventualmente, en estudios en animales.
Cita: AlAli, M., Latifi-Navid, S. & Khakzad, M.R. Synergistic induction of apoptosis by the epigenetic modulator decitabine and metformin in gastric cancer cells highlights the potential for combination therapy. Sci Rep 16, 14951 (2026). https://doi.org/10.1038/s41598-026-42417-y
Palabras clave: cáncer gástrico, decitabina, metformina, apoptosis, terapia combinada