Clear Sky Science · zh
心肌细胞来源的TGFB3减轻心脏纤维化并在心衰中维持心脏功能
这对心脏虚弱的人为何重要
心力衰竭是一种常见且严重的病症,心脏逐渐丧失泵血能力。导致病情加重的一个主要原因是心内瘢痕形成,称为纤维化,它会使心肌僵硬并加重症状。本研究发现了一种由心脏自身肌肉细胞产生的、令人意外的保护性信号,它可以减缓这种瘢痕化过程并帮助维持心脏功能,指向一种更精确的新型心衰治疗思路。
更深入地看心脏瘢痕化
在心力衰竭中,心脏并非只是“耗损殆尽”。相反,其组织会重塑:心肌细胞肥大或死亡,结缔组织细胞沉积过多胶原,形成坚硬的瘢痕样区域。多年来,一类强大的信号分子——TGF-β家族一直与这种瘢痕化相关。然而,阻断所有形式的TGF-β被证明过于粗糙,因这些分子也参与正常修复与免疫平衡,导致严重副作用。新研究探讨了家族中的一个特定成员——称为TGF-β3——是否实际上有助于心脏抵御失控的纤维化,而非推动它。
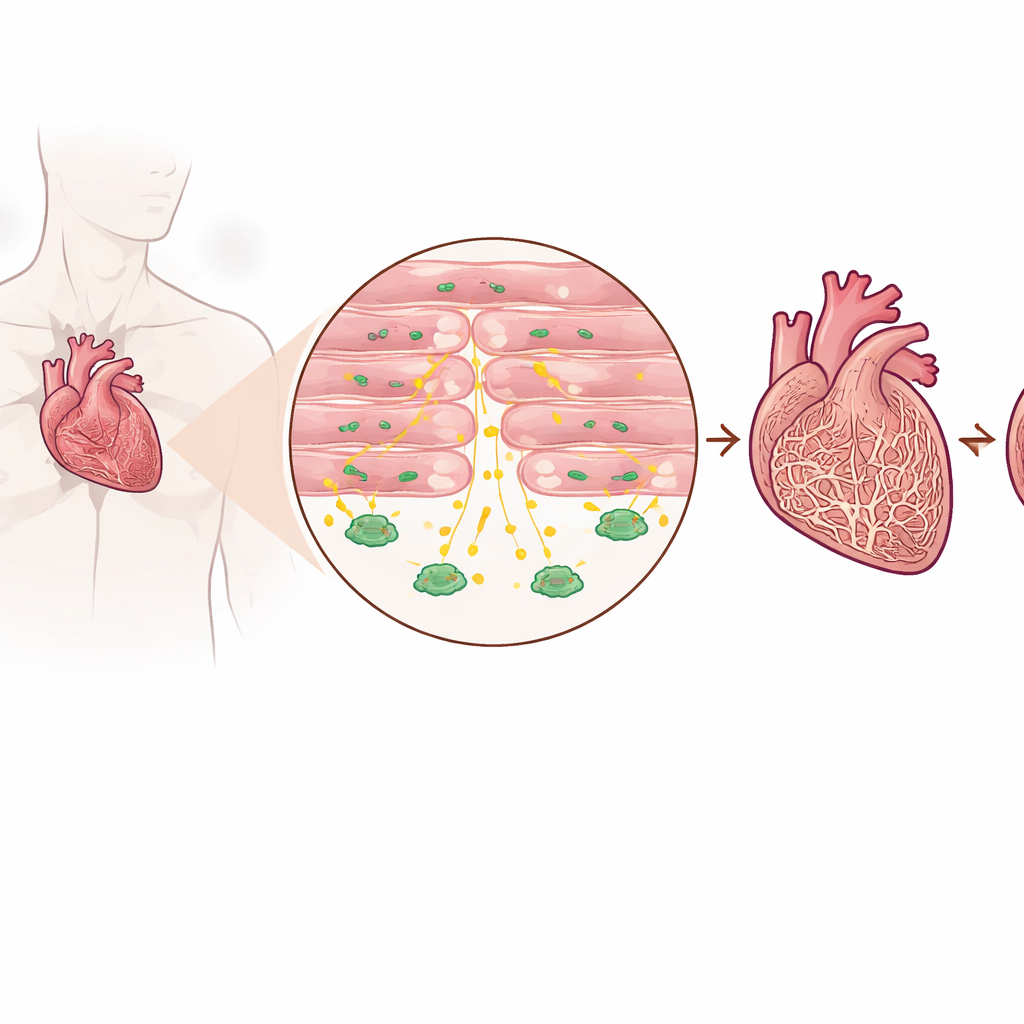
在病变心脏中检测到的保护性信号
研究者检查了来自晚期心衰患者与非心衰者的心脏组织,以及若干模拟心脏压力负荷的鼠模型。他们发现无论是在组织内还是在血液中,TGF-β3在衰竭心脏中的水平始终高于健康心脏。重要的是,这一升高并非主要来自通常形成瘢痕的细胞,而是来自心肌细胞——那些实际收缩以泵血的肌肉细胞。血中TGF-β3水平较高的患者通常也具有更高的常规心衰标志物水平,提示该分子反映了心脏所承受应激的强度。
在心肌细胞中关闭该信号
为了检验这一由心肌细胞产生的TGF-β3是有益还是有害,团队构建了可以选择性在心肌细胞中删除TGF-β3基因的小鼠。在正常静息条件下,这些小鼠的心脏在外观和功能上与其同窝鼠相似。但当动物接受一种收缩离开心脏的主动脉——这是诱导长期压力负荷并最终导致心衰的标准手术——差异变得明显。缺失心肌细胞TGF-β3的小鼠出现更差的泵血功能、心脏更为增大,以及肌纤维间更大量的胶原沉积,相较于在相同应激下的对照动物明显更严重。
心肌细胞如何与形成瘢痕的细胞对话
深入机制研究时,研究者比较了有无心肌细胞来源TGF-β3的心脏中的基因活动。缺失该信号的心脏显示出两种已知纤维化驱动因子CTGF和SERPINE1的显著上调,这些主要由负责产生结缔组织的成纤维细胞产生。在细胞培养实验中,当成纤维细胞接触经典的瘢痕化信号TGF-β1时,它们开启了这些纤维化基因并转为活化、产基质状态。然而,在此环境中加入TGF-β3则抑制了这种反应。暴露于来自缺失TGF-β3心肌细胞培养上清的成纤维细胞比暴露于正常心肌细胞上清的成纤维细胞更为活化,证实心肌细胞通常分泌一种能抑制成纤维细胞过度活性的因子。
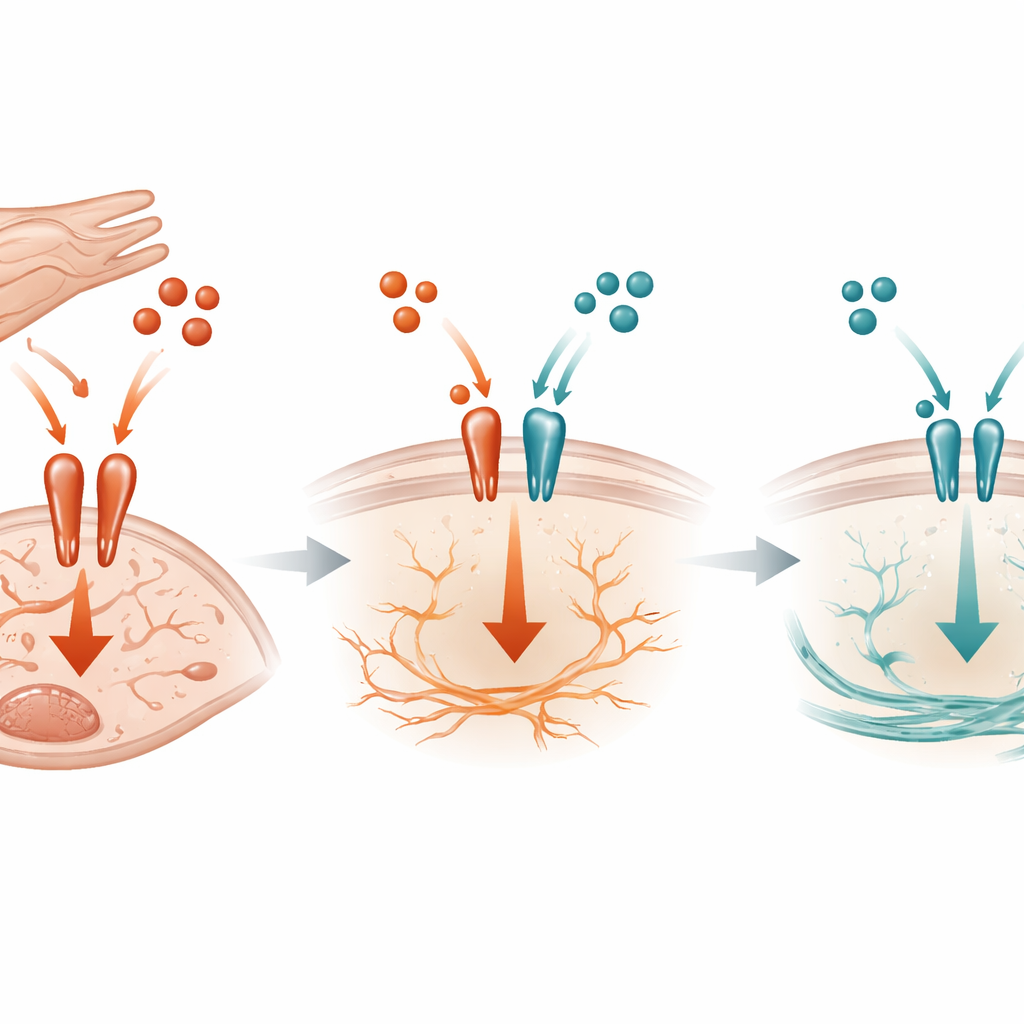
细胞表面上的分子拉锯战
在分子水平上,该研究显示TGF-β3像一种竞争性刹车,抑制更具侵袭性的TGF-β1信号。两种分子都使用成纤维细胞表面相同的受体复合体来触发细胞内活动。生化实验表明,TGF-β3可以结合这些受体并限制TGF-β1的结合,从而降低细胞内关键开关SMAD3的激活。当在压力负荷下小鼠缺失心肌细胞来源的TGF-β3时,SMAD3激活增加,CTGF和SERPINE1上升,纤维化加速。值得注意的是,这一效应并不依赖于通路内另一已知抑制因子,表明对受体的简单竞争是该保护机制的核心部分。
这对未来治疗意味着什么
对非专业读者而言,核心信息是:衰竭的心脏不仅是瘢痕的受害者;它也尝试自我保护。心肌细胞释放TGF-β3作为一种局部的内在防御,抗衡更强的促瘢痕信号,防止结缔组织过度活跃。当这种保护性信号缺失时,纤维化加剧,心脏功能更快衰退。与其全面阻断整个TGF-β系统,未来的治疗或许可针对性地增强或模拟心脏内的TGF-β3,强化器官自身限制有害瘢痕的能力,同时保留其它组织所需的修复功能。
引用: Xuan, J., Zhou, J., Huang, Y. et al. Cardiomyocyte-derived TGFB3 attenuates cardiac fibrosis and preserves cardiac function in heart failure. Sci Rep 16, 11534 (2026). https://doi.org/10.1038/s41598-026-42367-5
关键词: 心力衰竭, 心脏纤维化, TGF-β3, 心肌细胞, 成纤维细胞信号