Clear Sky Science · nl
Door cardiomyocyten afgegeven TGFB3 vermindert cardiale fibrose en behoudt hartfunctie bij hartfalen
Waarom dit belangrijk is voor mensen met een verzwakt hart
Hartfalen is een veelvoorkomende en ernstige aandoening waarbij het hart geleidelijk zijn pompvermogen verliest. Een belangrijke boosdoener is littekenvorming binnen het hart, fibrose genoemd, die het hartspierweefsel verstijft en de klachten verergert. Deze studie onthult een verrassend beschermend signaal dat door de hartspiercellen zelf wordt geproduceerd en dat het verhardingsproces kan vertragen en zo de hartfunctie kan helpen behouden. Dat wijst op een nieuwe, meer gerichte manier om hartfalen te behandelen.
Een nadere blik op hartlittekenvorming
Bij hartfalen slijt het hart niet simpelweg. In plaats daarvan ondergaat het weefsel een remodelering: spiercellen vergroten of sterven af, en bindweefselcellen leggen overtollig collageen neer, waardoor harde, littekenachtige gebieden ontstaan. Jarenlang is een krachtige familie van signaalmoleculen, bekend als TGF-beta, in verband gebracht met deze fibrose. Het blokkeren van alle vormen van TGF-beta bleek echter te grofmazig: het veroorzaakte ernstige bijwerkingen omdat deze moleculen ook bijdragen aan normale reparatie en immuunbalans. De nieuwe studie onderzoekt of één specifiek familielid, TGF-beta3, mogelijk het hart juist helpt beschermen tegen voortschrijdende fibrose in plaats van die aan te jagen.
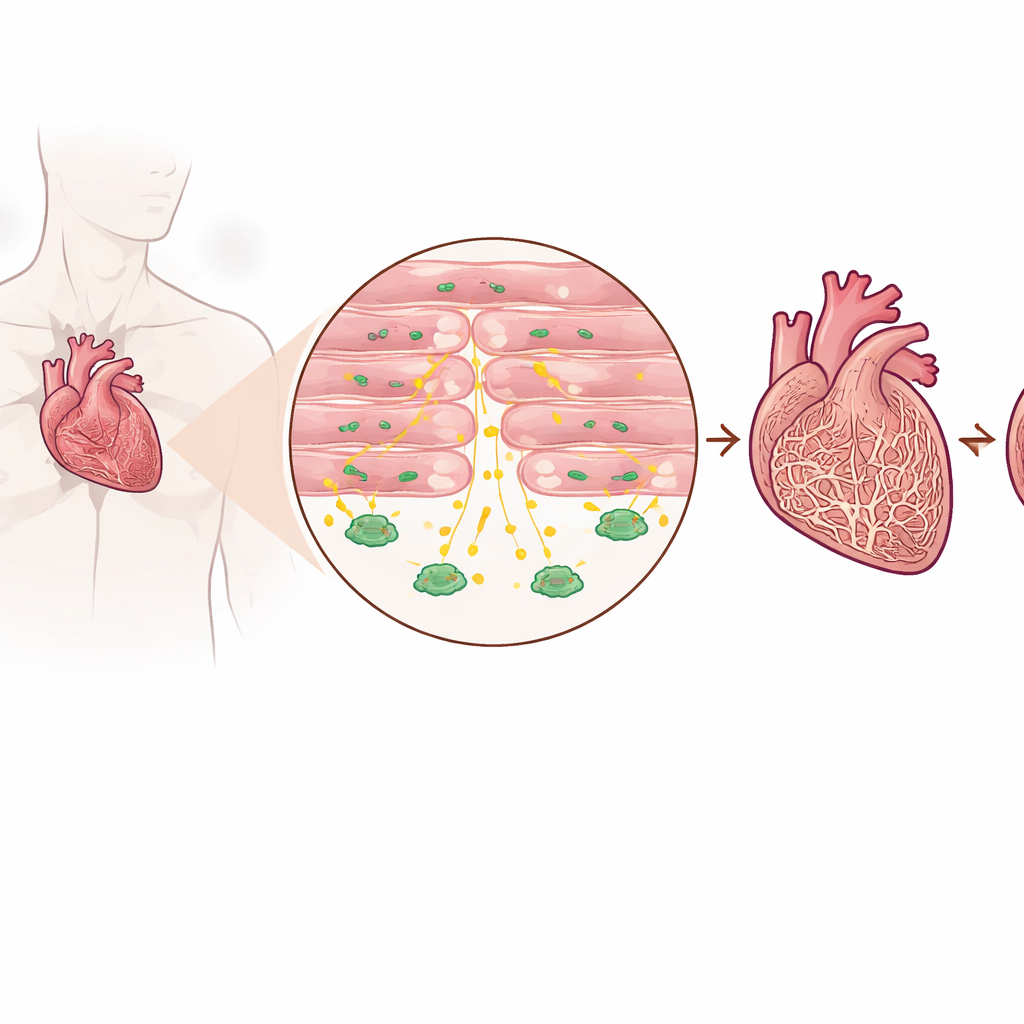
Een beschermend signaal detecteren in zieke harten
De onderzoekers bestudeerden hartweefsel van patiënten met gevorderd hartfalen en van mensen zonder hartfalen, evenals verschillende muismodellen die drukbelasting van het hart nabootsen. Ze vonden dat de niveaus van TGF-beta3 consequent hoger waren in falende harten dan in gezonde, zowel in het weefsel zelf als in de bloedbaan. Belangrijk is dat deze toename niet voornamelijk afkomstig was van de gebruikelijke littekenvormende cellen, maar van cardiomyocyten — de spiercellen die daadwerkelijk samentrekken om bloed te pompen. Patiënten met hogere bloedspiegels van TGF-beta3 hadden vaak ook hogere waarden van een standaard marker voor hartfalen, wat suggereert dat dit molecuul de mate van stress weerspiegelt waaronder het hart staat.
Het signaal in hartspiercellen uitschakelen
Om te testen of dit door cardiomyocyten geproduceerde TGF-beta3 behulpzaam of schadelijk was, creëerde het team muizen waarin het gen voor TGF-beta3 selectief kon worden verwijderd, uitsluitend in hartspiercellen. Onder normale, rustende omstandigheden zagen de harten van deze muizen er en functioneerden ze grotendeels hetzelfde als die van hun nestgenoten. Maar wanneer de dieren werden onderworpen aan een ingreep die de hoofdslagader die het hart verlaat vernauwt — een standaardmethode om chronische drukbelasting en uiteindelijk hartfalen te induceren — werden de verschillen duidelijk. Muizen zonder TGF-beta3 in hun cardiomyocyten ontwikkelden een slechtere pompfunctie, grotere harten en veel meer collageenophoping tussen spiervezels dan controledieren die aan dezelfde belasting werden blootgesteld.
Hoe hartspiercellen communiceren met littekenvormende cellen
Om het mechanisme te doorgronden vergeleken de onderzoekers genactiviteit in harten met en zonder cardiomyocytair TGF-beta3. Harten die dit signaal misten, toonden een sterke toename van twee bekende aanjagers van fibrose, CTGF en SERPINE1, die voornamelijk door fibroblasten worden geproduceerd — de cellen die verantwoordelijk zijn voor de aanmaak van bindweefsel. In kweekexperimenten, wanneer fibroblasten werden blootgesteld aan het klassieke littekenmakende signaal TGF-beta1, zetten zij deze fibrotische genen aan en namen ze een geactiveerde, matrix-producerende staat aan. Het toevoegen van TGF-beta3 aan de reactie dempte deze respons echter. Fibroblasten die werden blootgesteld aan medium afkomstig van TGF-beta3-deficiente cardiomyocyten raakten meer geactiveerd dan fibroblasten die medium van normale cardiomyocyten kregen, wat bevestigt dat de spiercellen doorgaans een factor uitscheiden die overmatige fibroblastactiviteit remt.
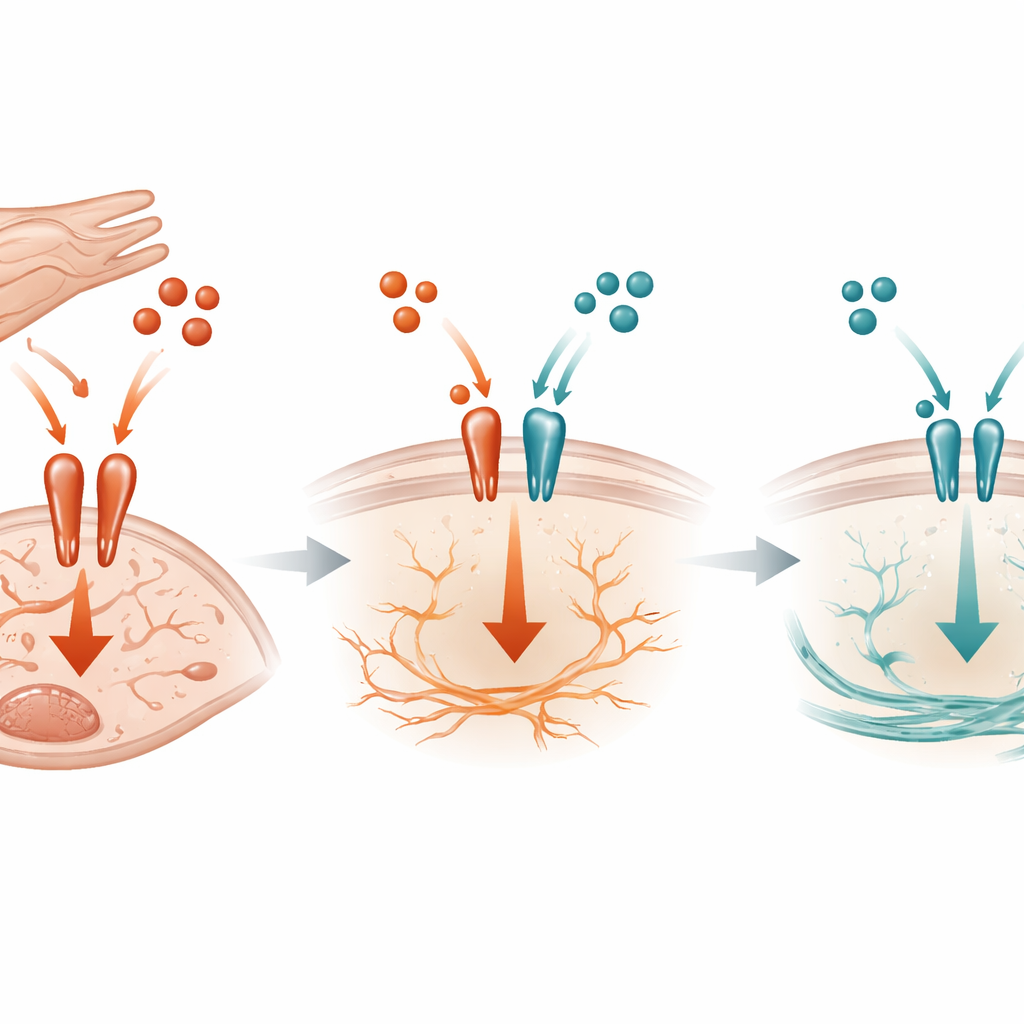
Een moleculaire touwtrek aan het celoppervlak
Op moleculair niveau toont de studie aan dat TGF-beta3 fungeert als een competitieve rem op het meer agressieve TGF-beta1-signaal. Beide moleculen gebruiken hetzelfde receptorkomplex op het oppervlak van fibroblasten om activiteit binnen de cel te activeren. Biochemische experimenten lieten zien dat TGF-beta3 aan deze receptoren kan binden en daarmee beperkt hoeveel TGF-beta1 zich kan vasthechten, waardoor de activatie van een belangrijke schakelaar binnen de cel, genaamd SMAD3, afneemt. Wanneer cardiomyocytair TGF-beta3 ontbreekt bij muizen onder drukbelasting, stijgt de SMAD3-activatie, nemen CTGF en SERPINE1 toe en versnelt de fibrose. Opvallend is dat dit effect niet afhankelijk leek van een andere bekende remmer binnen de route, wat suggereert dat eenvoudige competitie om de receptor een centraal onderdeel is van het beschermende mechanisme.
Wat dit kan betekenen voor toekomstige behandelingen
Voor niet-specialisten is de kernboodschap dat het falende hart niet alleen een slachtoffer van littekenvorming is; het probeert zichzelf ook te beschermen. Hartspiercellen geven TGF-beta3 af als een lokaal, ingebouwd verdedigingsmechanisme dat tegen sterkere pro-fibrotische signalen inwerkt en voorkomt dat het bindweefsel in overdrive gaat. Wanneer dit beschermende signaal ontbreekt, verergert de fibrose en gaat de hartfunctie sneller achteruit. In plaats van het hele TGF-beta-systeem te blokkeren, zouden toekomstige therapieën er wellicht op gericht kunnen zijn TGF-beta3 specifiek in het hart te versterken of na te bootsen, zodat het orgaan zijn eigen vermogen om schadelijke littekenvorming te beperken behoudt terwijl noodzakelijke herstelprocessen in andere weefsels onaangetast blijven.
Bronvermelding: Xuan, J., Zhou, J., Huang, Y. et al. Cardiomyocyte-derived TGFB3 attenuates cardiac fibrosis and preserves cardiac function in heart failure. Sci Rep 16, 11534 (2026). https://doi.org/10.1038/s41598-026-42367-5
Trefwoorden: hartfalen, cardiale fibrose, TGF-beta3, cardiomyocyten, fibroblastsignaal