Clear Sky Science · he
ה-TGFB3 שמקורו בתאי שריר הלב מפחית פיברוזיס קרדיאלי ושומר על תפקוד הלב בלב לכושל
מדוע זה חשוב לאנשים עם לב חלש
אי־ספיקה לבבית היא מחלה נפוצה וחמורה שבה הלב מאבד בהדרגה את יכולתו לשאוב דם. גורם מרכזי הוא יצירת צלקות בתוך הלב, המכונה פיברוזיס, שמקשיחה את רקמת שריר הלב ומחמירה את התסמינים. המחקר הזה חושף אות מגן מפתיע שמייצרים תאי השריר של הלב עצמם, ואשר יכול להאט את תהליך ההתמצקות הזה ולעזור לשמר את תפקוד הלב — מה שמצביע על גישה חדשה ומדויקת יותר לטיפול באי־ספיקה לבבית.
מבט מקרוב על צלקות בלב
באיי־ספיקה לבבית, הלב לא פשוט "מתבל". במקום זאת, רקמותיו מתרכבות מחדש: תאי השריר מתרחבים או מתים, ותאי החיבור מפרישים קולגן עודף, ויוצרים אזורים קשים דמויי צלקת. במשך שנים משפחת מולקולות איתות חזקה הידועה כ‑TGF‑beta נקשרה לתהליך זה. עם זאת, חסימת כל צורות ה‑TGF‑beta התגלתה ככלי גס מדי שגורם לתופעות לוואי קשות, כיוון שמולקולות אלה גם מסייעות בתיקון נורמלי ובאיזון חיסוני. העבודה החדשה שואלת האם אחד מחברי המשפחה, שנקרא TGF‑beta3, עלול דווקא לעזור ללב להגן על עצמו מפיברוזיס מתמשך במקום לגרום לו.
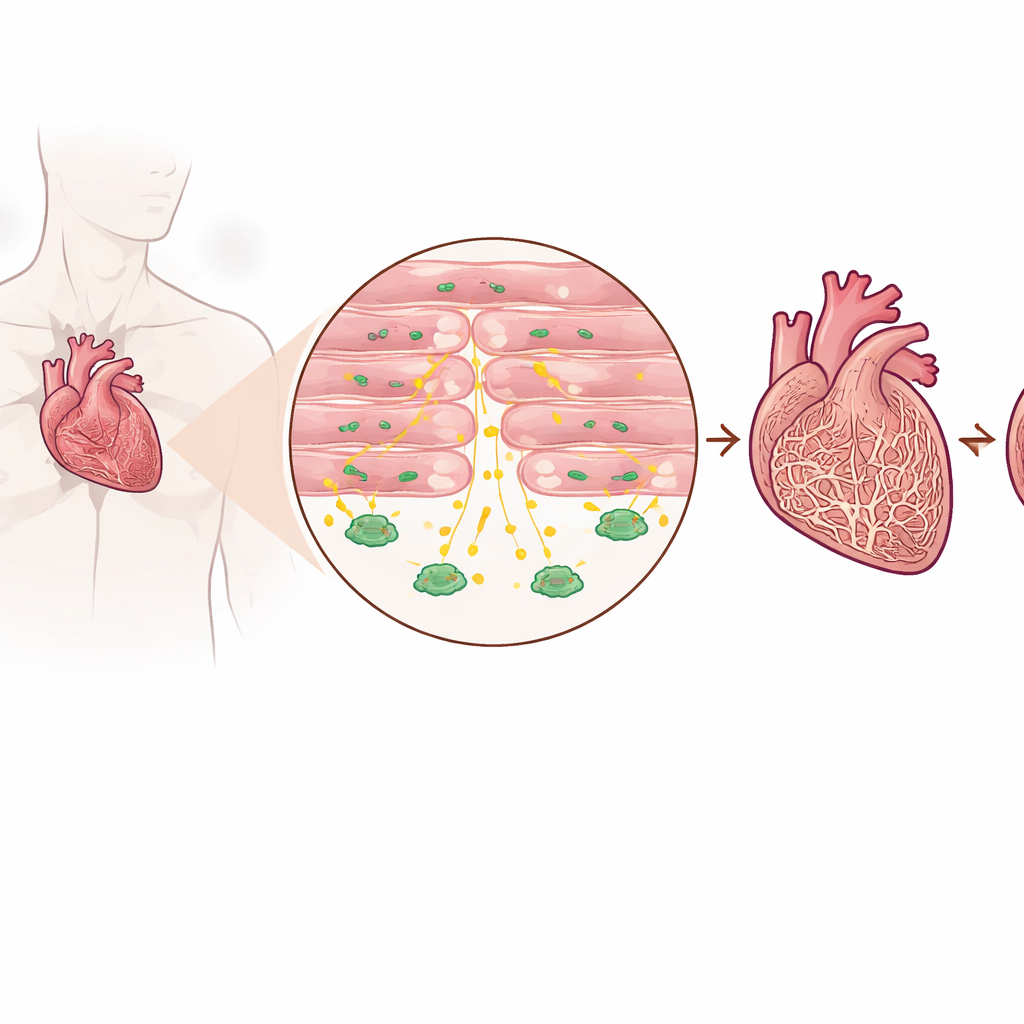
זיהוי אות מגן בלב חולה
החוקרים בדקו רקמת לב מחולים עם אי־ספיקה מתקדמת ומאנשים ללא אי־ספיקה, וכן במספר מודלים של עכברים המדמים עומס לחץ על הלב. הם מצאו שרמות ה‑TGF‑beta3 היו בעקביות גבוהות יותר בלבבות הכושלים מאשר בבריאים, הן ברקמה עצמה והן במחזור הדם. חשוב מכך, העלייה הזו לא נבעה בעיקר מהתאים הנוטים ליצור צלקת, אלא מהקרדיומיוציטים — תאי השריר שמקיימים את ההתכווצות לשאיבת דם. לחולים עם רמות גבוהות יותר של TGF‑beta3 בדם נטו גם להיות רמות גבוהות יותר של סימן שגרתי לאי־ספיקה לבבית, מה שמרמז שהמולקולה הזו משקפת את עוצמת הלחץ שהלב נמצא תחתיה.
כיבוי האות בתאי שריר הלב
כדי לבדוק האם ה‑TGF‑beta3 שמיוצר בקרדיומיוציטים מועיל או מזיק, הצוות הנדס עכברים שבהם ניתן היה למחוק באופן סלקטיבי את הגן ל‑TGF‑beta3 רק בתאי שריר הלב. בתנאים רגילים ומנוחתיים, לֵבָבם של עכברים אלה נראה ותפקד בדומה לזה של אחיהם. אך כאשר בעלי החיים עברו פרוצדורה שמצרה את העורק הראשי היוצא מהלב — שיטה סטנדרטית להשראת עומס לחץ כרוני ואי־ספיקה לבבית — ההבדלים הפכו בולטים. עכברים חסרי TGF‑beta3 בקרדיומיוציטים פיתחו תפקוד שאיבה גרוע יותר, לבבות גדולים יותר והרבה יותר הצטברות קולגן בין סיבי השריר לעומת בעלי החיים הביקורתיים שנחשפו לאותו לחץ.
כיצד תאי שריר הלב מתקשרים לתאים היוצרים צלקת
בחיפוש אחרי המנגנון, המשווים הפעילו של החוקרים השוו פעילות גנים בלבבות עם ובלי TGF‑beta3 של הקרדיומיוציטים. לבבות שחסרו את האות הראו עלייה חדת בשני גורמי פיברוזה ידועים, CTGF ו‑SERPINE1, שמיוצרים בעיקר על־ידי פיברובלסטים — התאים האחראים ליצירת רקמת החיבור. בניסויי תרבית תאים, כאשר פיברובלסטים חשופים לאות הצלקת הקלאסי TGF‑beta1 הם מדליקים את הגנים הפיברוטיים הללו ומקבלים מצב פעיל שיוצר מטריצה. הוספת TGF‑beta3 לתערובת, עם זאת, החלישה את התגובה הזו. פיברובלסטים שחושפו לנוזל מתאי קרדיומיוציטים חסרי TGF‑beta3 הפכו ליותר פעילים מאחרים שחשפו לנוזל מתאי קרדיומיוציטים נורמליים, מה שאישר שתאי השריר בדרך כלל מופקים גורם שמגביל פעילות יתר של הפיברובלסטים.
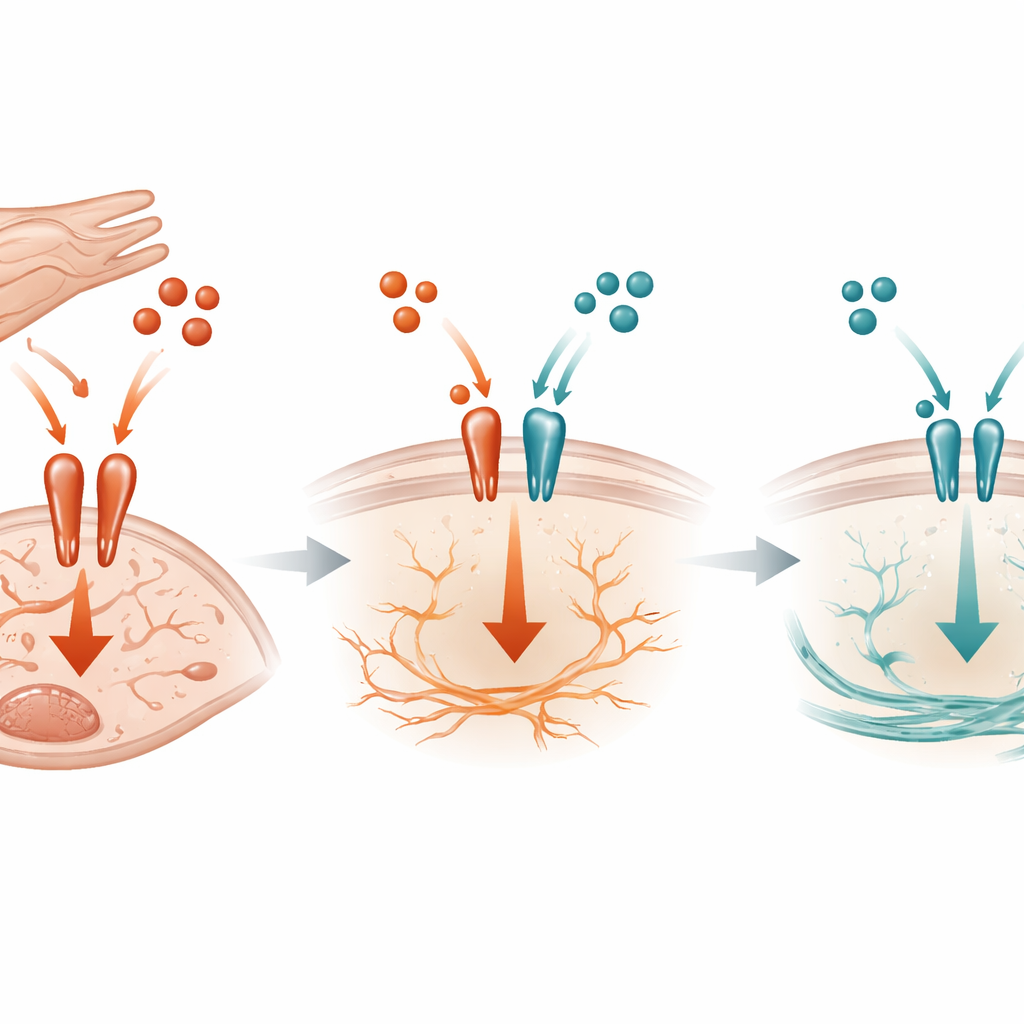
מאבק מולקולרי על פני שטח התא
ברמה המולקולרית, המחקר מראה כי ה‑TGF‑beta3 פועל כבלם תחרותי לאות היותר אגרסיבי של TGF‑beta1. שתי המולקולות משתמשות באותו קומפלקס קולטנים על פני שטח הפיברובלסט כדי להפעיל פעילות בתוך התא. ניסויים ביוכימיים חשפו כי TGF‑beta3 יכול להיקשר לקולטים אלה ולהגביל עד כמה TGF‑beta1 יכול להיצמד, ובכך לצמצם הפעלה של מתג מרכזי בתוך התא שנקרא SMAD3. כאשר מקור ה‑TGF‑beta3 מקרדיומיוציטים נעדר בעכברים תחת עומס לחץ, הפעלת SMAD3 עולה, CTGF ו‑SERPINE1 עולים, והפיברוזיס מואץ. יש לציין כי אפקט זה לא התבסס על מעכב ידוע אחר במסלול, מה שמרמז שתחרות פשוטה על הקולטן היא חלק מרכזי במנגנון המגן.
מה משמעות הדבר לטיפולים עתידיים
ללא מומחיות ספציפית, המסר המרכזי הוא שהלב הכושל אינו רק קורבן לצלקת; הוא גם מנסה להגן על עצמו. תאי שריר הלב משחררים TGF‑beta3 כהגנה מקומית ובנויה שמושכת נגד אותות פרו‑צלקת חזקים יותר ושומרת על רקמת החיבור מלהיכנס למצב יתר. כאשר אות מגן זה חסר, הפיברוזיס מחמיר ותפקוד הלב נפגע מהר יותר. במקום לחסום את כל מערכת ה‑TGF‑beta, טיפולים עתידיים עשויים לכוון להגביר או לחקות ספציפית את ה‑TGF‑beta3 בלב, ולחזק את יכולתו המובנית של האיבר להגביל צלקות מזיקות תוך שמירה על תהליכי ריפוי נדרשים ברקמות אחרות.
ציטוט: Xuan, J., Zhou, J., Huang, Y. et al. Cardiomyocyte-derived TGFB3 attenuates cardiac fibrosis and preserves cardiac function in heart failure. Sci Rep 16, 11534 (2026). https://doi.org/10.1038/s41598-026-42367-5
מילות מפתח: אי־ספיקה לבבית, צלקת לבבית (פיברוזיס), TGF‑beta3, קרדיומיוציטים, אותות לפיברובלסטים