Clear Sky Science · tr
Kardiyomiyot kaynaklı TGFB3, kalp yetmezliğinde kardiyak fibrozisi azaltır ve kalp fonksiyonunu korur
Zayıf kalbi olan kişiler için bunun önemi
Kalp yetmezliği, kalbin kan pompalama yeteneğini zamanla kaybettiği yaygın ve ciddi bir durumdur. Bunun başlıca nedenlerinden biri kalp içinde oluşan skarlaşma, yani fibrozistir; bu durum kalp kasını sertleştirir ve belirtileri kötüleştirir. Bu çalışma, kalbin kendi kas hücreleri tarafından üretilen ve bu skarlaşma sürecini yavaşlatabilen, kalp fonksiyonunu korumaya yardımcı olabilecek şaşırtıcı bir koruyucu sinyali ortaya koyuyor; bu da kalp yetmezliğine daha hassas bir yaklaşımın yolunu açıyor.
Kalp skarlaşmasına daha yakından bakış
Kalp yetmezliğinde kalbin basitçe “aşınmadığı” görülüyor. Bunun yerine doku yeniden şekilleniyor: kas hücreleri büyüyor veya ölüyor ve bağ dokusu hücreleri aşırı kollajen biriktirerek sert skar benzeri alanlar oluşturuyor. Yıllardır güçlü bir sinyal ailesi olan TGF-beta bu skarlaşmayla ilişkilendirilmişti. Ancak TGF-beta'nın tüm biçimlerini engellemek fazla kaba bir yaklaşım olduğunu gösterdi; çünkü bu moleküller normal onarım ve bağışıklık dengesine de yardımcı oluyor ve tam blokaj ciddi yan etkilere yol açtı. Yeni çalışma, TGF-beta ailesinin belirli bir üyesi olan TGF-beta3'ün, aslında fibrozisi tetiklemek yerine kalbin kendisini kontrolsüz skarlaşmaya karşı savunmasına yardımcı olup olmadığını sorguluyor.
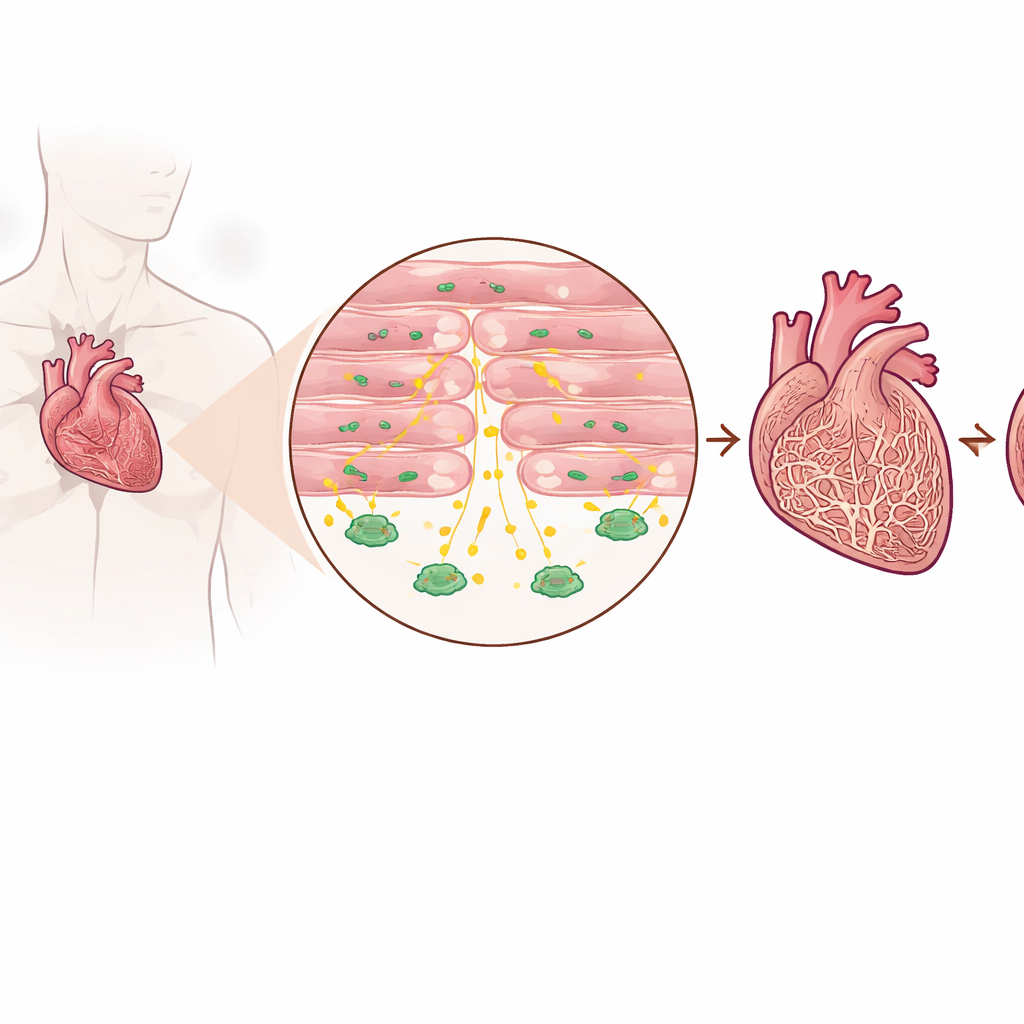
Hastalıklı kalplerde koruyucu bir sinyalin saptanması
Araştırmacılar ileri evre kalp yetmezliği olan hastaların ve kalp yetmezliği olmayan kişilerin kalp dokularını ile kalbe basınç yükünü taklit eden birkaç fare modelini incelediler. TGF-beta3 düzeylerinin, hem doku içinde hem de kan dolaşımında, başarısız kalplerde sağlıklı kalplere göre tutarlı şekilde daha yüksek olduğunu buldular. Önemli olarak, bu artış esas olarak skar oluşturan tip hücrelerden değil, kan pompalamak için kasılan kas hücreleri olan kardiyomiyositlerden geliyordu. Kanda daha yüksek TGF-beta3 düzeyine sahip hastaların, standart bir kalp yetmezliği belirteci düzeylerinin de genellikle daha yüksek olduğu görüldü; bu, bu molekülün kalbin maruz kaldığı stresin şiddetini yansıttığını düşündürüyor.
Kalp kası hücrelerinde sinyalin kapatılması
Bu kardiyomiyot kaynaklı TGF-beta3'ün faydalı mı yoksa zararlı mı olduğunu test etmek için ekip, TGF-beta3 geninin yalnızca kalp kası hücrelerinde seçici olarak silinebildiği fareler geliştirdi. Normal dinlenme koşullarında bu farelerin kalpleri, kardeşleriyle hemen hemen aynı görünümde ve işlevdeydi. Ancak hayvanlar kalpten çıkan ana atardamarı daraltan—kronik basınç yükü ve nihayetinde kalp yetmezliğini indüklemek için standart bir prosedür—bir işleme tabi tutulduğunda farklar çarpıcı hale geldi. Kardiyomiyositlerinde TGF-beta3 eksik olan fareler, aynı strese maruz kalan kontrol hayvanlarına göre daha kötü pompalama fonksiyonu, daha büyük kalpler ve kas lifleri arasına çok daha fazla kollajen birikimi geliştirdiler.
Kalp kası hücrelerinin skar oluşturan hücrelerle nasıl iletişim kurduğu
Mekaniğe daha derinlemesine bakmak için araştırmacılar, kardiyomiyosit TGF-beta3 bulunan ve bulunmayan kalplerde gen aktivitesini karşılaştırdılar. Bu sinyali kaybetmiş kalplerde, esas olarak bağ dokusu yapan fibroblastlar tarafından üretilen iki iyi bilinen fibrozis sürücüsü olan CTGF ve SERPINE1'de keskin bir artış görüldü. Hücre kültürü deneylerinde, fibroblastlar klasik skarlaşma sinyali olan TGF-beta1'e maruz bırakıldığında bu fibrotik genleri açıyor ve aktive olmuş, matris üreten bir duruma geçiyorlardı. Ancak karışıma TGF-beta3 eklenmesi bu yanıtı zayıflattı. TGF-beta3 eksik kardiyomiyotların sıvısıyla banyo edilen fibroblastlar, normal kardiyomiyotların sıvısına maruz kalanlardan daha fazla aktive oldu; bu, kas hücrelerinin normalde fibroblast aşırı aktivitesini sınırlayan bir faktör salgıladığını doğruluyor.
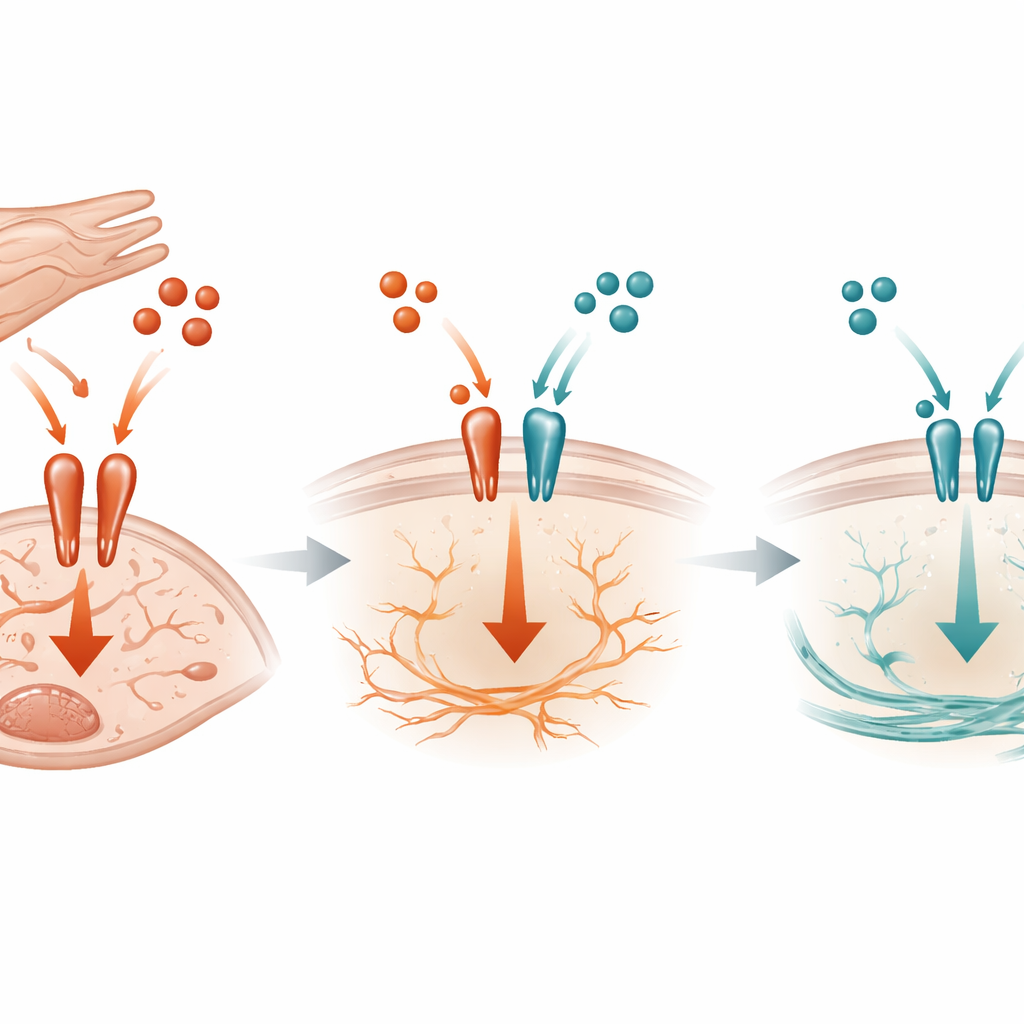
Hücre yüzeyinde moleküler bir çekişme
Moleküler düzeyde çalışma, TGF-beta3'ün daha agresif TGF-beta1 sinyaline karşı rekabetçi bir fren gibi davrandığını gösteriyor. Her iki molekül de fibroblast yüzeylerindeki aynı reseptör kompleksini kullanarak hücre içinde aktivasyonu tetikliyor. Biyokimyasal deneyler, TGF-beta3'ün bu reseptörlere bağlanabileceğini ve TGF-beta1'in ne kadar bağlanabileceğini sınırlayarak hücre içindeki anahtar bir anahtar olan SMAD3'ün aktivasyonunu azaltabildiğini ortaya koydu. Basınç yükü altındaki farelerde kardiyomiyot kaynaklı TGF-beta3 yok olduğunda SMAD3 aktivasyonu yükseliyor, CTGF ve SERPINE1 artıyor ve fibrozis hızlanıyor. Dikkate değer şekilde, bu etkinin yol içerisindeki bilinen başka bir inhibitöre bağlı olmadığı görüldü; bu da koruyucu mekanizmanın önemli bir parçasının reseptör için basit rekabet olduğunu düşündürüyor.
Gelecekteki tedaviler için anlamı
Uzman olmayan bir kişi için ana mesaj, başarısız kalbin yalnızca skarlaşmanın kurbanı olmadığı; aynı zamanda kendini korumaya çalıştığıdır. Kalp kası hücreleri, daha güçlü yara oluşturucu sinyallere karşı çekişen yerel, dahili bir savunma olarak TGF-beta3 salgılıyor ve bağ dokusunun aşırı çalışmasını engelliyor. Bu koruyucu sinyal eksik olduğunda fibrozis kötüleşiyor ve kalp fonksiyonu daha hızlı düşüyor. TGF-beta sisteminin tamamını bloklamak yerine, gelecekteki tedaviler özellikle kalpte TGF-beta3'ü artırmayı veya taklit etmeyi hedefleyebilir; bu, organın zararlı skarlaşmayı sınırlama yeteneğini güçlendirirken diğer dokularda gerekli onarımı koruyabilir.
Atıf: Xuan, J., Zhou, J., Huang, Y. et al. Cardiomyocyte-derived TGFB3 attenuates cardiac fibrosis and preserves cardiac function in heart failure. Sci Rep 16, 11534 (2026). https://doi.org/10.1038/s41598-026-42367-5
Anahtar kelimeler: kalp yetmezliği, kardiyak fibrozis, TGF-beta3, kardiyomiyositler, fibroblast sinyalleşmesi