Clear Sky Science · zh
槲皮素-4'-O-β-D-葡萄糖吡喃苷通过SIRT5介导的TFR1去琥珀酰化抑制糖尿病性肾病中的铁死亡
这对糖尿病患者为何重要
肾病是糖尿病最严重的长期并发症之一,也是需要透析或移植的主要原因。本研究探讨了一种来自植物的天然化合物——槲皮素-4'-O-β-D-葡萄糖吡喃苷(QODG),以及它如何通过阻断一种由铁和氧化应激驱动的特定细胞死亡形式来保护肾脏免受糖尿病相关损伤。理解这一过程可能为在血糖和血压控制之外开发更安全的辅助疗法打开新的思路。
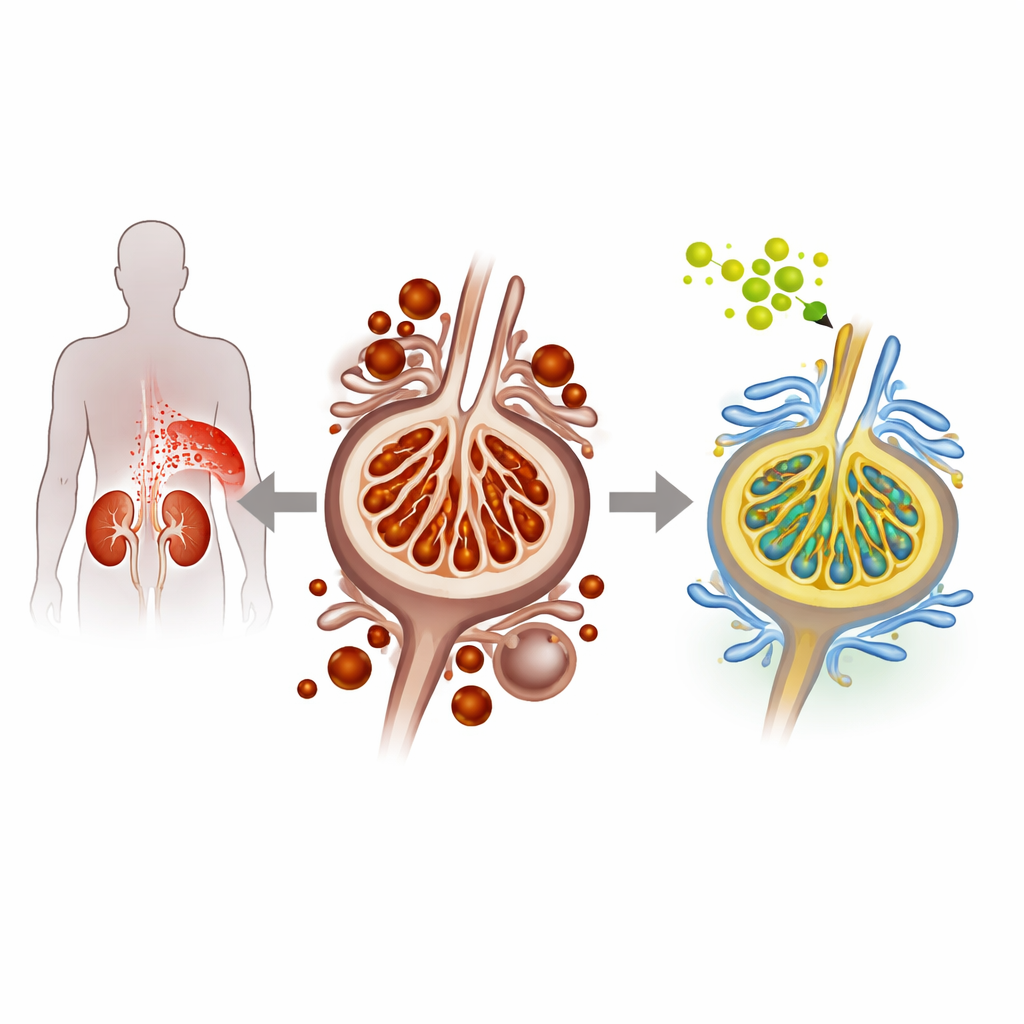
高糖如何损害肾脏的滤过细胞
在糖尿病性肾病中,高血糖逐渐损伤足细胞——这些精细的细胞衬在肾小球滤过单元并防止蛋白从尿中流失。研究者使用了培养的鼠源足细胞和糖尿病小鼠模型来模拟这一情况。在高糖条件下,足细胞出现了一种称为铁死亡的特殊细胞死亡迹象,这种死亡由过量铁和细胞膜中被氧化损伤的脂质积累所驱动。研究组观察到细胞内铁含量增加、脂质过氧化增强以及天然保护性蛋白水平下降,所有这些都指向铁死亡增强和肾脏应激加剧。
一种能缓和铁驱动损伤的植物分子
QODG是一种与槲皮素相关的类黄酮苷,槲皮素存在于许多水果和药用植物中。当研究者用QODG处理高糖条件下的足细胞时,细胞存活明显改善且呈剂量依赖性。氧化损伤指标(如脂质过氧化和丙二醛)下降,而超氧化物歧化酶和过氧化氢酶等抗氧化防御上升。同时,作为铁死亡关键防护因子的GPX4和SLC7A11蛋白水平增加,而细胞表面主要的铁输入通道转铁蛋白受体1(TFR1)水平下降。在糖尿病小鼠中,QODG处理减轻了肾结构损伤,降低了血液和尿液中的肾功能异常指标,并在促氧化力量与抗氧化系统之间恢复了更健康的平衡。
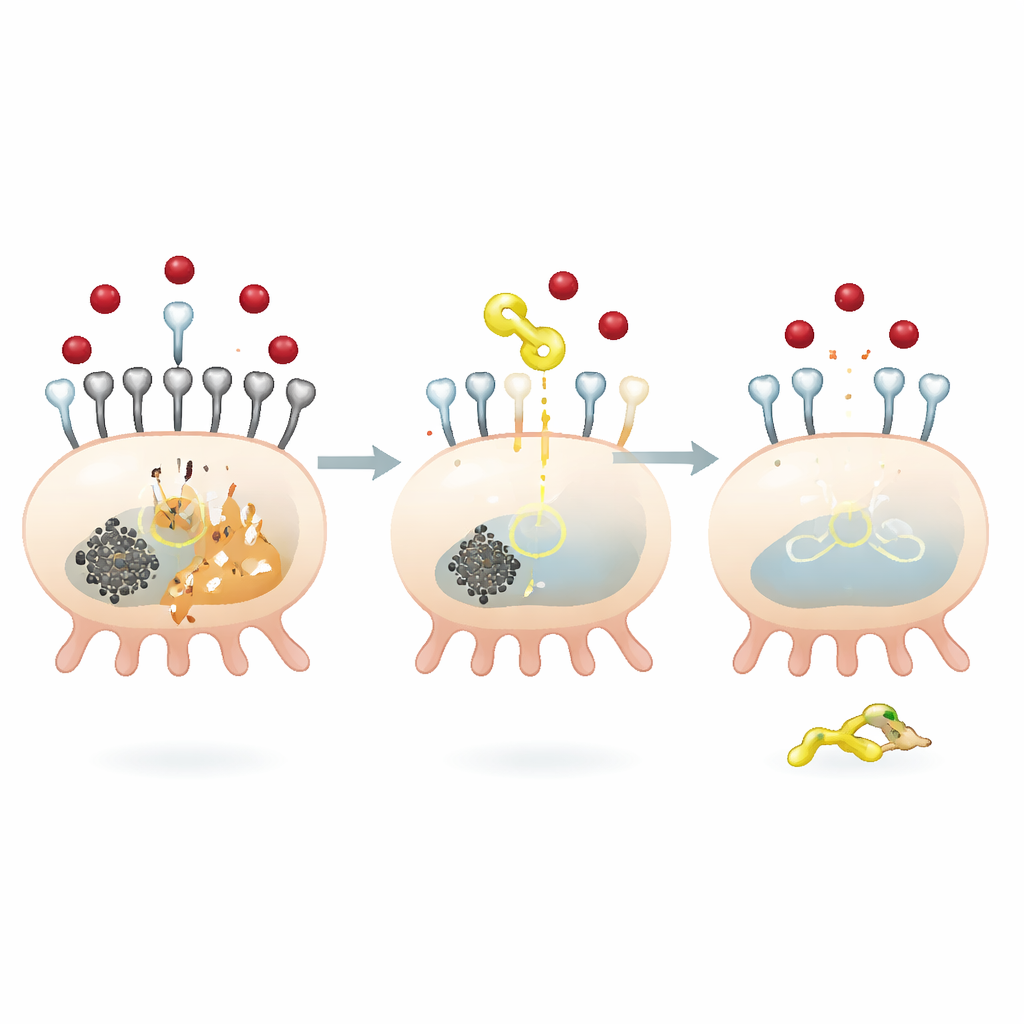
对肾细胞铁进入的分子刹车
为了解QODG如何发挥这些保护作用,研究组将注意力集中在一种名为SIRT5的蛋白上,这是一种能从其他蛋白上去除被称为琥珀酰基的小化学标签的酶。高糖使足细胞内整体琥珀酰化水平升高且SIRT5水平下降。QODG能够逆转这一现象:它提升了SIRT5,同时将整体琥珀酰化水平降低,而供体分子(琥珀酰基供体)的供应并未改变。研究者发现SIRT5特异性地调控TFR1在单个位点——氨基酸残基赖氨酸626(K626)上的琥珀酰化。当沉默SIRT5时,TFR1的琥珀酰化增加、稳定性增强且表达量上升,导致铁摄取增加和更强的铁死亡信号。相反,恢复SIRT5会降低TFR1的稳定性和表达,抑制铁流入和细胞死亡。
证明调控因子与铁门之间的联系
研究组用多种互补技术证实了SIRT5可与TFR1直接结合并调节其修饰状态。通过对TFR1不同潜在琥珀酰化位点进行突变,结果显示只有在赖氨酸626处的改变同时影响了琥珀酰化和TFR1总蛋白水平,锁定了该位点为关键控制点。生化拉下实验和基于近距离的成像分析进一步证实了SIRT5与TFR1的直接相互作用。在功能上,单独过表达SIRT5就能使足细胞更耐受铁死亡,但强制恢复TFR1水平会抹去这种保护作用,恢复铁积累和氧化损伤。这些发现将SIRT5和TFR1置于一条单一通路中,共同决定在糖尿病条件下肾细胞对铁驱动损伤的敏感性。
这可能对未来治疗意味着什么
总体而言,研究表明QODG可通过上调SIRT5进而去除TFR1的化学标签来缓解细胞和小鼠的糖尿病肾脏损伤,从而使这一铁输入“门”不稳定并抑制铁死亡。对普通读者来说,关键观点是:一种基于植物的化合物似乎通过关闭向有害细胞死亡提供原料的“铁门”来帮助肾小球滤过细胞。尽管还需要在更大动物研究乃至人体研究中进一步验证,这些结果强调了一种有前景的策略:用天然分子靶向铁处理和氧化性细胞死亡,以延缓或预防糖尿病肾病的发展。
引用: Wu, M., Ye, W. & Ye, X. Quercetin-4’-O-β-D-glucopyranoside inhibits ferroptosis though SIRT5-mediated desuccinylation of TFR1 in diabetic nephropathy. Sci Rep 16, 12384 (2026). https://doi.org/10.1038/s41598-026-41148-4
关键词: 糖尿病性肾病, 肾脏保护, 铁死亡, 类黄酮, 铁代谢