Clear Sky Science · ar
كويرسيتين-4’-O-β-D-غلوكوبيرانوسيد يثبط الفيروبتوزيس عبر إزالة السكسينيل التي يوسِّطها SIRT5 من TFR1 في اعتلال الكلية السكري
لماذا يهم هذا الأشخاص المصابين بالسكري
تُعد أمراض الكلى إحدى أخطر المضاعفات طويلة الأمد للسكري وأحد الأسباب الرئيسية التي تدفع الأشخاص إلى الخضوع لغسيل الكلى أو الحاجة إلى زرع الأعضاء. تستقصي هذه الدراسة مركبًا طبيعيًا مستخلصًا من النبات، كويرسيتين-4’-O-β-D-غلوكوبيرانوسيد (QODG)، وكيف قد يحمي الكلى من الأضرار المرتبطة بالسكري عن طريق حجب شكل محدد من موت الخلايا الذي يقوده الحديد والإجهاد التأكسدي. قد يفتح فهم هذه الآلية الطريق لعلاجات جديدة أكثر أمانًا تكمل السيطرة التقليدية على سكر الدم وضغط الدم.
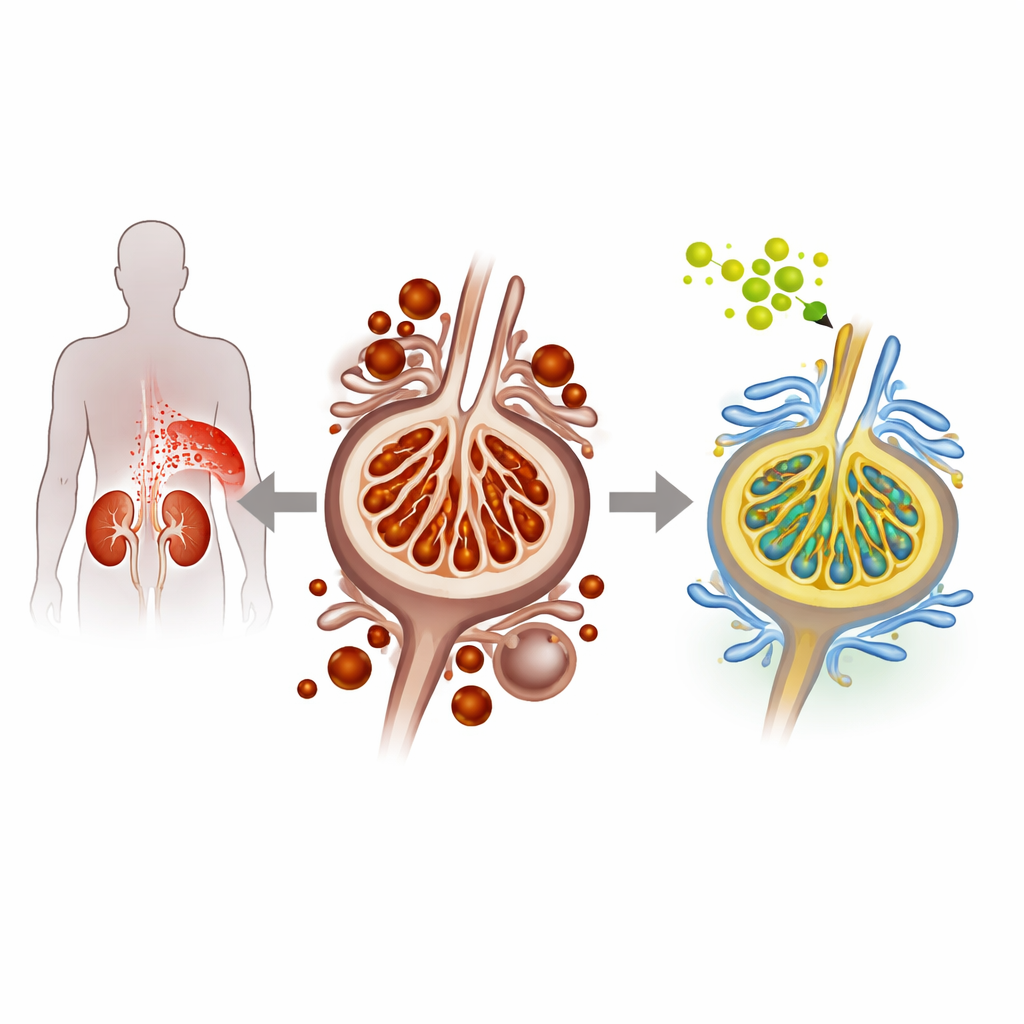
عندما يضر السكر خلايا مرشحات الكلية
في اعتلال الكلية السكري، يؤدي ارتفاع سكر الدم تدريجيًا إلى إتلاف البروتوسيتات (podocytes)، وهي خلايا حساسة تبطن وحدات الترشيح في الكلية وتمنع تسرب البروتين إلى البول. استخدم الباحثون خلايا بروتوسيتات مزروعة من الفئران ونموذج فأري سكري لمحاكاة هذه الحالة. تحت ظروف درجة سكر مرتفعة، ظهرت على البروتوسيتات علامات نوع خاص من موت الخلايا يُسمى الفيروبتوزيس، والذي يغذيه فائض الحديد وتراكم الدهون المؤكسدة والمتضررة في أغشية الخلايا. لوحظ وجود كمية أكبر من الحديد داخل الخلايا، وزيادة تأكسد الدهون، وانخفاض مستويات البروتينات الوقائية الطبيعية، وكلها تشير إلى تفاقم الفيروبتوزيس وضغط أعظم على الكلى.
جزيء نباتي يخفف الضرر المدفوع بالحديد
QODG هو غليكوسيد فلافونويد مرتبط بالكويرسيتين، المركب الموجود في العديد من الفواكه والنباتات الطبية. عندما عالج الباحثون بروتوسيتات تحت سكر مرتفع بـ QODG، تحسنت بقاء الخلايا بطريقة تعتمد على الجرعة بوضوح. انخفضت مؤشرات الضرر التأكسدي، مثل تأكسد الدهون والمالونالديهايد، بينما ارتفعت الدفاعات المضادة للأكسدة مثل سوبرأوكسيد ديسميوتاز والكاتالاز. في الوقت نفسه، زادت مستويات البروتين لكل من GPX4 وSLC7A11، وهما حارسان أساسيان ضد الفيروبتوزيس، وانخفضت مستويات مستقبل الترانسفيرين 1 (TFR1)، بوابة إدخال الحديد الرئيسية على سطح الخلية. في الفئران المصابة بالسكري، خفف علاج QODG من التلف البنيوي للكلى، وخفّض مؤشرات اختلال وظائف الكلى في الدم والبول، وأعاد توازنًا صحيًا بين القوى المؤكسدة الضارة وأنظمة المضادات المؤكسدة الوقائية.
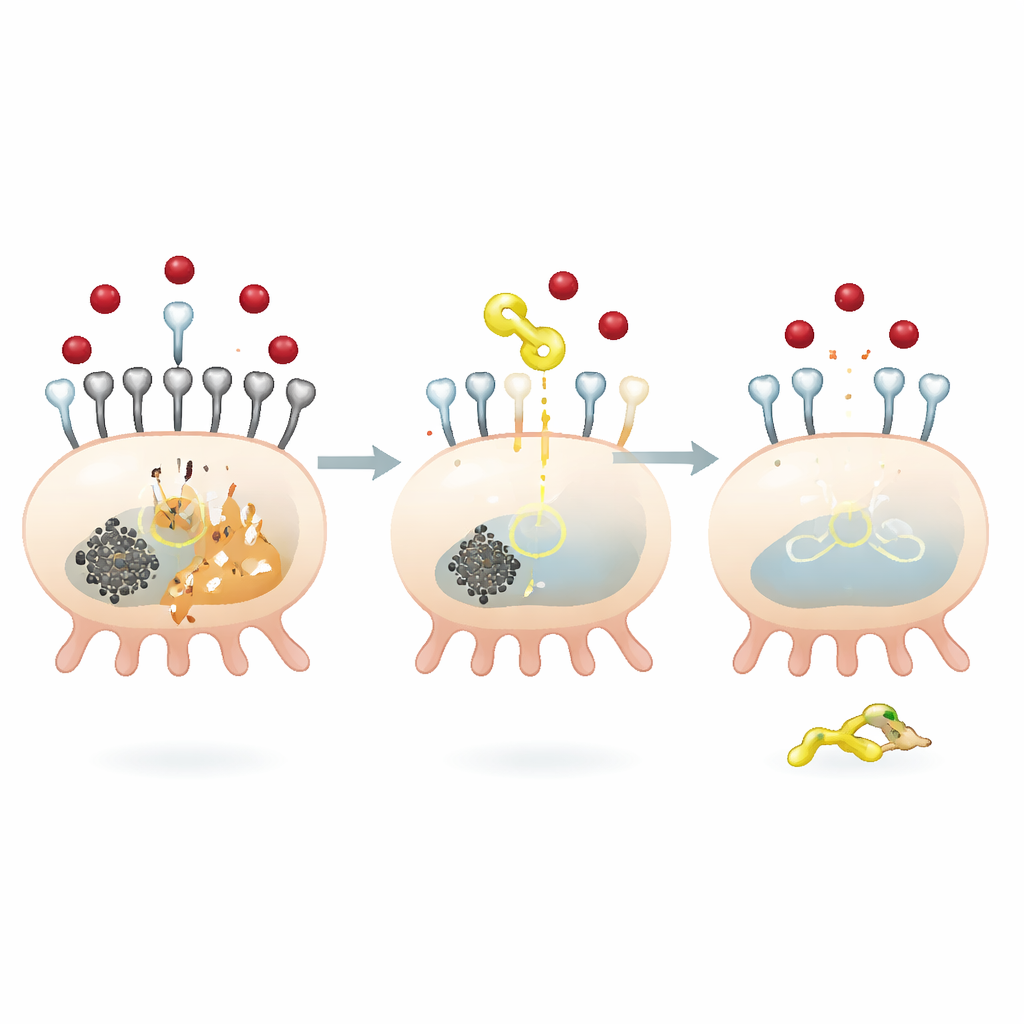
فرملة جزيئية لدخول الحديد إلى خلايا الكلية
لفهم كيفية إحداث QODG لهذه التأثيرات الوقائية، ركز الفريق على بروتين يسمى SIRT5، وهو إنزيم يزيل علامة كيميائية صغيرة تُعرف بمجموعة السكسينيل من بروتينات أخرى. زيادة الجلوكوز رفعت مستوى السكسينلة العامة داخل البروتوسيتات وخفضت مستويات SIRT5. عكس QODG هذا التأثير: عزز SIRT5 بينما خفض السكسينلة الإجمالية، من دون تغيير إمداد جزيء مانح السكسينيل. وجد الباحثون أن SIRT5 يتحكم تحديدًا بسكسينلة TFR1 في موقع واحد، وهو بقاعدة أمينية تُدعى ليسين 626. عند إسكات SIRT5، ازداد سكسينلة TFR1 وأصبح أكثر استقرارًا وأكثر وفرة، مما أدى إلى زيادة امتصاص الحديد وتعزيز إشارات الفيروبتوزيس. وبالعكس، أدت إعادة SIRT5 إلى تقليل استقرار وتعبير TFR1، وكبح تدفق الحديد وموت الخلايا.
إثبات الرابط بين المنظِّم وبوابة الحديد
استخدم الفريق عدة تقنيات تكميلية لتأكيد أن SIRT5 يرتبط فعليًا بـ TFR1 ويعدّل حالة تعديله. أظهر تغيير مواقع سكسينلة محتملة مختلفة على TFR1 أن التغييرات عند ليسين 626 فقط هي التي عدّلت كلًا من السكسينلة ومستويات بروتين TFR1 الكلية، محددةً هذا الموقع كنقطة تحكم حاسمة. أكدت تجارب السحب الحيوي والتحليل البصري القائم على القرب التفاعلي التماس المباشر بين SIRT5 وTFR1. وظيفيًا، جعلت الإفراط في التعبير عن SIRT5 الخلايا أكثر مقاومة للفيروبتوزيس بمفرده، لكن إجبار ارتفاع مستويات TFR1 أزال هذه الحماية، معيدًا تراكم الحديد والضرر التأكسدي. تضع هذه النتائج SIRT5 وTFR1 في مسار واحد يحدد مدى تعرض خلايا الكلية للإصابة المدفوعة بالحديد في ظروف السكري.
ماذا قد يعني هذا للعلاجات المستقبلية
بشكل عام، تُظهر الدراسة أن QODG يمكن أن يخفف تلف الكلى السكري في الخلايا والفئران عن طريق رفع SIRT5، الذي يزيل بعد ذلك علامة كيميائية من TFR1، مما يزعزع استقرار بوابة دخول الحديد هذه ويقلل الفيروبتوزيس. للفهم العام: الفكرة الرئيسية هي أن مركبًا نباتيًا يبدو أنه يساعد خلايا مرشحات الكلية عبر إغلاق "باب الحديد" الذي يغذي شكلًا مدمرًا من موت الخلايا. بينما هناك حاجة لمزيد من العمل في دراسات حيوانية أوسع وفي نهاية المطاف تجارب بشرية، تبرز هذه النتائج استراتيجية واعدة: استهداف تعامل الحديد والموت الخلوي التأكسدي بجزيئات طبيعية لإبطاء أو منع مرض الكلية السكري.
الاستشهاد: Wu, M., Ye, W. & Ye, X. Quercetin-4’-O-β-D-glucopyranoside inhibits ferroptosis though SIRT5-mediated desuccinylation of TFR1 in diabetic nephropathy. Sci Rep 16, 12384 (2026). https://doi.org/10.1038/s41598-026-41148-4
الكلمات المفتاحية: اعتلال الكلية السكري, حماية الكلى, الفيروبتوزيس, الفلافونويدات, تمثّل الحديد