Clear Sky Science · nl
Quercetine-4’-O-β-D-glucopyranoside remt ferroptose via SIRT5-gemedieerde desuccinylatie van TFR1 bij diabetische nefropathie
Waarom dit belangrijk is voor mensen met diabetes
Nieraandoeningen behoren tot de ernstigste langetermijncomplicaties van diabetes en zijn een belangrijke reden waarom mensen dialyse of transplantaties nodig hebben. Deze studie onderzoekt een van planten afgeleid natuurlijk verbinding, quercetine-4'-O-β-D-glucopyranoside (QODG), en hoe deze de nieren zou kunnen beschermen tegen diabetesgerelateerde schade door een specifiek type celdood te blokkeren dat wordt aangedreven door ijzer en oxidatieve stress. Inzicht in dit proces kan de deur openen naar nieuwe, veiligere behandelingen die standaardmaatregelen voor bloedsuiker- en bloeddrukcontrole aanvullen.
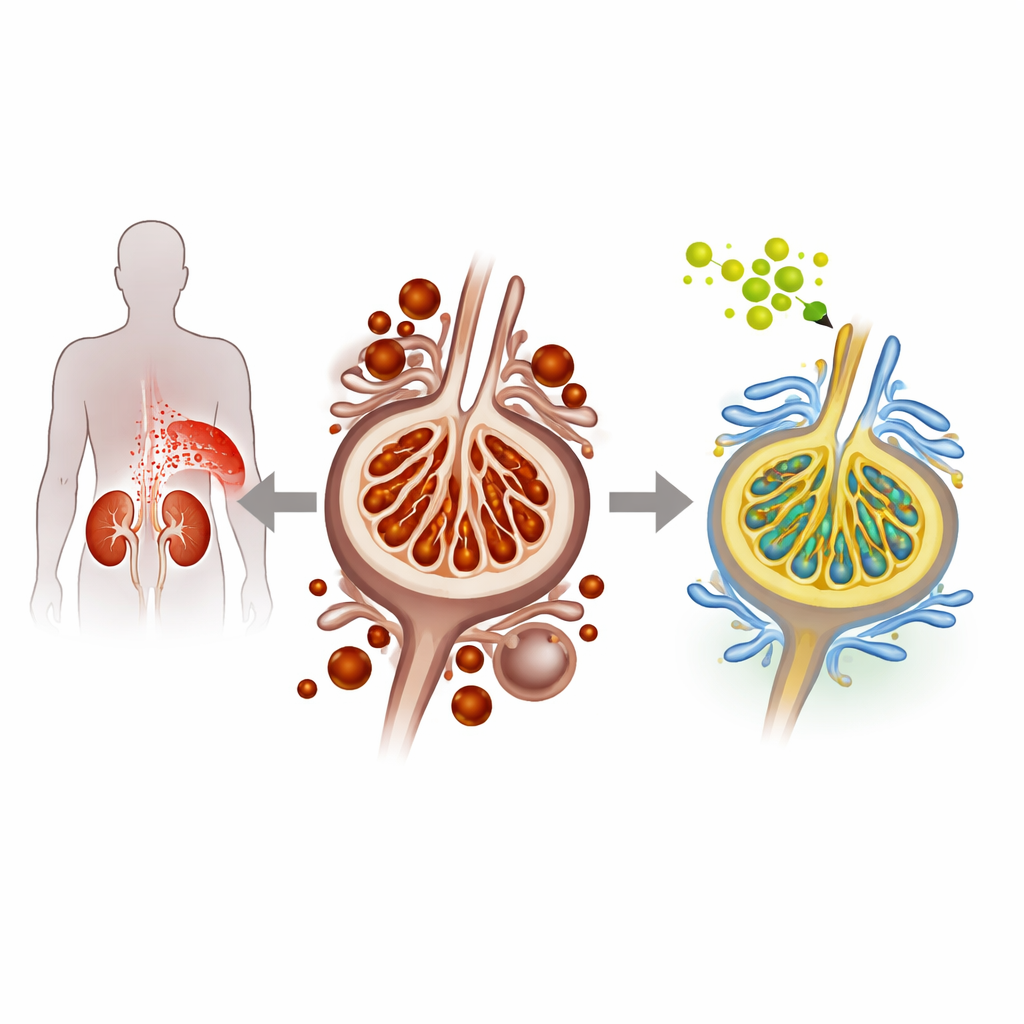
Wanneer suiker de filtercellen van de nier beschadigt
Bij diabetische nefropathie beschadigt hoge bloedsuikerspiegel geleidelijk podocyten, de fragiele cellen die de filtratie-eenheden van de nier bekleden en voorkomen dat eiwitten in de urine terechtkomen. De onderzoekers gebruikten zowel gekweekte muis-podocyten als een diabetisch muismodel om deze toestand na te bootsen. Onder hoge-glucoseomstandigheden vertoonden de podocyten kenmerken van een specifiek type celdood genaamd ferroptose, dat wordt gevoed door overtollig ijzer en de ophoping van beschadigde, geoxideerde vetten in celmembranen. Het team observeerde meer ijzer in de cellen, grotere lipidenperoxidatie en verminderde niveaus van natuurlijke beschermende eiwitten, wat allemaal wijst op verhoogde ferroptose en verslechterde nierstress.
Een plantaire molecule die ijzergedreven schade bedwingt
QODG is een flavonoïde glycoside verwant aan quercetine, een verbinding die voorkomt in veel vruchten en medicinale planten. Wanneer de onderzoekers hoge-glucose podocyten behandelden met QODG, verbeterde de overleving van cellen duidelijk en dosisafhankelijk. Merkers van oxidatieve schade, zoals lipidenperoxidatie en malondialdehyde, daalden, terwijl antioxidatieve verdedigingen zoals superoxide dismutase en catalase stegen. Tegelijkertijd namen de eiwitniveaus van GPX4 en SLC7A11, twee belangrijke beschermers tegen ferroptose, toe en daalden de niveaus van transferrinereceptor 1 (TFR1), een belangrijk poortje voor ijzeropname aan het celoppervlak. In diabetische muizen verminderde QODG-behandeling structurele nierschade, verlaagde bloed- en urinemarkers voor nierfunctiestoornis en herstelde het evenwicht tussen schadelijke oxidatieve krachten en beschermende antioxidatieve systemen.
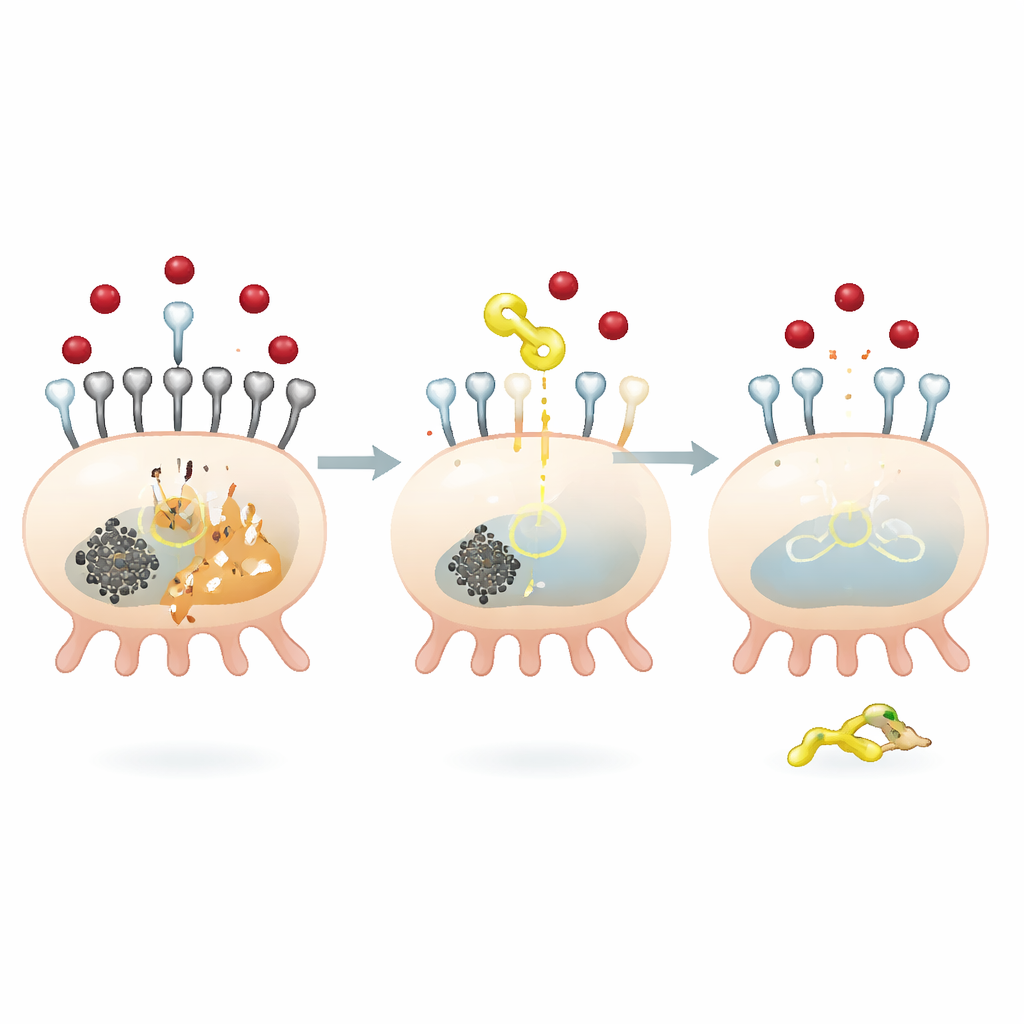
Een moleculaire rem op ijzerinvoer in niercellen
Om te begrijpen hoe QODG deze beschermende effecten uitoefent, richtte het team zich op een eiwit genaamd SIRT5, een enzym dat een klein chemisch label, bekend als een succinylgroep, van andere eiwitten verwijdert. Hoge glucose verhoogde de globale succinylatie in podocyten en verlaagde SIRT5-niveaus. QODG keerde dit om: het verhoogde SIRT5 terwijl het de totale succinylatie weer naar beneden bracht, zonder de beschikbaarheid van het succinyl-donor molecuul te veranderen. De onderzoekers ontdekten dat SIRT5 specifiek de succinylatie van TFR1 op één locatie regelt, een aminozuurpositie genaamd lysine 626. Wanneer SIRT5 werd uitgeschakeld, werd TFR1 zwaarder gesuccinyleerd, stabieler en overvloediger, wat leidde tot verhoogde ijzeropname en sterkere ferroptosesignalen. Omgekeerd verminderde het herstellen van SIRT5 de stabiliteit en expressie van TFR1, waardoor de ijzerstroom en celdood werden afgeremd.
Het verband tussen de regulator en de ijzerpoort aantonen
Het team gebruikte meerdere complementaire technieken om te bevestigen dat SIRT5 fysiek bindt aan TFR1 en diens modificatiestatus aanpast. Het muteren van verschillende potentiële succinylatieplaatsen op TFR1 toonde aan dat alleen veranderingen op lysine 626 zowel succinylatie als totale TFR1-eiwitniveaus beïnvloedden, waarmee dit als het kritische controlepunt werd geïdentificeerd. Biochemische pull-down experimenten en een nabijheidsgebaseerde beeldvormingstest bevestigden de directe interactie tussen SIRT5 en TFR1. Functioneel maakte overexpressie van SIRT5 alleen podocyten resistenter tegen ferroptose, maar het geforceerd verhogen van TFR1-niveaus tilde deze bescherming op en herstelde ijzeraccumulatie en oxidatieve schade. Deze bevindingen plaatsen SIRT5 en TFR1 in één pad dat bepaalt hoe kwetsbaar niercellen zijn voor ijzergedreven schade onder diabetische omstandigheden.
Wat dit kan betekenen voor toekomstige behandelingen
Samengevat laat de studie zien dat QODG de diabetische nierschade in cellen en muizen kan verlichten door SIRT5 te verhogen, dat vervolgens een chemisch label van TFR1 verwijdert, deze ijzerimportpoort destabiliseert en ferroptose dempt. Voor een geïnteresseerde lezer is het kernidee dat een plantaardige verbinding de filtercellen van de nier lijkt te helpen door de "ijzerd deur" te sluiten die een destructieve vorm van celdood voedt. Hoewel er meer werk nodig is in grotere dierstudies en uiteindelijk in mensen, benadrukken deze resultaten een veelbelovende strategie: het richten op ijzerhantering en oxidatieve celdood met natuurlijke moleculen om diabetische nierziekte te vertragen of te voorkomen.
Bronvermelding: Wu, M., Ye, W. & Ye, X. Quercetin-4’-O-β-D-glucopyranoside inhibits ferroptosis though SIRT5-mediated desuccinylation of TFR1 in diabetic nephropathy. Sci Rep 16, 12384 (2026). https://doi.org/10.1038/s41598-026-41148-4
Trefwoorden: diabetische nefropathie, nierbescherming, ferroptose, flavonoïden, ijzermetabolisme