Clear Sky Science · it
Quercetina-4’-O-β-D-glucopiranoside inibisce la ferroptosi tramite la desuccinilazione mediata da SIRT5 di TFR1 nella nefropatia diabetica
Perché è importante per le persone con diabete
La malattia renale è una delle complicanze croniche più gravi del diabete ed è una delle principali ragioni per cui le persone necessitano di dialisi o trapianto. Questo studio esplora un composto naturale di origine vegetale, la quercetina-4’-O-β-D-glucopiranoside (QODG), e come potrebbe proteggere i reni dai danni correlati al diabete bloccando una specifica forma di morte cellulare guidata dal ferro e dallo stress ossidativo. Comprendere questo meccanismo potrebbe aprire la strada a nuovi trattamenti più sicuri che completino il controllo standard della glicemia e della pressione arteriosa.
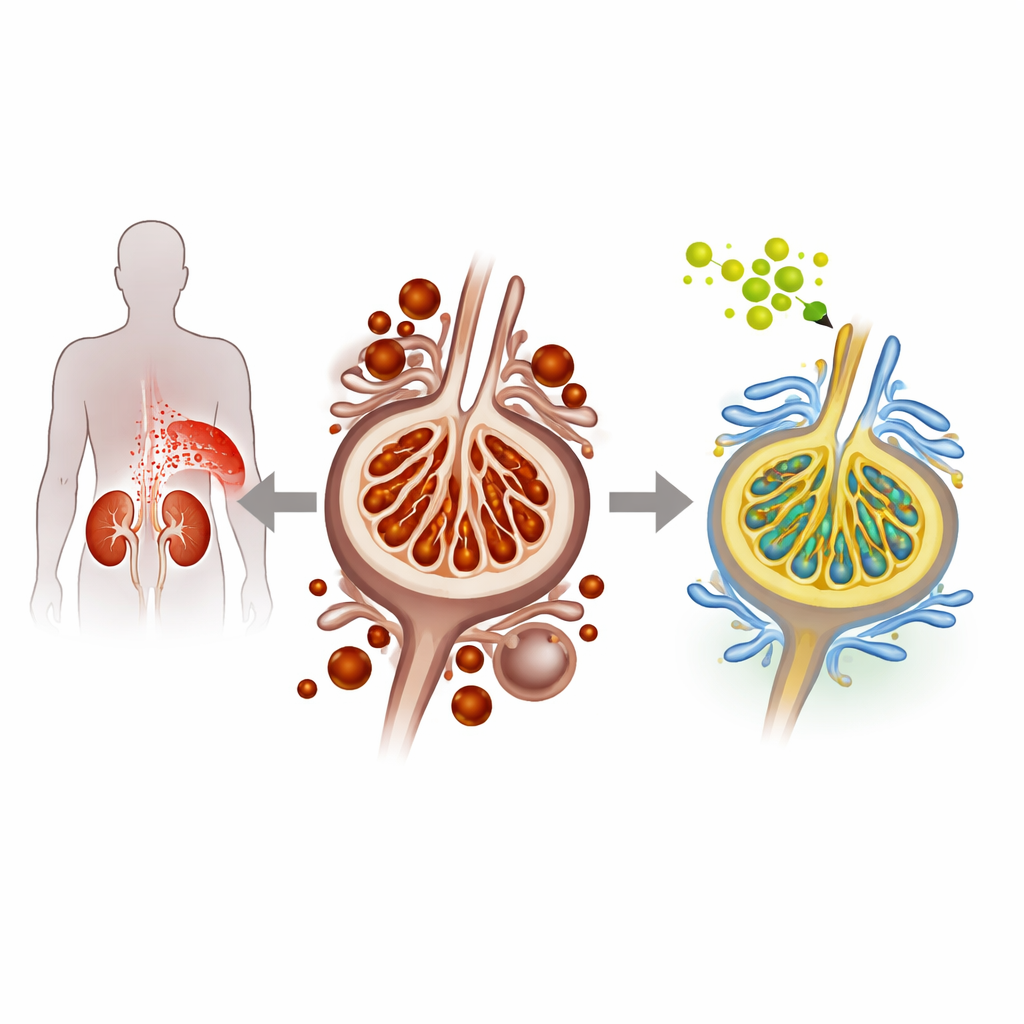
Quando lo zucchero danneggia le cellule filtranti del rene
Nella nefropatia diabetica, l’iperglicemia danneggia progressivamente i podociti, le cellule delicate che rivestono le unità filtranti del rene e impediscono la perdita di proteine nelle urine. I ricercatori hanno usato sia podociti murini coltivati sia un modello murino diabetico per riprodurre questa condizione. In condizioni di alto glucosio, i podociti hanno mostrato segnali di una forma particolare di morte cellulare chiamata ferroptosi, alimentata dall’eccesso di ferro e dall’accumulo di lipidi ossidati danneggiati nelle membrane cellulari. Il gruppo ha osservato un aumento del ferro intracellulare, una maggiore perossidazione lipidica e livelli ridotti di proteine protettive naturali, indicazioni di ferroptosi accentuata e peggioramento dello stress renale.
Una molecola vegetale che attenua il danno indotto dal ferro
QODG è un glicoside flavonoide correlato alla quercetina, un composto presente in molti frutti e piante medicinali. Quando i ricercatori hanno trattato i podociti in alto glucosio con QODG, la sopravvivenza cellulare è migliorata in modo chiaro e dose-dipendente. I marcatori di danno ossidativo, come la perossidazione lipidica e il malondialdeide, sono diminuiti, mentre le difese antiossidanti quali la superossido dismutasi e la catalasi sono aumentate. Allo stesso tempo, i livelli proteici di GPX4 e SLC7A11, due guardiani chiave contro la ferroptosi, sono aumentati, mentre i livelli del recettore della transferrina 1 (TFR1), una principale porta d’ingresso del ferro sulla superficie cellulare, sono diminuiti. Nei topi diabetici, il trattamento con QODG ha ridotto il danno strutturale renale, abbassato i marker ematici e urinari di disfunzione renale e ristabilito un equilibrio più sano tra forze ossidative dannose e sistemi antiossidanti protettivi.
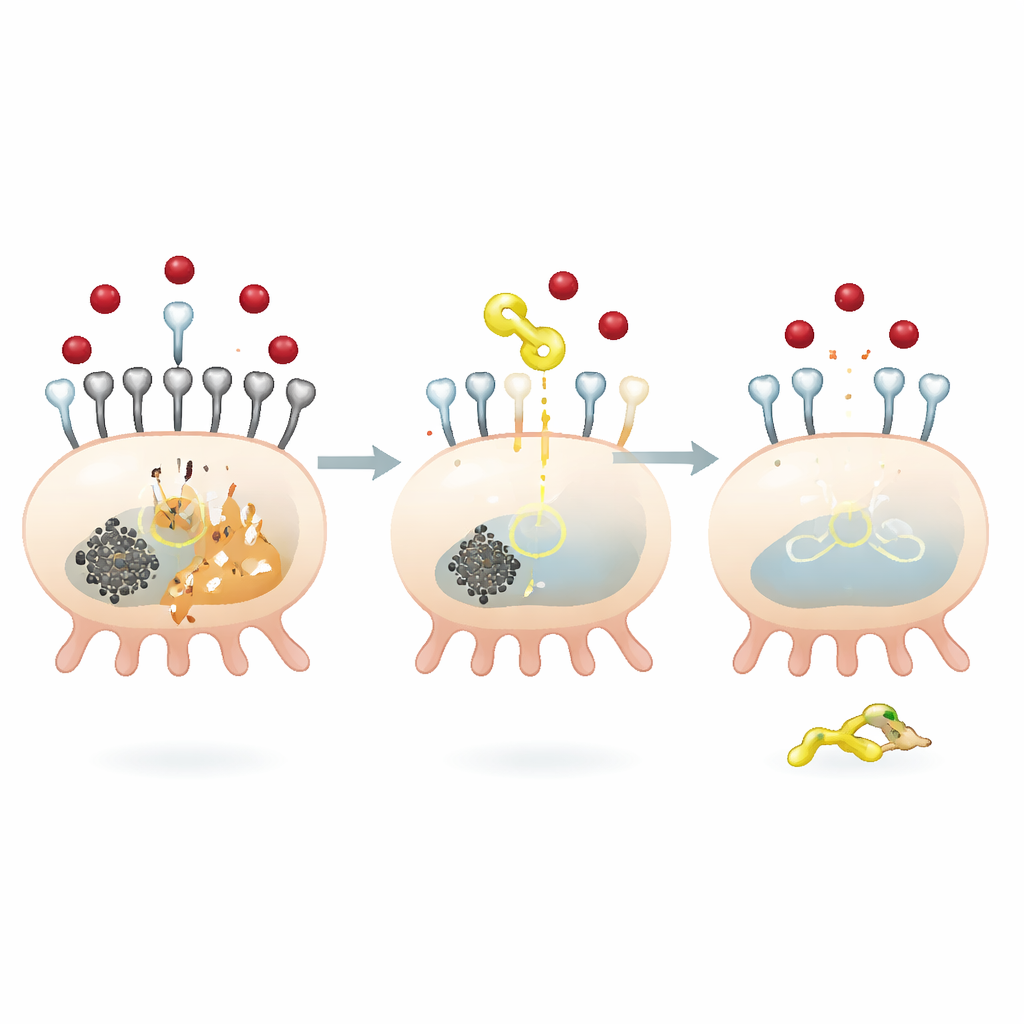
Un freno molecolare all’ingresso del ferro nelle cellule renali
Per capire come QODG eserciti questi effetti protettivi, il gruppo si è concentrato su una proteina chiamata SIRT5, un enzima che rimuove un piccolo gruppo chimico noto come succinile da altre proteine. L’alto glucosio aumentava la succinilazione globale nei podociti e riduceva i livelli di SIRT5. QODG ha invertito questo quadro: ha aumentato SIRT5 riportando la succinilazione complessiva a livelli più bassi, senza alterare la disponibilità del donatore di succinile. I ricercatori hanno scoperto che SIRT5 controlla specificamente la succinilazione di TFR1 in un sito, una posizione amminoacidica chiamata lisina 626. Quando SIRT5 veniva silenziata, TFR1 risultava più succinilata, più stabile e più abbondante, portando a un aumento dell’assorbimento di ferro e a segnali di ferroptosi più intensi. Al contrario, ripristinare SIRT5 riduceva la stabilità e l’espressione di TFR1, limitando l’ingresso di ferro e la morte cellulare.
Dimostrare il legame tra il regolatore e la porta del ferro
Il team ha utilizzato diverse tecniche complementari per confermare che SIRT5 si lega fisicamente a TFR1 e ne regola lo stato di modificazione. La mutazione dei diversi potenziali siti di succinilazione su TFR1 ha mostrato che solo le variazioni alla lisina 626 modificavano sia la succinilazione sia i livelli totali della proteina TFR1, identificando questo come il punto di controllo critico. Esperimenti biochimici di pull-down e un saggio di imaging basato sulla prossimità hanno confermato l’interazione diretta tra SIRT5 e TFR1. Funzionalmente, la sovraespressione di SIRT5 da sola rendeva i podociti più resistenti alla ferroptosi, ma il ripristino forzato dei livelli di TFR1 annullava questa protezione, ripristinando l’accumulo di ferro e il danno ossidativo. Questi risultati collocano SIRT5 e TFR1 in un’unica via che determina quanto le cellule renali siano vulnerabili al danno indotto dal ferro nelle condizioni diabetiche.
Cosa potrebbe significare per i trattamenti futuri
Nel complesso, lo studio mostra che QODG può attenuare il danno renale diabetico in cellule e topi aumentando SIRT5, che poi rimuove un tag chimico da TFR1, destabilizzando questa porta d’ingresso del ferro e riducendo la ferroptosi. Per il lettore non specialistico, l’idea chiave è che un composto di origine vegetale sembra aiutare le cellule filtranti del rene chiudendo la “porta del ferro” che alimenta una forma distruttiva di morte cellulare. Pur richiedendo ulteriori studi su animali più grandi e, in futuro, sull’uomo, questi risultati evidenziano una strategia promettente: mirare alla gestione del ferro e alla morte cellulare ossidativa con molecole naturali per rallentare o prevenire la malattia renale diabetica.
Citazione: Wu, M., Ye, W. & Ye, X. Quercetin-4’-O-β-D-glucopyranoside inhibits ferroptosis though SIRT5-mediated desuccinylation of TFR1 in diabetic nephropathy. Sci Rep 16, 12384 (2026). https://doi.org/10.1038/s41598-026-41148-4
Parole chiave: nefropatia diabetica, protezione renale, ferroptosi, flavonoidi, metabolismo del ferro