Clear Sky Science · fr
La quercétine-4’-O-β-D-glucopyranoside inhibe la ferroptose via la déssuccinylation de la TFR1 médiée par SIRT5 dans la néphropathie diabétique
Pourquoi cela compte pour les personnes atteintes de diabète
La maladie rénale est l’une des complications chroniques les plus graves du diabète et une des principales raisons pour lesquelles les patients ont besoin d’hémodialyse ou de greffes. Cette étude examine un composé d’origine végétale, la quercétine-4’-O-β-D-glucopyranoside (QODG), et la manière dont il pourrait protéger les reins des atteintes liées au diabète en bloquant une forme spécifique de mort cellulaire alimentée par le fer et le stress oxydatif. Comprendre ce mécanisme pourrait ouvrir la voie à des traitements nouveaux et potentiellement plus sûrs, qui viendraient compléter le contrôle classique de la glycémie et de la pression artérielle.
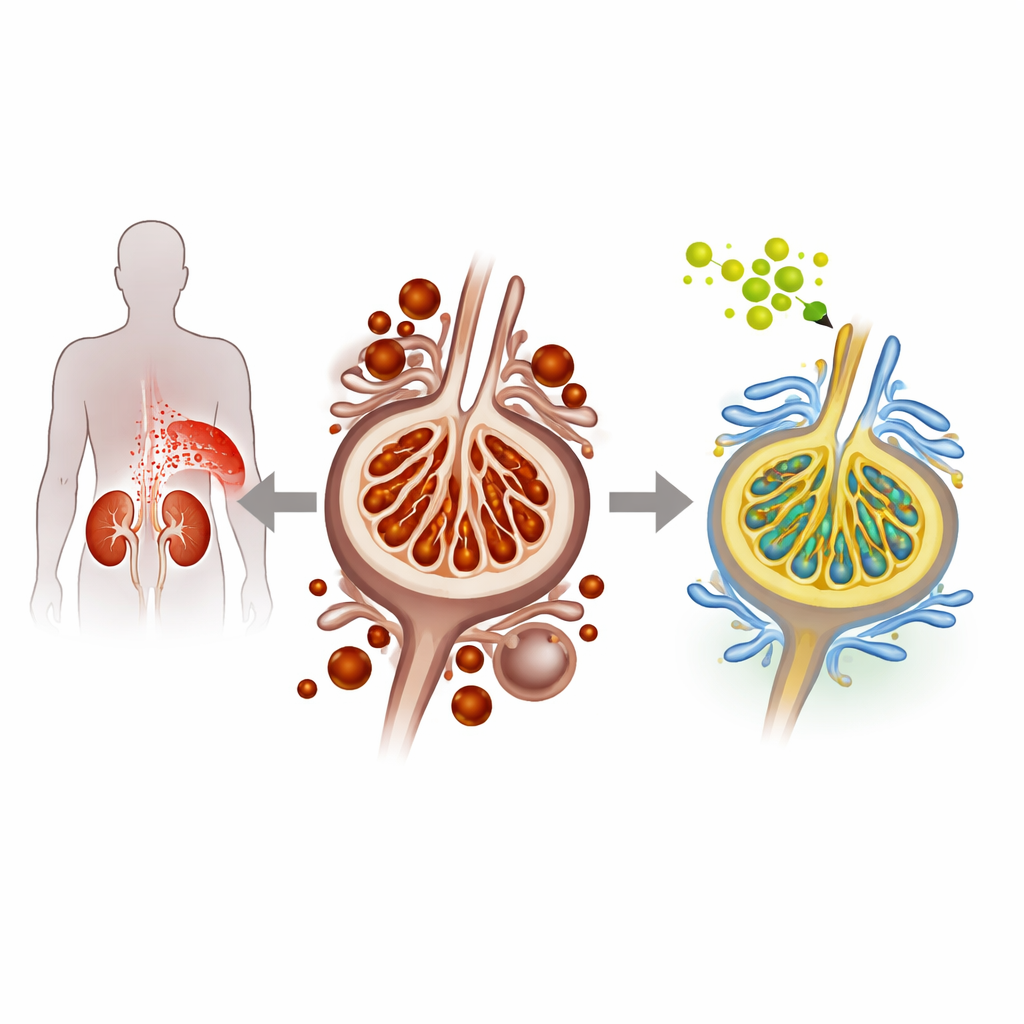
Quand le sucre abîme les cellules filtres du rein
Dans la néphropathie diabétique, l’hyperglycémie endommage progressivement les podocytes, ces cellules fragiles qui tapissent les unités de filtration du rein et empêchent les protéines de fuir dans l’urine. Les chercheurs ont utilisé des podocytes de souris en culture et un modèle murin diabétique pour reproduire cette situation. En conditions de forte concentration en glucose, les podocytes présentaient des signes d’un type particulier de mort cellulaire appelé ferroptose, alimentée par un excès de fer et l’accumulation de lipides oxydés endommagés dans les membranes cellulaires. L’équipe a observé davantage de fer intracellulaire, une augmentation de la peroxydation lipidique et une diminution des protéines protectrices naturelles, autant d’indices d’une ferroptose accrue et d’un stress rénal aggravé.
Une molécule végétale qui calme les dégâts induits par le fer
La QODG est un glycoside flavonoïde apparenté à la quercétine, un composé présent dans de nombreux fruits et plantes médicinales. Lorsque les chercheurs ont traité des podocytes exposés à un fort taux de glucose avec la QODG, la survie cellulaire s’est améliorée de manière nette et dépendante de la dose. Les marqueurs des dommages oxydatifs, tels que la peroxydation lipidique et le malondialdéhyde, ont diminué, tandis que les défenses antioxydantes comme la superoxyde dismutase et la catalase ont augmenté. Simultanément, les niveaux protéiques de GPX4 et SLC7A11, deux gardiens clés contre la ferroptose, ont augmenté, et les niveaux du récepteur de la transferrine 1 (TFR1), principale porte d’entrée du fer à la surface cellulaire, ont diminué. Chez les souris diabétiques, le traitement par QODG a réduit les lésions structurelles rénales, abaissé les marqueurs sanguins et urinaires de dysfonction rénale et rétabli un équilibre plus sain entre forces oxydantes délétères et systèmes antioxydants protecteurs.
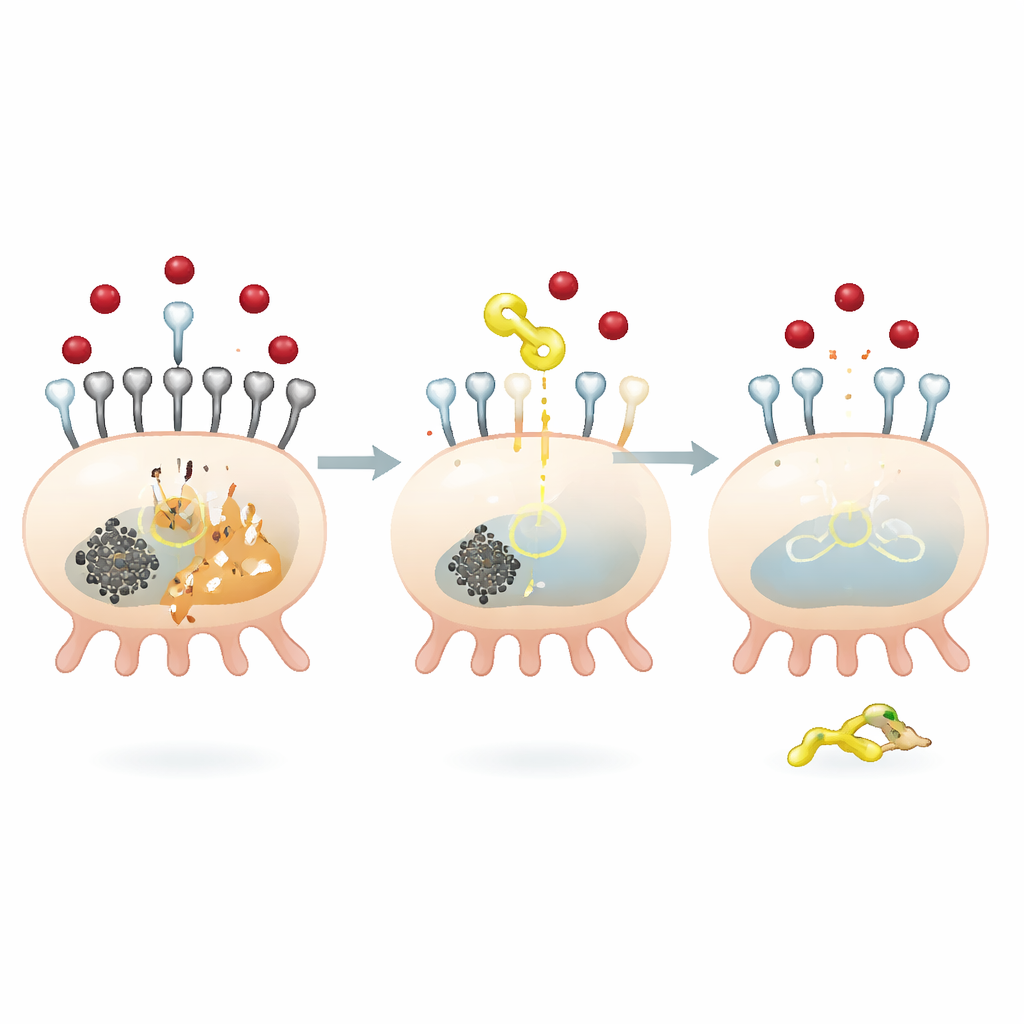
Un frein moléculaire à l’entrée du fer dans les cellules rénales
Pour comprendre comment la QODG exerce ces effets protecteurs, l’équipe s’est concentrée sur une protéine appelée SIRT5, une enzyme qui retire une petite marque chimique, le groupe succinyl, d’autres protéines. Une forte glycémie augmentait la succinylation globale au sein des podocytes et réduisait les niveaux de SIRT5. La QODG a inversé ces effets : elle a augmenté SIRT5 tout en ramenant la succinylation globale à la baisse, sans modifier la disponibilité du donneur de succinyl. Les chercheurs ont montré que SIRT5 contrôle spécifiquement la succinylation de la TFR1 en un site unique, un résidu aminé appelé lysine 626. Lorsque SIRT5 était réduit, la TFR1 devenait davantage succinylée, plus stable et plus abondante, entraînant une augmentation de l’entrée de fer et des signaux de ferroptose renforcés. À l’inverse, restaurer SIRT5 diminuait la stabilité et l’expression de la TFR1, freinant l’afflux de fer et la mort cellulaire.
Prouver le lien entre le régulateur et la porte d’entrée du fer
L’équipe a utilisé plusieurs techniques complémentaires pour confirmer que SIRT5 se lie physiquement à la TFR1 et modifie son état de modification. La mutation de différents sites potentiels de succinylation sur la TFR1 a montré que seules les modifications de la lysine 626 altéraient à la fois la succinylation et le niveau total de protéine TFR1, désignant ce site comme le point de contrôle critique. Des expériences biochimiques d’affinité et un test d’imagerie de proximité ont confirmé l’interaction directe entre SIRT5 et TFR1. Sur le plan fonctionnel, la surexpression de SIRT5 seule rendait les podocytes plus résistants à la ferroptose, mais la réintroduction forcée de niveaux élevés de TFR1 annulait cette protection, restaurant l’accumulation de fer et les dommages oxydatifs. Ces résultats placent SIRT5 et TFR1 dans une même voie qui détermine la vulnérabilité des cellules rénales aux lésions induites par le fer en contexte diabétique.
Ce que cela pourrait signifier pour les traitements futurs
Au total, l’étude montre que la QODG peut atténuer les lésions rénales diabétiques in vitro et chez la souris en augmentant SIRT5, qui ensuite enlève une marque chimique sur la TFR1, déstabilisant cette porte d’entrée du fer et réduisant la ferroptose. Pour un lecteur non spécialiste, l’idée clé est qu’un composé d’origine végétale semble aider les cellules filtres du rein en « fermant la porte du fer » qui alimente une forme destructrice de mort cellulaire. Bien que des travaux supplémentaires soient nécessaires dans des modèles animaux plus larges puis chez l’humain, ces résultats mettent en lumière une stratégie prometteuse : cibler la gestion du fer et la mort cellulaire oxydative avec des molécules naturelles pour ralentir ou prévenir la néphropathie diabétique.
Citation: Wu, M., Ye, W. & Ye, X. Quercetin-4’-O-β-D-glucopyranoside inhibits ferroptosis though SIRT5-mediated desuccinylation of TFR1 in diabetic nephropathy. Sci Rep 16, 12384 (2026). https://doi.org/10.1038/s41598-026-41148-4
Mots-clés: néphropathie diabétique, protection rénale, ferroptose, flavonoïdes, métabolisme du fer