Clear Sky Science · pt
Quercetina-4’-O-β-D-glucopiranosídeo inibe a ferroptose por meio da dessuccinilação mediada por SIRT5 de TFR1 na nefropatia diabética
Por que isso importa para pessoas com diabetes
A doença renal é uma das complicações crônicas mais graves do diabetes e uma das principais razões pelas quais pessoas precisam de diálise ou transplante. Este estudo investiga um composto natural derivado de plantas, a quercetina-4'-O-β-D-glucopiranosídeo (QODG), e como ele pode proteger os rins dos danos relacionados ao diabetes ao bloquear uma forma específica de morte celular impulsionada por ferro e estresse oxidativo. Compreender esse processo pode abrir caminho para tratamentos novos e mais seguros que complementem o controle padrão da glicemia e da pressão arterial.
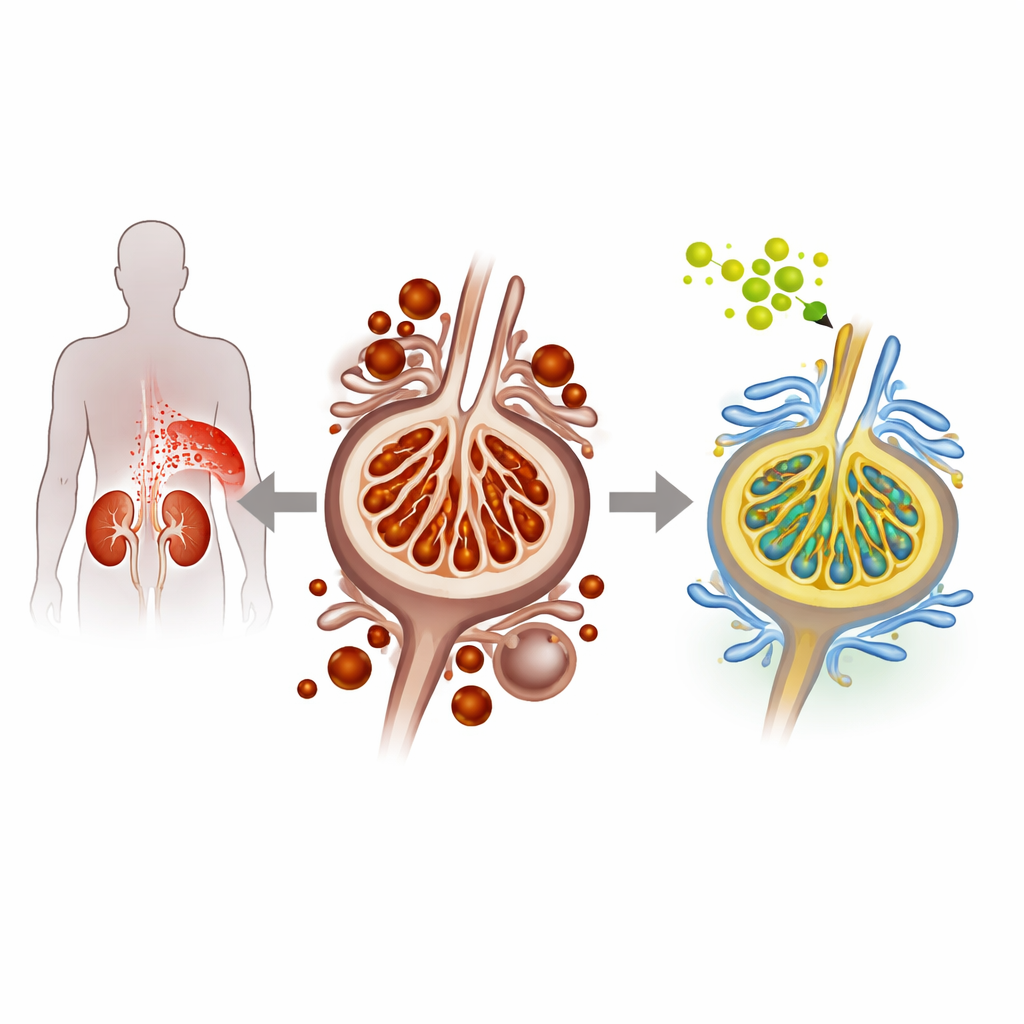
Quando o açúcar danifica as células filtrantes do rim
Na nefropatia diabética, a hiperglicemia lesiona gradualmente os podócitos, as células delicadas que revestem as unidades de filtração do rim e impedem o vazamento de proteínas na urina. Os pesquisadores usaram tanto podócitos de camundongo em cultura quanto um modelo de camundongo diabético para reproduzir essa condição. Sob condições de alto teor de glicose, os podócitos exibiram sinais de um tipo particular de morte celular chamado ferroptose, que é alimentado pelo excesso de ferro e pelo acúmulo de lipídios oxidados danificados nas membranas celulares. A equipe observou mais ferro dentro das células, maior peroxidação lipídica e níveis reduzidos de proteínas protetoras naturais, todos indicando aumento da ferroptose e agravamento do estresse renal.
Uma molécula vegetal que acalma o dano impulsionado pelo ferro
QODG é um glicosídeo flavonoide relacionado à quercetina, um composto encontrado em muitas frutas e plantas medicinais. Quando os pesquisadores trataram podócitos expostos a alta glicose com QODG, a sobrevivência celular melhorou de forma claramente dependente da dose. Marcadores de dano oxidativo, como peroxidação lipídica e malondialdeído, diminuíram, enquanto defesas antioxidantes como superóxido dismutase e catalase aumentaram. Ao mesmo tempo, os níveis das proteínas GPX4 e SLC7A11, dois guardiões fundamentais contra a ferroptose, aumentaram, e os níveis do receptor de transferrina 1 (TFR1), uma importante porta de entrada de ferro na superfície celular, caíram. Em camundongos diabéticos, o tratamento com QODG reduziu a lesão estrutural renal, baixou marcadores sanguíneos e urinários de disfunção renal e restaurou um equilíbrio mais saudável entre forças oxidativas danosas e sistemas antioxidantes protetores.
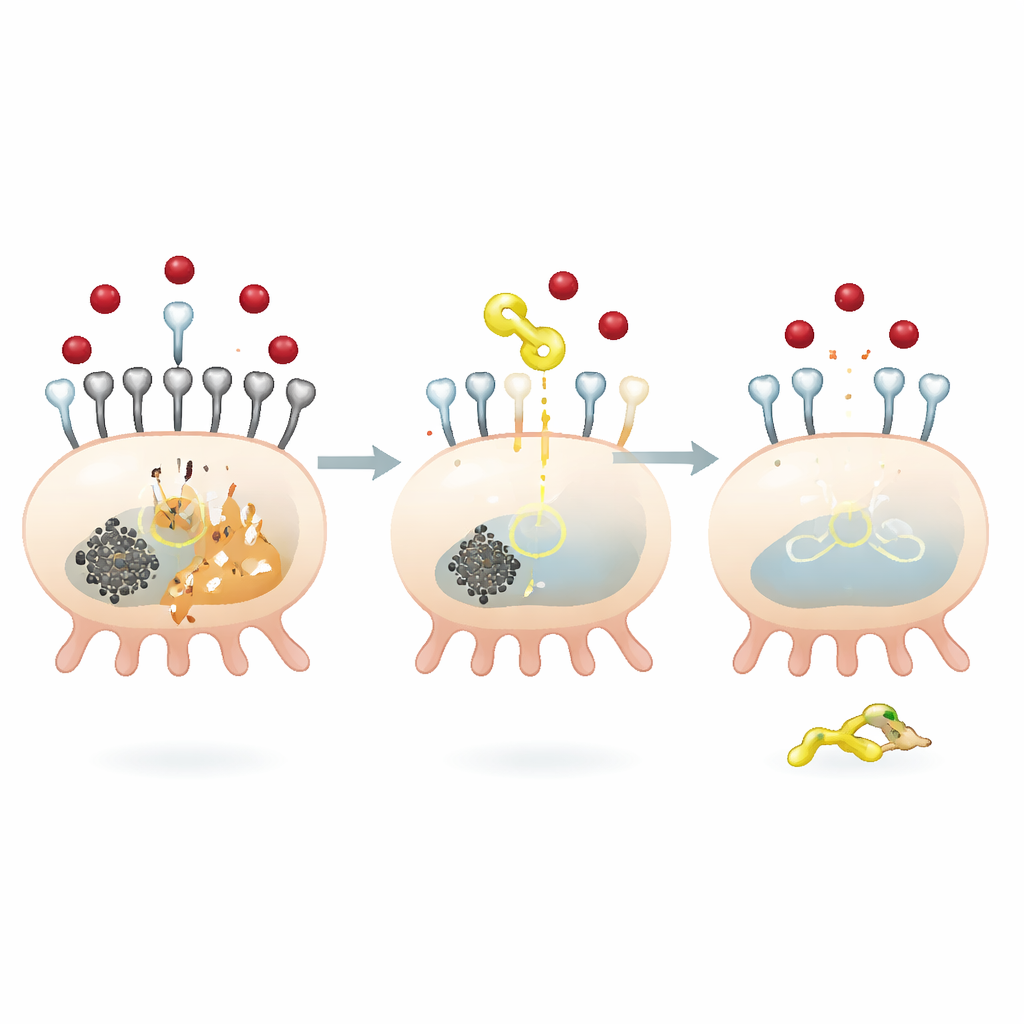
Um freio molecular na entrada de ferro nas células renais
Para entender como o QODG exerce esses efeitos protetores, a equipe concentrou-se em uma proteína chamada SIRT5, uma enzima que remove um pequeno marcador químico conhecido como grupo succinil de outras proteínas. A glicose alta aumentou a succinilação global dentro dos podócitos e reduziu os níveis de SIRT5. QODG reverteu isso: elevou SIRT5 enquanto reduzia a succinilação geral, sem alterar o suprimento da molécula doadora de succinil. Os pesquisadores descobriram que SIRT5 controla especificamente a succinilação de TFR1 em um sítio, uma posição de aminoácido chamada lisina 626. Quando SIRT5 foi silenciado, TFR1 tornou-se mais succinilado, mais estável e mais abundante, levando ao aumento da captação de ferro e a sinais mais fortes de ferroptose. Por outro lado, restaurar SIRT5 reduziu a estabilidade e a expressão de TFR1, contendo a entrada de ferro e a morte celular.
Comprovando a ligação entre o regulador e a porta de entrada do ferro
A equipe usou várias técnicas complementares para confirmar que SIRT5 se liga fisicamente a TFR1 e ajusta seu estado de modificação. Mutar diferentes sítios potenciais de succinilação em TFR1 mostrou que apenas alterações na lisina 626 modificaram tanto a succinilação quanto os níveis totais de proteína TFR1, identificando esse como o ponto crítico de controle. Experimentos bioquímicos de pull-down e um ensaio de imagem baseado em proximidade confirmaram a interação direta entre SIRT5 e TFR1. Funcionalmente, a superexpressão de SIRT5 por si só tornou os podócitos mais resistentes à ferroptose, mas forçar a restauração dos níveis de TFR1 eliminou essa proteção, restaurando o acúmulo de ferro e o dano oxidativo. Essas descobertas posicionam SIRT5 e TFR1 numa única via que determina quão vulneráveis as células renais são ao dano impulsionado por ferro em condições diabéticas.
O que isso pode significar para tratamentos futuros
Em geral, o estudo mostra que QODG pode aliviar o dano renal diabético em células e em camundongos ao aumentar SIRT5, que então remove um marcador químico de TFR1, desestabilizando esta porta de entrada de ferro e atenuando a ferroptose. Para o leitor leigo, a ideia central é que um composto de origem vegetal parece ajudar as células filtrantes do rim fechando a "porta do ferro" que alimenta uma forma destrutiva de morte celular. Embora sejam necessários mais estudos em animais maiores e, eventualmente, em humanos, esses resultados destacam uma estratégia promissora: direcionar o manejo do ferro e a morte celular oxidativa com moléculas naturais para retardar ou prevenir a doença renal diabética.
Citação: Wu, M., Ye, W. & Ye, X. Quercetin-4’-O-β-D-glucopyranoside inhibits ferroptosis though SIRT5-mediated desuccinylation of TFR1 in diabetic nephropathy. Sci Rep 16, 12384 (2026). https://doi.org/10.1038/s41598-026-41148-4
Palavras-chave: nefropatia diabética, proteção renal, ferroptose, flavonoides, metabolismo do ferro