Clear Sky Science · ru
Кверцетин-4’-O-β-D-глюкопиранозид ингибирует ферроптоз через десукцинилирование TFR1, опосредованное SIRT5, при диабетической нефропатии
Почему это важно для людей с диабетом
Заболевания почек — одно из самых серьёзных отдалённых осложнений диабета и одна из основных причин, по которым людям требуется диализ или пересадка органа. В этом исследовании изучается природное растительное соединение кверцетин-4’-O-β-D-глюкопиранозид (QODG) и то, как оно может защищать почки от поражения, связанного с диабетом, блокируя специфическую форму клеточной гибели, обусловленную железом и окислительным стрессом. Понимание этого механизма может открыть путь к новым, более безопасным терапиям, дополняющим стандартный контроль уровня сахара и артериального давления.
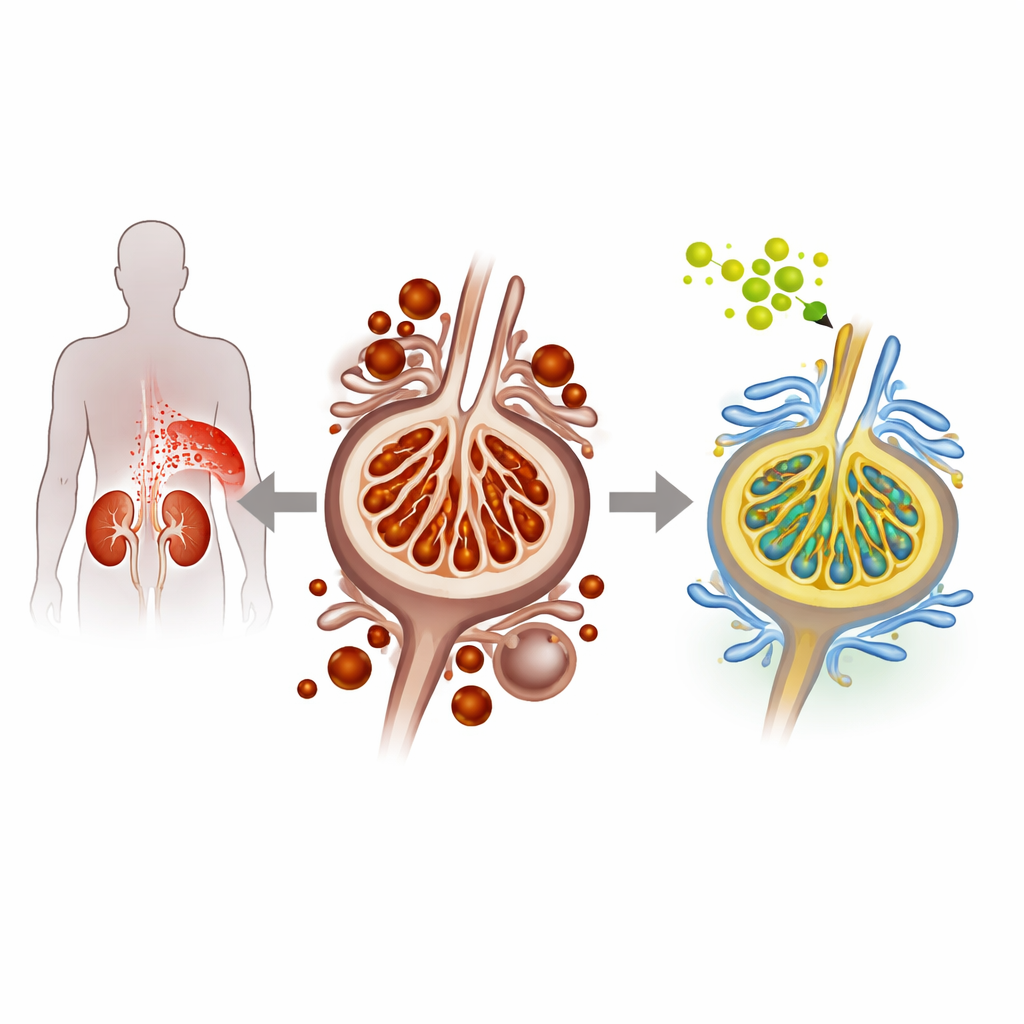
Когда сахар повреждает клетки фильтра почки
При диабетической нефропатии высокий уровень сахара в крови постепенно повреждает подоциты — хрупкие клетки, выстилающие фильтрующие структуры почки и предотвращающие потерю белка с мочой. Исследователи использовали как культивируемые мышиные подоциты, так и модель диабетической мыши, чтобы смоделировать это состояние. При высоком содержании глюкозы подоциты демонстрировали признаки особой формы клеточной смерти — ферроптоза, который подпитывается избытком железа и накоплением повреждённых, окисленных липидов в мембранах. Команда наблюдала увеличение содержания железа в клетках, усиление перекисного окисления липидов и снижение уровней естественных защитных белков — всё это указывает на усиление ферроптоза и прогрессирующий стресс в почке.
Растительная молекула, снижающая ущерб от железа
QODG — это гликозид флавоноида, родственный кверцетину, соединению, встречающемуся во многих фруктах и лекарственных растениях. При обработке подоцитов в условиях высокой глюкозы QODG улучшал выживаемость клеток в явной дозозависимой манере. Маркёры окислительного повреждения, такие как перекисное окисление липидов и малоновый диальдегид, снижались, в то время как антиоксидантные механизмы — супероксид дисмутаза и каталаза — повышались. Одновременно уровни белков GPX4 и SLC7A11, двух ключевых защитников от ферроптоза, увеличивались, а уровни трансферринового рецептора 1 (TFR1), основного входа для железа на поверхности клетки, снижались. У диабетических мышей лечение QODG уменьшало структурные повреждения почек, снижало кровяные и мочевые маркёры дисфункции почек и восстанавливало более здоровый баланс между повреждающими окислительными факторами и защитными антиоксидантными системами.
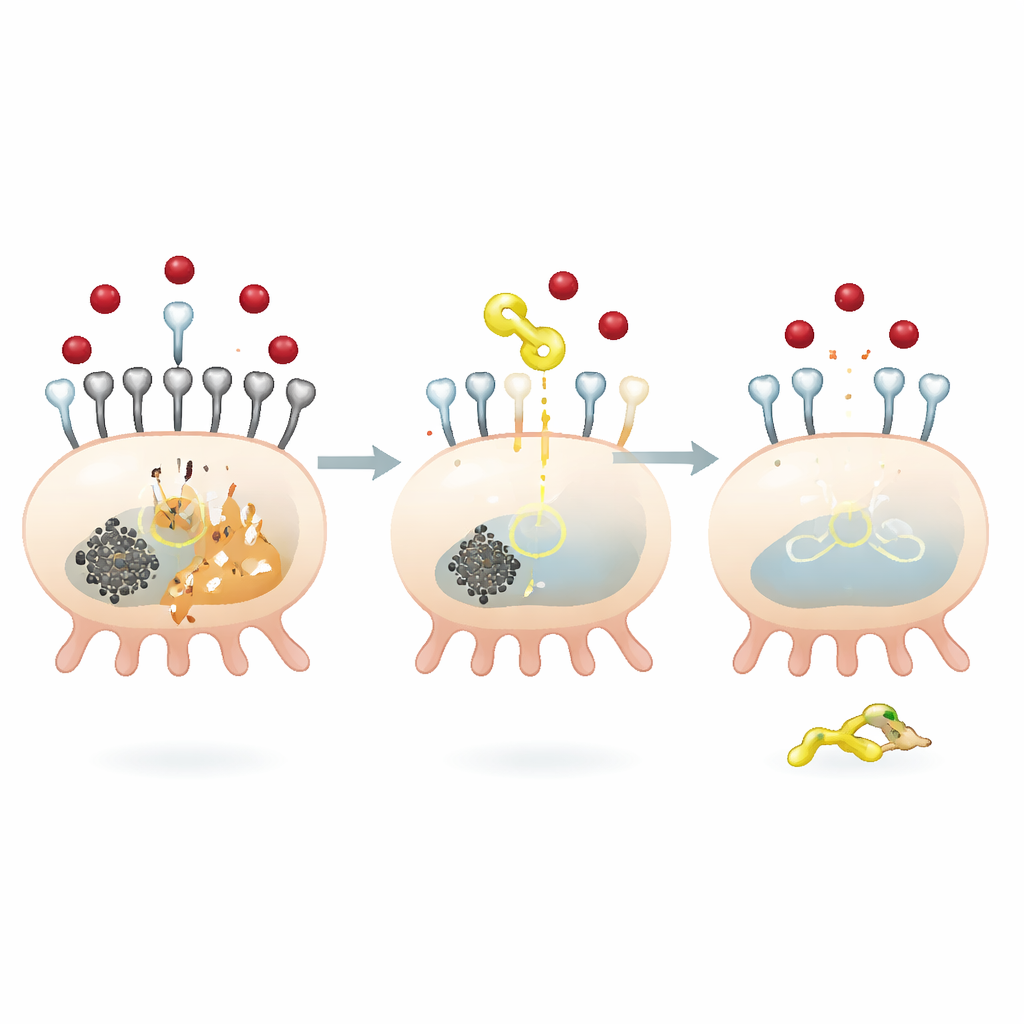
Молекулярный тормоз для поступления железа в клетки почек
Чтобы понять, как QODG оказывает эти защитные эффекты, команда сосредоточилась на белке SIRT5 — ферменте, снимающем маленькую химическую метку, известную как сукцинил-, с других белков. Высокая глюкоза увеличивала глобальную сукцинилирование в подоцитах и снижала уровень SIRT5. QODG обращал это: он повышал SIRT5 и снижал общий уровень сукцинилирования, не изменяя при этом запаса молекулы-донора сукцинила. Исследователи обнаружили, что SIRT5 специфически контролирует сукцинилирование TFR1 в одной позиции — аминокислоте лизин 626. При молчании SIRT5 TFR1 становился более интенсивно сукцинилированным, более стабильным и более многочисленным, что приводило к увеличению поступления железа и усилению сигналов ферроптоза. Наоборот, восстановление SIRT5 уменьшало стабильность и экспрессию TFR1, сдерживая приток железа и гибель клеток.
Доказательства связи между регулятором и «железными воротами»
Команда использовала несколько взаимодополняющих методов, чтобы подтвердить, что SIRT5 физически связывается с TFR1 и регулирует его модификацию. Мутация различных потенциальных сайтов сукцинилирования на TFR1 показала, что только изменения в лизине 626 меняли и уровень сукцинилирования, и общий уровень белка TFR1, указывая на эту позицию как на критическую точку контроля. Биохимические эксперименты по вытягиванию белков и метод визуализации на основе близости подтвердили прямое взаимодействие между SIRT5 и TFR1. Функционально, переэкспрессия SIRT5 сама по себе делала подоциты более устойчивыми к ферроптозу, но принудительное восстановление уровней TFR1 уничтожало эту защиту, возобновляя накопление железа и окислительное повреждение. Эти результаты помещают SIRT5 и TFR1 в одну сигнальную цепочку, определяющую уязвимость клеток почечного фильтра к поражению, вызванному железом, в условиях диабета.
Что это может значить для будущих лечебных подходов
В целом исследование показывает, что QODG может смягчать диабетическое повреждение почек в клеточных и мышиных моделях, повышая уровень SIRT5, который затем снимает химическую метку с TFR1, дестабилизируя этот «ворот» для импорта железа и снижая ферроптоз. Для неспециалиста ключевая идея такова: растительное соединение, по-видимому, помогает клеткам фильтра почки, «закрывая дверь для железа», питающее разрушительную форму клеточной гибели. Хотя необходима дальнейшая работа на крупных животных моделях и в конечном счёте на людях, эти результаты подчёркивают перспективную стратегию: нацеленность на обращение с железом и окислительную клеточную гибель с помощью природных молекул, чтобы замедлить или предотвратить диабетическую болезнь почек.
Цитирование: Wu, M., Ye, W. & Ye, X. Quercetin-4’-O-β-D-glucopyranoside inhibits ferroptosis though SIRT5-mediated desuccinylation of TFR1 in diabetic nephropathy. Sci Rep 16, 12384 (2026). https://doi.org/10.1038/s41598-026-41148-4
Ключевые слова: диабетическая нефропатия, защита почек, ферроптоз, флавоноиды, железный обмен