Clear Sky Science · pl
Quercetyna-4’-O-β-D-glukopiranozyd hamuje ferroptozę poprzez desuccynylację TFR1 zależną od SIRT5 w nefropatii cukrzycowej
Dlaczego to ma znaczenie dla osób z cukrzycą
Choroba nerek jest jednym z najpoważniejszych długoterminowych powikłań cukrzycy i jedną z głównych przyczyn konieczności dializ lub przeszczepów. To badanie analizuje naturalny związek pochodzenia roślinnego, quercetynę-4'-O-β-D-glukopiranozyd (QODG), oraz mechanizm, dzięki któremu może ona chronić nerki przed uszkodzeniami związanymi z cukrzycą poprzez blokowanie konkretnego typu śmierci komórkowej napędzanej żelazem i stresem oksydacyjnym. Zrozumienie tego procesu może otworzyć drogę do nowych, bezpieczniejszych terapii uzupełniających standardowe leczenie kontroli cukru i ciśnienia krwi.
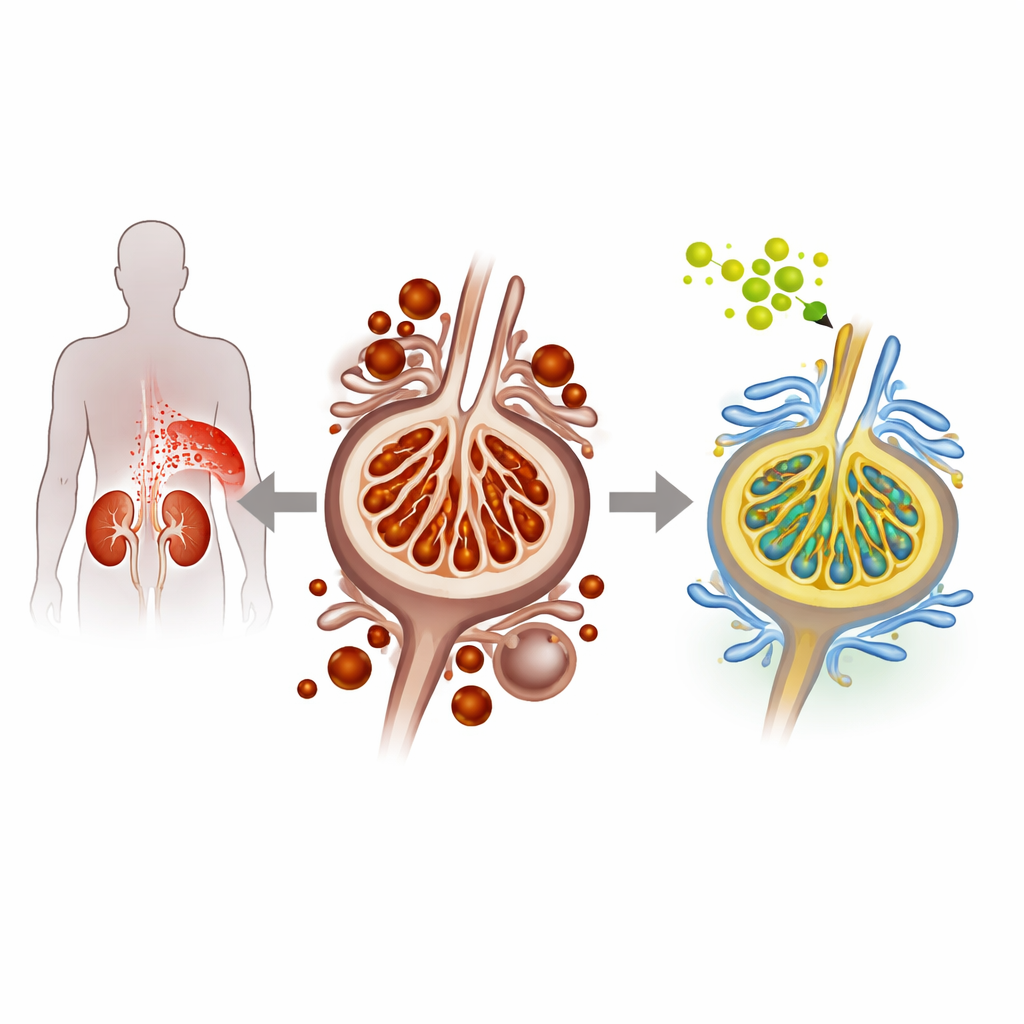
Kiedy cukier uszkadza komórki filtrujące nerki
W nefropatii cukrzycowej wysokie stężenie glukozy stopniowo uszkadza podocyty, delikatne komórki wyściełające jednostki filtrujące nerki i zapobiegające utracie białka z moczem. Naukowcy użyli zarówno hodowanych mysich podocytów, jak i modelu myszy cukrzyczej, aby odtworzyć ten stan. W warunkach wysokoglikemicznych podocyty wykazywały cechy specyficznego typu śmierci komórkowej zwanej ferroptozą, napędzanej nadmiarem żelaza i nagromadzeniem uszkodzonych, zoksydowanych lipidów w błonach komórkowych. Zespół zaobserwował wzrost zawartości żelaza w komórkach, zwiększoną peroksydację lipidów oraz obniżone poziomy naturalnych białek ochronnych — wszystko to wskazuje na nasiloną ferroptozę i pogorszenie stresu nerkowego.
Cząsteczka roślinna łagodząca uszkodzenia wywołane żelazem
QODG to glikozyd flawonoidowy powiązany z quercetyną, związkiem występującym w wielu owocach i roślinach leczniczych. Gdy badacze leczyli podocyty w warunkach wysokiej glukozy QODG, przeżywalność komórek poprawiła się w wyraźnie zależny od dawki sposób. Markery uszkodzeń oksydacyjnych, takie jak peroksydacja lipidów i malondialdehyd, zmalały, podczas gdy obronne enzymy antyoksydacyjne, takie jak dysmutaza ponadtlenkowa i katalaza, wzrosły. Równocześnie poziomy białek GPX4 i SLC7A11 — dwóch kluczowych strażników przeciwko ferroptozie — zwiększyły się, a poziom receptora transferyny 1 (TFR1), głównej bramki importu żelaza na powierzchni komórki, spadł. U myszy z cukrzycą leczenie QODG zmniejszyło strukturalne uszkodzenia nerek, obniżyło markery dysfunkcji nerek we krwi i moczu oraz przywróciło zdrowszą równowagę między siłami oksydacyjnymi a systemami antyoksydacyjnymi.
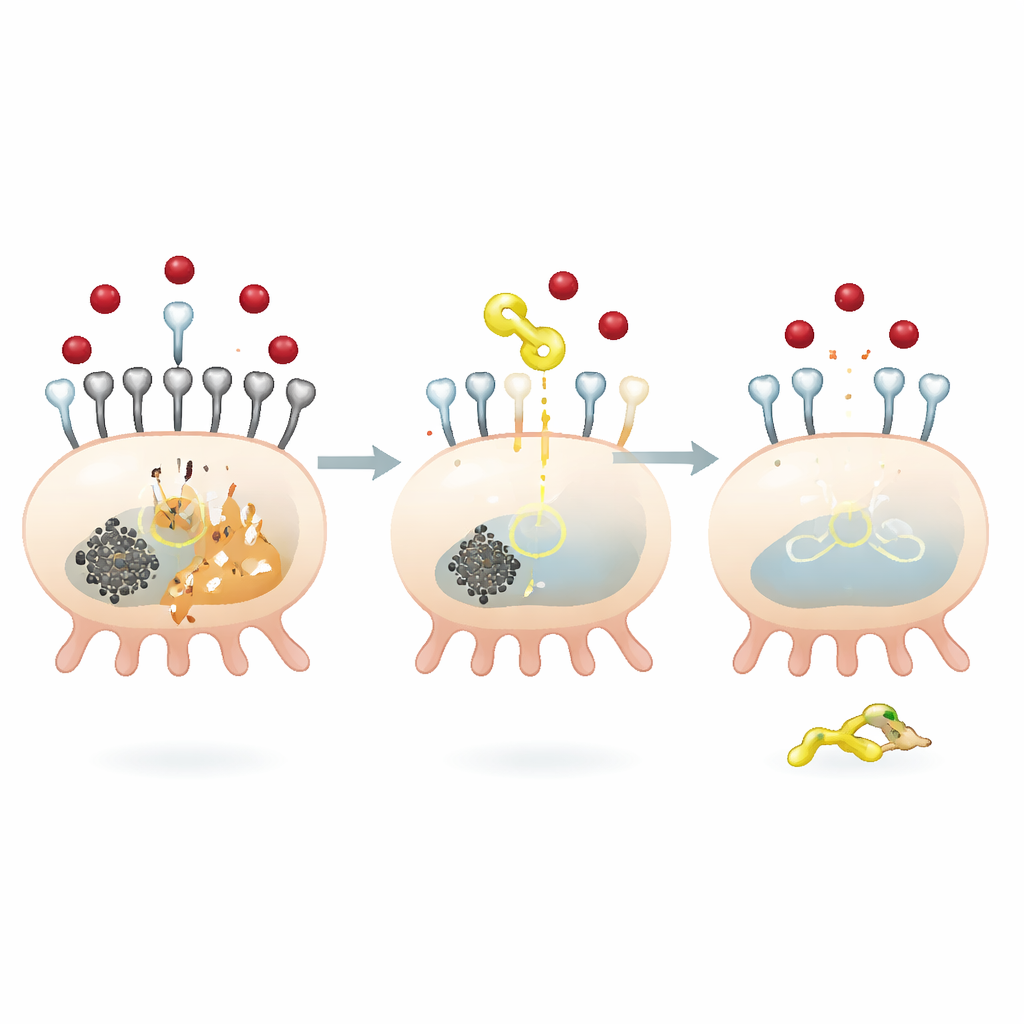
Czynnnik molekularny blokujący wejście żelaza do komórek nerkowych
Aby zrozumieć, jak QODG wywiera te ochronne efekty, zespół skupił się na białku SIRT5 — enzymie usuwającym niewielką grupę chemiczną zwaną grupą sukcynylową z innych białek. Wysoka glukoza zwiększała ogólną sukcyny-lację w podocytach i obniżała poziomy SIRT5. QODG odwracało te zmiany: podnosiło SIRT5 i jednocześnie redukowało ogólną sukcyny-lację, bez zmiany podaży donorów grupy sukcynylowej. Badacze stwierdzili, że SIRT5 specyficznie kontroluje sukcyny-lację TFR1 w jednym miejscu — przy reszcie aminokwasowej zwanej lizyną 626. Gdy SIRT5 był przytłumiony, TFR1 stał się bardziej sukcyny-lowany, stabilniejszy i bardziej obfity, co prowadziło do zwiększonego poboru żelaza i silniejszych sygnałów ferroptozy. Przywrócenie SIRT5 zmniejszało stabilność i ekspresję TFR1, ograniczając napływ żelaza i śmierć komórek.
Dowód powiązania między regulatorem a bramką żelazową
Zespół wykorzystał kilka komplementarnych technik, aby potwierdzić, że SIRT5 fizycznie wiąże się z TFR1 i modyfikuje jego stan. Mutacje różnych potencjalnych miejsc sukcyny-lacji na TFR1 wykazały, że tylko zmiany przy lizynie 626 zmieniały zarówno sukcyny-lację, jak i całkowite poziomy białka TFR1, wskazując na to miejsce jako krytyczny punkt kontroli. Doświadczenia typu pull-down i testy obrazowania oparte na bliskości potwierdziły bezpośrednią interakcję między SIRT5 a TFR1. Funkcjonalnie, nadekspresja SIRT5 sama w sobie uczyniła podocyty bardziej odpornymi na ferroptozę, lecz wymuszone ponowne zwiększenie poziomów TFR1 likwidowało tę ochronę, przywracając akumulację żelaza i uszkodzenia oksydacyjne. Wyniki te umieszczają SIRT5 i TFR1 w jednej ścieżce, która decyduje o podatności komórek nerkowych na uraz wywołany żelazem w warunkach cukrzyczych.
Co to może oznaczać dla przyszłych terapii
Podsumowując, badanie pokazuje, że QODG może łagodzić uszkodzenia nerek związane z cukrzycą w komórkach i u myszy przez zwiększenie SIRT5, które następnie usuwa grupę chemiczną z TFR1, destabilizując tę bramkę importu żelaza i tłumiąc ferroptozę. Dla czytelnika niebędącego specjalistą kluczowa myśl jest taka, że związek pochodzenia roślinnego wydaje się pomagać komórkom filtrującym nerki, „zamy-kając drzwi żelaza”, które zasilają niszczący typ śmierci komórkowej. Choć potrzebne są dalsze badania na większych modelach zwierzęcych, a ostatecznie w badaniach u ludzi, wyniki te podkreślają obiecującą strategię: celowanie w gospodarkę żelazem i oksydacyjną śmierć komórkową za pomocą naturalnych związków, aby spowolnić lub zapobiec nefropatii cukrzycowej.
Cytowanie: Wu, M., Ye, W. & Ye, X. Quercetin-4’-O-β-D-glucopyranoside inhibits ferroptosis though SIRT5-mediated desuccinylation of TFR1 in diabetic nephropathy. Sci Rep 16, 12384 (2026). https://doi.org/10.1038/s41598-026-41148-4
Słowa kluczowe: nefropatia cukrzycowa, ochrona nerek, ferroptoza, flawonoidy, metabolizm żelaza