Clear Sky Science · tr
Quercetin-4’-O-β-D-glucopyranoside, diyabetik nefropatide TFR1’in SIRT5 aracılı de-suksinilasyonu yoluyla ferroptozisi engelliyor
Bu, diyabetli kişiler için neden önemli
Böbrek hastalığı, diyabetin en ciddi uzun vadeli komplikasyonlarından biridir ve insanların diyalize veya nakile ihtiyaç duymasının önde gelen nedenlerinden biridir. Bu çalışma, bitkilerden türetilen doğal bir bileşik olan kersetin-4'-O-β-D-glukopiranozid (QODG) ile diyabete bağlı hasardan böbrekleri nasıl koruyabileceğini; demir ve oksidatif stresle tetiklenen belirli bir hücre ölümü biçimini engelleyerek incelemektedir. Bu sürecin anlaşılması, standart kan şekeri ve tansiyon kontrolünü tamamlayacak daha güvenli yeni tedavilere kapı aralayabilir.
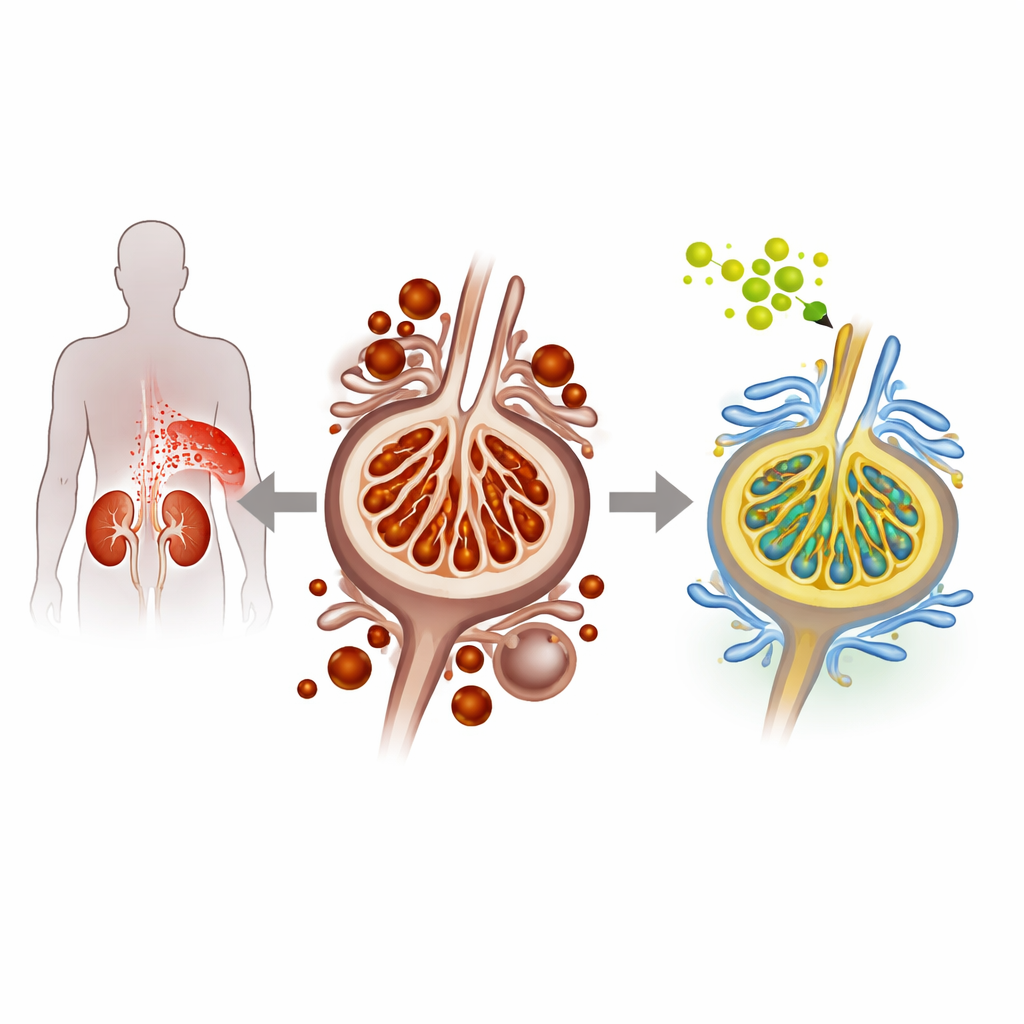
Şeker, böbreğin filtre hücrelerine zarar verdiğinde
Diyabetik nefropatide, yüksek kan şekeri zamanla böbreğin filtreleme birimlerini döşeyen ve protein kaçışını önleyen narin hücreler olan podositlere zarar verir. Araştırmacılar bu durumu taklit etmek için hem kültürde yetiştirilen fare podosit hücrelerini hem de diyabetik fare modelini kullandılar. Yüksek glukoz koşullarında podositlerde, aşırı demir ve hücre zarlarında biriken okside olmuş yağların tetiklediği ferroptozis adı verilen belirli bir hücre ölümü türünün belirtileri görüldü. Araştırma ekibi, hücre içi demirin arttığını, lipid peroksidasyonunun yükseldiğini ve doğal koruyucu protein düzeylerinin azaldığını gözlemledi; bunların hepsi artmış ferroptozis ve kötüleşen böbrek stresine işaret ediyordu.
Demir kaynaklı hasarı yatıştıran bir bitki molekülü
QODG, birçok meyvede ve tıbbi bitkide bulunan kersetine akraba bir flavonoid glikoziddir. Araştırmacılar yüksek glukozlu podositleri QODG ile muamele ettiğinde, hücre canlılığı belirgin bir doz-bağımlı şekilde iyileşti. Lipid peroksidasyon ve malondialdehit gibi oksidatif hasar belirteçleri azaldı, süperoksit dismutaz ve katalaz gibi antioksidan savunmalar yükseldi. Aynı zamanda ferroptozise karşı iki ana koruyucu olan GPX4 ve SLC7A11 protein düzeyleri arttı, hücre yüzeyindeki ana demir giriş kapısı olan transferrin reseptörü 1 (TFR1) düzeyleri ise düştü. Diyabetik farelerde QODG tedavisi yapısal böbrek hasarını azalttı, kan ve idrarla ölçülen böbrek fonksiyon bozukluğu belirteçlerini düşürdü ve zararlı oksidatif güçlerle koruyucu antioksidan sistemler arasındaki dengeyi düzeltti.
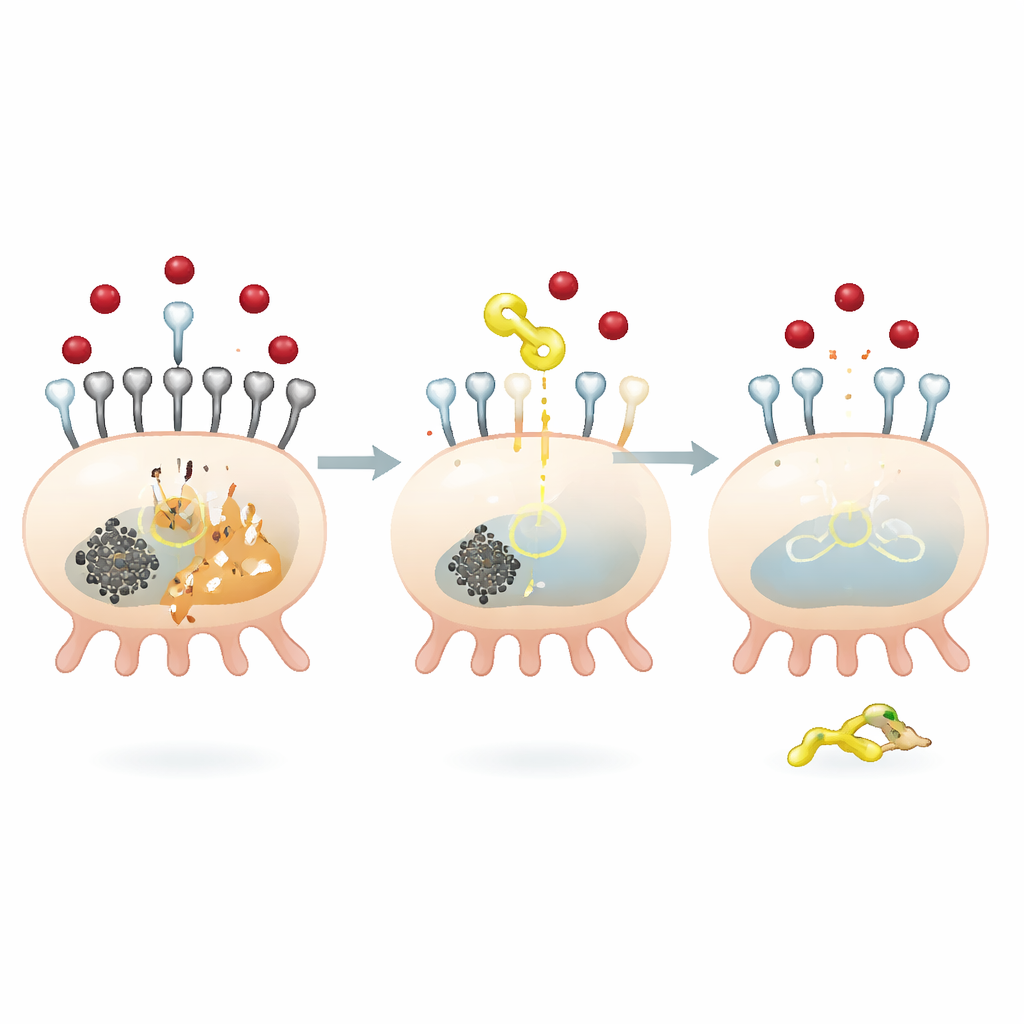
Böbrek hücrelerine demir girişini yavaşlatan moleküler bir fren
QODG’nin bu koruyucu etkileri nasıl sağladığını anlamak için ekip SIRT5 adlı bir proteine odaklandı; bu enzim diğer proteinlerden küçük bir kimyasal işaret olan suksinil grubunu çıkarır. Yüksek glukoz podositlerde global suksinilasyonu artırdı ve SIRT5 düzeylerini azalttı. QODG bunun tersini yaptı: SIRT5’i yükseltti ve toplam suksinilasyonu düşürdü, suksinil verici molekülün arzını değiştirmeden. Araştırmacılar SIRT5’in özellikle TFR1’in bir bölgesindeki, lizin 626 olarak adlandırılan amino asit pozisyonundaki suksinilasyonu kontrol ettiğini buldular. SIRT5 susturulduğunda, TFR1 daha fazla suksinillendi, daha kararlı ve daha bol bulundu; bu da artan demir alımı ve güçlenen ferroptozis sinyallerine yol açtı. Aksine, SIRT5’in geri getirilmesi TFR1 kararlılığını ve ifadesini azaltarak demir girişini ve hücre ölümünü dizginledi.
Yönlendirici ile demir kapısı arasındaki bağı kanıtlamak
Ekip, SIRT5’in fiziksel olarak TFR1’e bağlandığını ve onun modifikasyon durumunu ayarladığını doğrulamak için birkaç tamamlayıcı teknik kullandı. TFR1 üzerindeki farklı potansiyel suksinilasyon bölgelerinin mutasyona uğratılması, yalnızca lizin 626’daki değişikliklerin hem suksinilasyonu hem de toplam TFR1 protein düzeylerini etkilediğini gösterdi ve burayı kritik kontrol noktası olarak işaretledi. Biyokimyasal çekme (pull-down) deneyleri ve yakınlık tabanlı görüntüleme testi, SIRT5 ile TFR1 arasında doğrudan etkileşimi doğruladı. İşlevsel olarak, yalnızca SIRT5’in fazla eksprese edilmesi podositleri ferroptozise karşı daha dirençli hale getirdi, ancak TFR1 düzeylerini zorla geri yükseltmek bu korumayı ortadan kaldırdı; demir birikimini ve oksidatif hasarı yeniden getirdi. Bu bulgular, SIRT5 ve TFR1’i diyabetik koşullarda böbrek hücrelerinin demir kaynaklı hasara karşı duyarlılığını belirleyen tek bir yolakta konumlandırıyor.
Gelecekteki tedaviler için ne anlama gelebilir
Genel olarak çalışma, QODG’nin hücrelerde ve farelerde diyabetik böbrek hasarını azaltabildiğini; bunun SIRT5’i yükselterek TFR1’den kimyasal bir etiketi kaldırdığı, böylece bu demir giriş kapısını kararsızlaştırdığı ve ferroptozisi bastırdığı sonucuna varıyor. Bir okuyucu için temel fikir, bitki kökenli bir bileşiğin böbreğin filtre hücrelerine, yıkıcı bir hücre ölümü biçimini besleyen “demir kapısını” kapatarak yardımcı göründüğüdür. Daha büyük hayvan çalışmalarında ve nihayetinde insanlarda daha fazla çalışma gerekse de, bu sonuçlar umut verici bir stratefiyi vurguluyor: diyabetik böbrek hastalığını yavaşlatmak veya önlemek için demir yönetimini ve oksidatif hücre ölümü yollarını doğal moleküllerle hedeflemek.
Atıf: Wu, M., Ye, W. & Ye, X. Quercetin-4’-O-β-D-glucopyranoside inhibits ferroptosis though SIRT5-mediated desuccinylation of TFR1 in diabetic nephropathy. Sci Rep 16, 12384 (2026). https://doi.org/10.1038/s41598-026-41148-4
Anahtar kelimeler: diyabetik nefropati, böbrek koruması, ferroptozis, flavonoidler, demir metabolizması