Clear Sky Science · sv
Quercetin-4’-O-β-D-glucopyranoside hämmar ferroptos genom SIRT5-medierad desuccinylation av TFR1 vid diabetisk nefropati
Varför detta är viktigt för personer med diabetes
Njursjukdom är en av de allvarligaste långsiktiga komplikationerna till diabetes och en ledande orsak till att människor behöver dialys eller transplantationer. Denna studie undersöker en naturligt växtextraherad förening, quercetin-4'-O-β-D-glucopyranoside (QODG), och hur den kan skydda njurarna från diabetesrelaterad skada genom att blockera en specifik form av celldöd driven av järn och oxidativ stress. Att förstå denna process kan öppna dörren för nya, säkrare behandlingar som kompletterar standardkontroll av blodsocker och blodtryck.
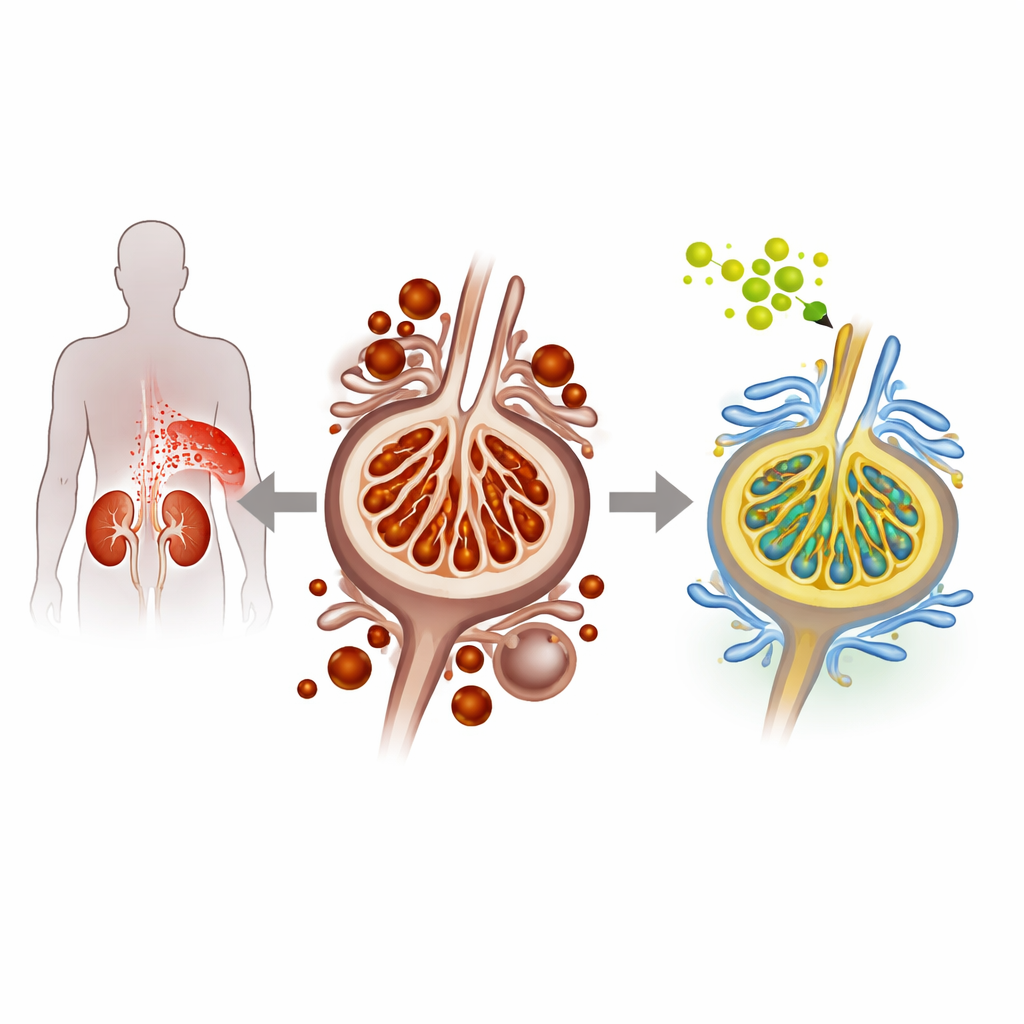
När socker skadar njurens filtrerande celler
Vid diabetisk nefropati skadar högt blodsocker gradvis podocyter, de känsliga cellerna som bekläder njurens filtreringselement och förhindrar proteiner från att läcka ut i urinen. Forskarna använde både odlade muspodocyter och en diabetisk musmodell för att efterlikna detta tillstånd. Under högglukosförhållanden visade podocyterna tecken på en särskild typ av celldöd kallad ferroptos, som drivs av överskott av järn och uppbyggnad av skadade, oxiderade lipider i cellmembran. Teamet observerade mer järn i cellerna, ökad lipidperoxidation och minskade nivåer av naturliga skyddsproteiner, vilket tillsammans tyder på ökad ferroptos och förvärrad njurstress.
En växtmolekyl som dämpar järndrivet skada
QODG är en flavonoidglykosid nära besläktad med quercetin, en förening som finns i många frukter och medicinalväxter. När forskarna behandlade högglukospodocyter med QODG förbättrades cellsurvivaliteten på ett tydligt dosberoende sätt. Markörer för oxidativ skada, såsom lipidperoxidation och malondialdehyd, sjönk medan antioxidativa försvar som superoxiddismutas och katalas ökade. Samtidigt ökade proteinnivåerna av GPX4 och SLC7A11, två nyckelvakter mot ferroptos, och nivåerna av transferrinreceptor 1 (TFR1), en viktig järnimportport i cellmembranet, minskade. I diabetiska möss minskade QODG-behandling strukturella njurskador, sänkte blod- och urinmarkörer för njurdysfunktion och återställde en hälsosammare balans mellan skadliga oxidativa krafter och skyddande antioxidativa system.
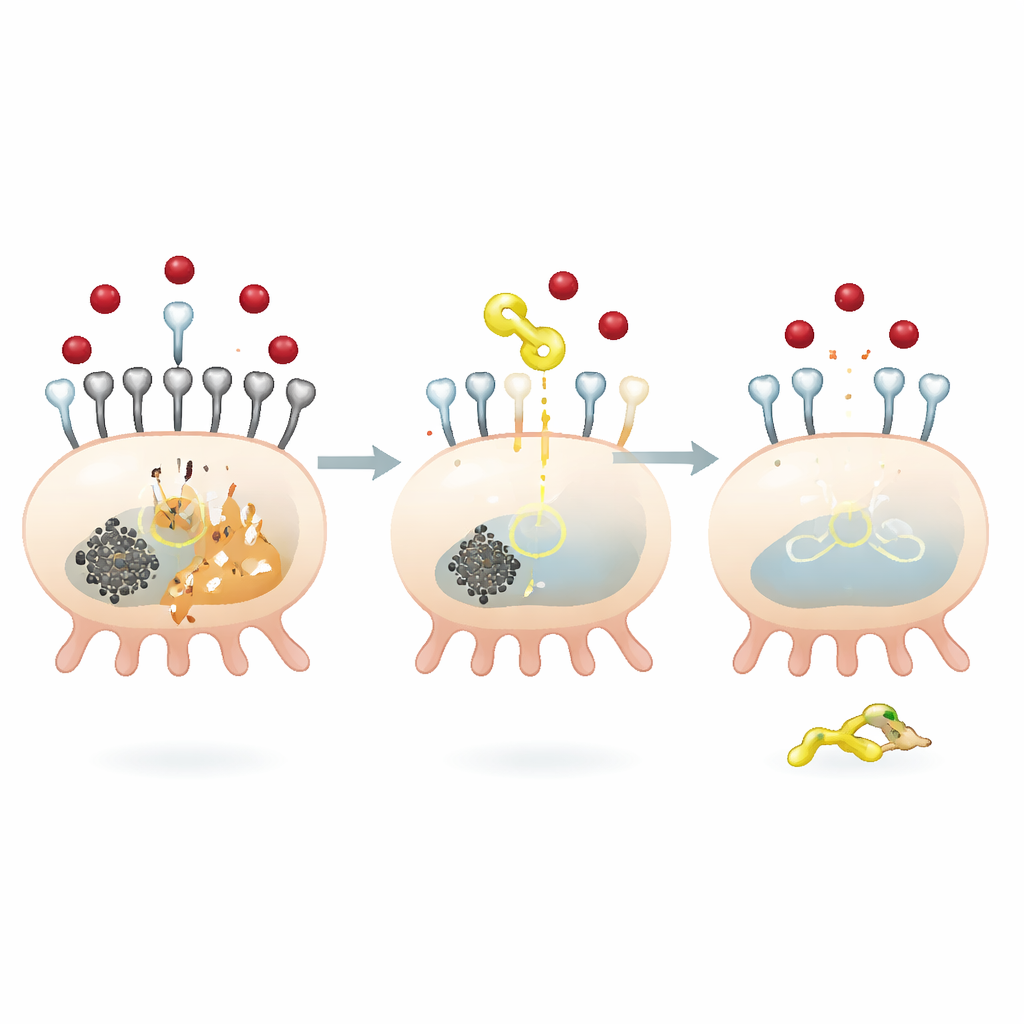
En molekylär broms på järninsläpp i njurceller
För att förstå hur QODG ger dessa skyddande effekter fokuserade teamet på ett protein kallat SIRT5, ett enzym som avlägsnar en liten kemisk märkning känd som en succinylgrupp från andra proteiner. Högt glukos ökade den globala succinylationen i podocyter och minskade SIRT5-nivåerna. QODG vände detta: det ökade SIRT5 samtidigt som den övergripande succinylationen återgick nedåt, utan att förändra tillgången på succinyl-donormolekylen. Forskarna fann att SIRT5 specifikt kontrollerar succinylationen av TFR1 vid en enda plats, en aminosyraposition kallad lysin 626. När SIRT5 tystades blev TFR1 mer succinylerad, mer stabil och mer riklig, vilket ledde till ökat järnupptag och starkare ferroptossignaler. Omvänt minskade återställande av SIRT5 TFR1-stabilitet och -uttryck, vilket bromsade järninflödet och celldöden.
Bevisa sambandet mellan regulatorn och järnporten
Teamet använde flera kompletterande tekniker för att bekräfta att SIRT5 fysiskt binder till TFR1 och justerar dess modifieringstillstånd. Mutering av olika potentiella succinylationsställen på TFR1 visade att endast förändringar vid lysin 626 påverkade både succinylation och total TFR1-proteinnivå, vilket identifierar detta som den kritiska kontrollpunkten. Biokemiska pull-down-experiment och en proximetsbaserad bildteknik bekräftade direkt interaktion mellan SIRT5 och TFR1. Funktionellt gjorde överuttryck av SIRT5 ensam podocyter mer motståndskraftiga mot ferroptos, men att tvinga upp TFR1-nivåerna igen utslett detta skydd och återställde järnansamling och oxidativ skada. Dessa fynd placerar SIRT5 och TFR1 i en enda väg som avgör hur sårbara njurceller är för järndriven skada under diabetiska förhållanden.
Vad detta kan betyda för framtida behandlingar
Sammantaget visar studien att QODG kan mildra diabetisk njurskada i celler och möss genom att öka SIRT5, som sedan tar bort en kemisk märkning från TFR1, destabiliserar denna järnimportport och dämpar ferroptos. För en lekmannaläsare är huvudidén att en växtbaserad förening verkar hjälpa njurens filtreringsceller genom att stänga det ”järndörren” som matar en destruktiv form av celldöd. Även om mer arbete krävs i större djurstudier och så småningom hos människor, lyfter resultaten fram en lovande strategi: att rikta in sig på järnhantering och oxidativ celldöd med naturliga molekyler för att bromsa eller förebygga diabetisk njursjukdom.
Citering: Wu, M., Ye, W. & Ye, X. Quercetin-4’-O-β-D-glucopyranoside inhibits ferroptosis though SIRT5-mediated desuccinylation of TFR1 in diabetic nephropathy. Sci Rep 16, 12384 (2026). https://doi.org/10.1038/s41598-026-41148-4
Nyckelord: diabetisk nefropati, njurskydd, ferroptos, flavonoider, järnmetabolism