Clear Sky Science · es
Quercetina-4’-O-β-D-glucopiranósido inhibe la ferroptosis mediante la desuccinilación de TFR1 mediada por SIRT5 en la nefropatía diabética
Por qué esto importa para las personas con diabetes
La enfermedad renal es una de las complicaciones crónicas más graves de la diabetes y una de las principales causas por las que las personas necesitan diálisis o trasplantes. Este estudio explora un compuesto natural de origen vegetal, quercetina-4'-O-β-D-glucopiranósido (QODG), y cómo podría proteger los riñones del daño relacionado con la diabetes bloqueando una forma específica de muerte celular impulsada por el hierro y el estrés oxidativo. Comprender este proceso podría abrir la puerta a tratamientos nuevos y más seguros que complementen el control habitual de la glucemia y la tensión arterial.
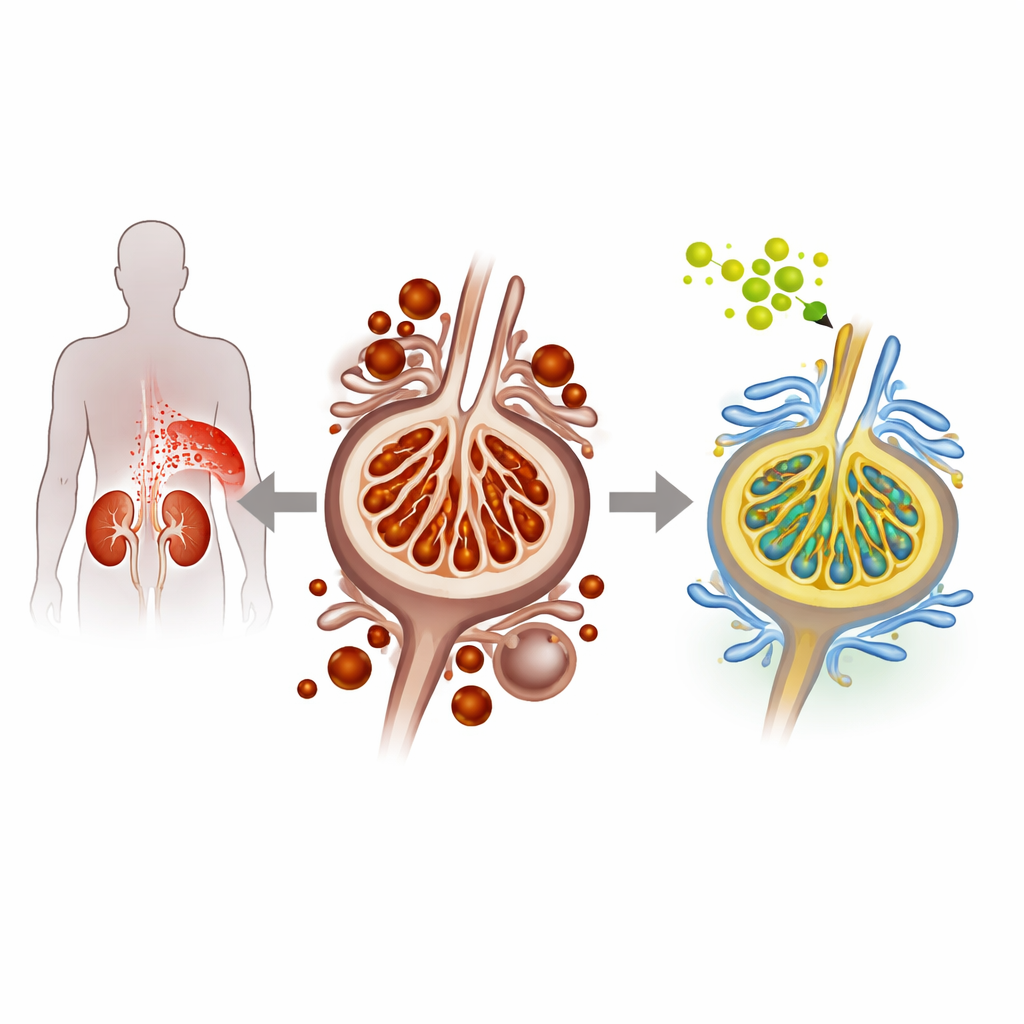
Cuando el azúcar daña las células filtro del riñón
En la nefropatía diabética, la hiperglucemia lesiona de forma progresiva a los podocitos, las células delicadas que recubren las unidades de filtración del riñón y evitan la pérdida de proteínas en la orina. Los investigadores emplearon tanto podocitos de ratón en cultivo como un modelo murino diabético para reproducir esta condición. Bajo condiciones de alto contenido de glucosa, los podocitos mostraron signos de un tipo particular de muerte celular llamada ferroptosis, que se alimenta del exceso de hierro y de la acumulación de lípidos dañados y oxidados en las membranas. El equipo observó más hierro intracelular, mayor peroxidación lipídica y niveles reducidos de proteínas protectoras naturales, todo lo cual indica una ferroptosis incrementada y un empeoramiento del estrés renal.
Una molécula vegetal que calma el daño impulsado por el hierro
QODG es una glucósido flavonoide relacionado con la quercetina, un compuesto presente en muchas frutas y plantas medicinales. Cuando los investigadores trataron podocitos expuestos a alta glucosa con QODG, la supervivencia celular mejoró de forma clara y dependiente de la dosis. Los marcadores de daño oxidativo, como la peroxidación lipídica y el malondialdehído, disminuyeron, mientras que las defensas antioxidantes como la superóxido dismutasa y la catalasa aumentaron. Al mismo tiempo, los niveles de proteína de GPX4 y SLC7A11, dos guardianes clave contra la ferroptosis, se incrementaron, y los niveles del receptor de transferrina 1 (TFR1), una puerta principal de entrada de hierro en la superficie celular, disminuyeron. En ratones diabéticos, el tratamiento con QODG redujo la lesión estructural renal, rebajó marcadores en sangre y orina de disfunción renal y restauró un equilibrio más sano entre fuerzas oxidativas dañinas y sistemas antioxidantes protectores.
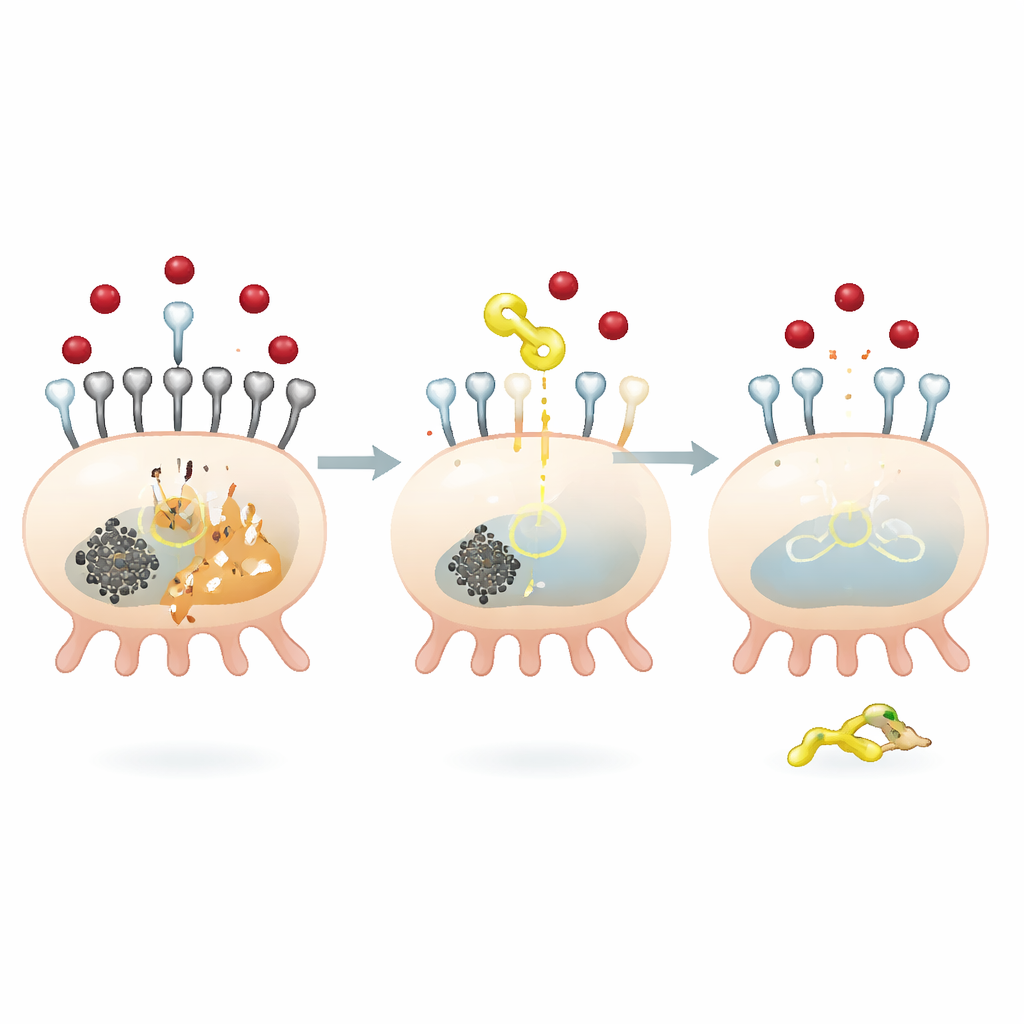
Un freno molecular sobre la entrada de hierro en las células renales
Para entender cómo QODG produce estos efectos protectores, el equipo se centró en una proteína llamada SIRT5, una enzima que elimina una pequeña etiqueta química conocida como grupo succinilo de otras proteínas. La alta glucosa aumentó la succinilación global dentro de los podocitos y redujo los niveles de SIRT5. QODG revirtió esto: aumentó SIRT5 mientras reducía la succinilación global, sin alterar la disponibilidad de la molécula donadora del succinilo. Los investigadores hallaron que SIRT5 controla específicamente la succinilación de TFR1 en un sitio concreto, una posición de aminoácido llamada lisina 626. Cuando SIRT5 fue silenciado, TFR1 presentó mayor succinilación, se volvió más estable y más abundante, provocando un aumento de la captación de hierro y señales más intensas de ferroptosis. Por el contrario, restaurar SIRT5 redujo la estabilidad y la expresión de TFR1, frenando la entrada de hierro y la muerte celular.
Demostrando el vínculo entre el regulador y la puerta de entrada del hierro
El equipo utilizó varias técnicas complementarias para confirmar que SIRT5 se une físicamente a TFR1 y ajusta su estado de modificación. Mutar diferentes sitios potenciales de succinilación en TFR1 mostró que solo los cambios en la lisina 626 alteraron tanto la succinilación como los niveles totales de proteína TFR1, señalando este residuo como el punto de control crítico. Experimentos bioquímicos de pull-down y un ensayo de imagen basado en proximidad confirmaron la interacción directa entre SIRT5 y TFR1. Funcionalmente, la sobreexpresión de SIRT5 por sí sola hizo a los podocitos más resistentes a la ferroptosis, pero forzar de nuevo los niveles de TFR1 eliminó esta protección, restaurando la acumulación de hierro y el daño oxidativo. Estos hallazgos sitúan a SIRT5 y TFR1 en una vía única que determina cuán vulnerables son las células renales al daño impulsado por el hierro en condiciones diabéticas.
Qué podría significar esto para tratamientos futuros
En conjunto, el estudio muestra que QODG puede aliviar el daño renal diabético en células y ratones al aumentar SIRT5, que a su vez elimina una etiqueta química de TFR1, desestabilizando esta puerta de entrada del hierro y atenuando la ferroptosis. Para un lector no especialista, la idea clave es que un compuesto de origen vegetal parece ayudar a las células filtro del riñón cerrando la "puerta del hierro" que alimenta una forma destructiva de muerte celular. Aunque se necesita más trabajo en estudios con animales de mayor tamaño y, finalmente, en humanos, estos resultados destacan una estrategia prometedora: dirigirse al manejo del hierro y a la muerte celular por oxidación con moléculas naturales para frenar o prevenir la enfermedad renal diabética.
Cita: Wu, M., Ye, W. & Ye, X. Quercetin-4’-O-β-D-glucopyranoside inhibits ferroptosis though SIRT5-mediated desuccinylation of TFR1 in diabetic nephropathy. Sci Rep 16, 12384 (2026). https://doi.org/10.1038/s41598-026-41148-4
Palabras clave: nefropatía diabética, protección renal, ferroptosis, flavonoides, metabolismo del hierro