Clear Sky Science · de
Quercetin-4’-O-β-D-glucopyranosid hemmt Ferroptose durch SIRT5-vermittelte Desuccinylierung von TFR1 bei diabetischer Nephropathie
Warum das für Menschen mit Diabetes wichtig ist
Nierenerkrankungen gehören zu den schwerwiegendsten Langzeitkomplikationen von Diabetes und sind eine Hauptursache dafür, dass Menschen Dialyse oder Transplantationen benötigen. Diese Studie untersucht eine natürlich vorkommende Pflanzenverbindung, Quercetin-4'-O-β-D-glucopyranosid (QODG), und wie sie die Nieren vor diabetesbedingten Schäden schützen könnte, indem sie eine spezifische Form des Zelltods blockiert, die durch Eisen und oxidativen Stress ausgelöst wird. Das Verständnis dieses Mechanismus könnte den Weg für neue, sichere Behandlungsansätze öffnen, die Standardmaßnahmen zur Blutzucker- und Blutdruckkontrolle sinnvoll ergänzen.
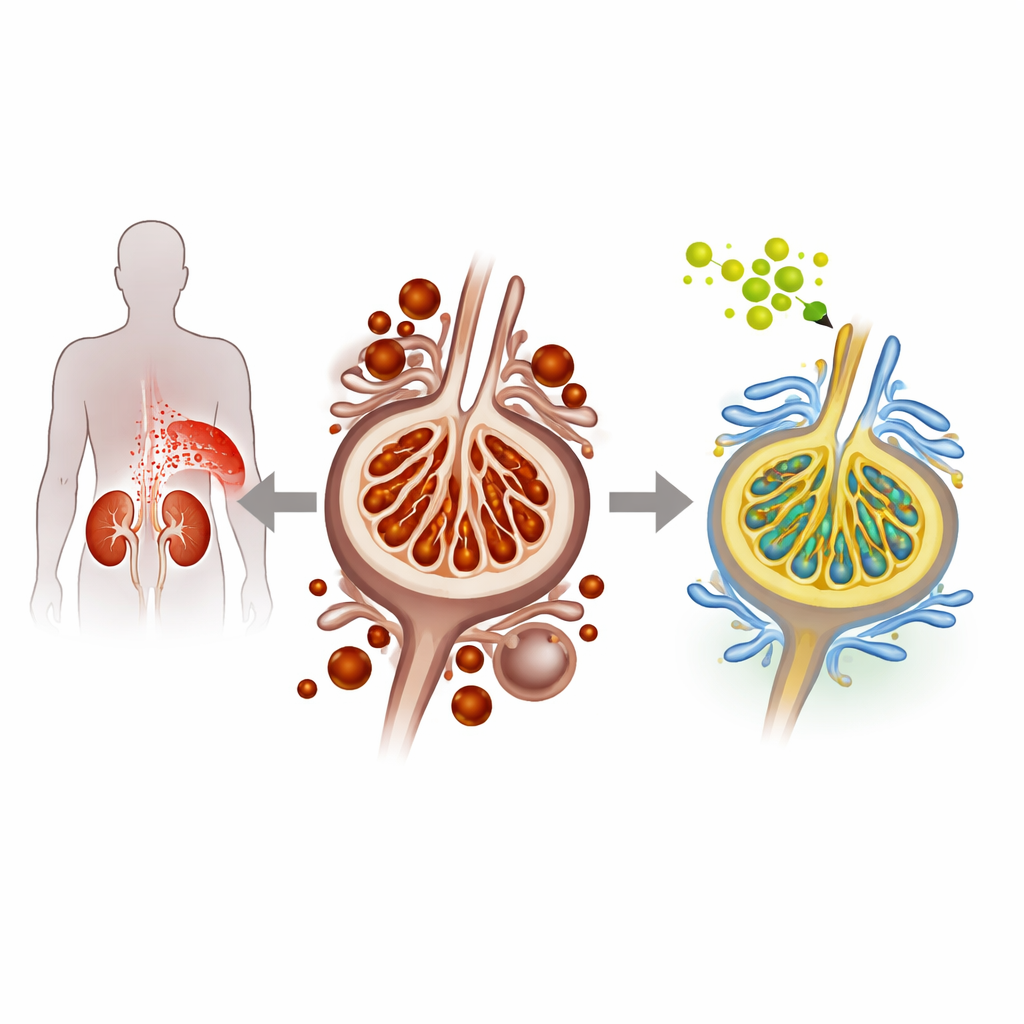
Wenn Zucker die Filterzellen der Niere schädigt
Bei der diabetischen Nephropathie schädigt hoher Blutzucker allmählich Podocyten, die empfindlichen Zellen, die die Nierenfilter auskleiden und Proteinverlust im Urin verhindern. Die Forschenden verwendeten sowohl kultivierte Maus-Podocyten als auch ein diabetisches Mausmodell, um diesen Zustand nachzuahmen. Unter Hochglukosebedingungen zeigten die Podocyten Anzeichen einer bestimmten Form des Zelltods, der Ferroptose genannt wird und durch überschüssiges Eisen sowie die Ansammlung beschädigter, oxidierter Lipide in Zellmembranen angetrieben wird. Das Team beobachtete mehr zelluläres Eisen, stärkere Lipidperoxidation und reduzierte Mengen natürlicher Schutzproteine — alles Hinweise auf verstärkte Ferroptose und zunehmenden Nierenstress.
Ein Pflanzenmolekül, das eisenbedingte Schäden beruhigt
QODG ist ein Flavonoid-Glykosid, verwandt mit Quercetin, einem in vielen Früchten und Heilpflanzen vorkommenden Stoff. Behandelten die Forschenden Hochglukose-Podocyten mit QODG, verbesserte sich das Überleben der Zellen deutlich dosisabhängig. Marker oxidativer Schäden wie Lipidperoxidation und Malondialdehyd sanken, während antioxidative Abwehrmechanismen wie Superoxiddismutase und Katalase zunahmen. Gleichzeitig stiegen die Proteinmengen von GPX4 und SLC7A11, zwei wichtigen Schutzfaktoren gegen Ferroptose, während die Spiegel des Transferrinrezeptors 1 (TFR1), einem zentralen Tor für Eisenaufnahme an der Zelloberfläche, abnahmen. Bei diabetischen Mäusen reduzierte die QODG-Behandlung strukturelle Nierenschäden, senkte Blut- und Urinmarker für Nierenfunktionsstörungen und stellte ein gesünderes Gleichgewicht zwischen schädlichen oxidativen Kräften und schützenden Antioxidantien wieder her.
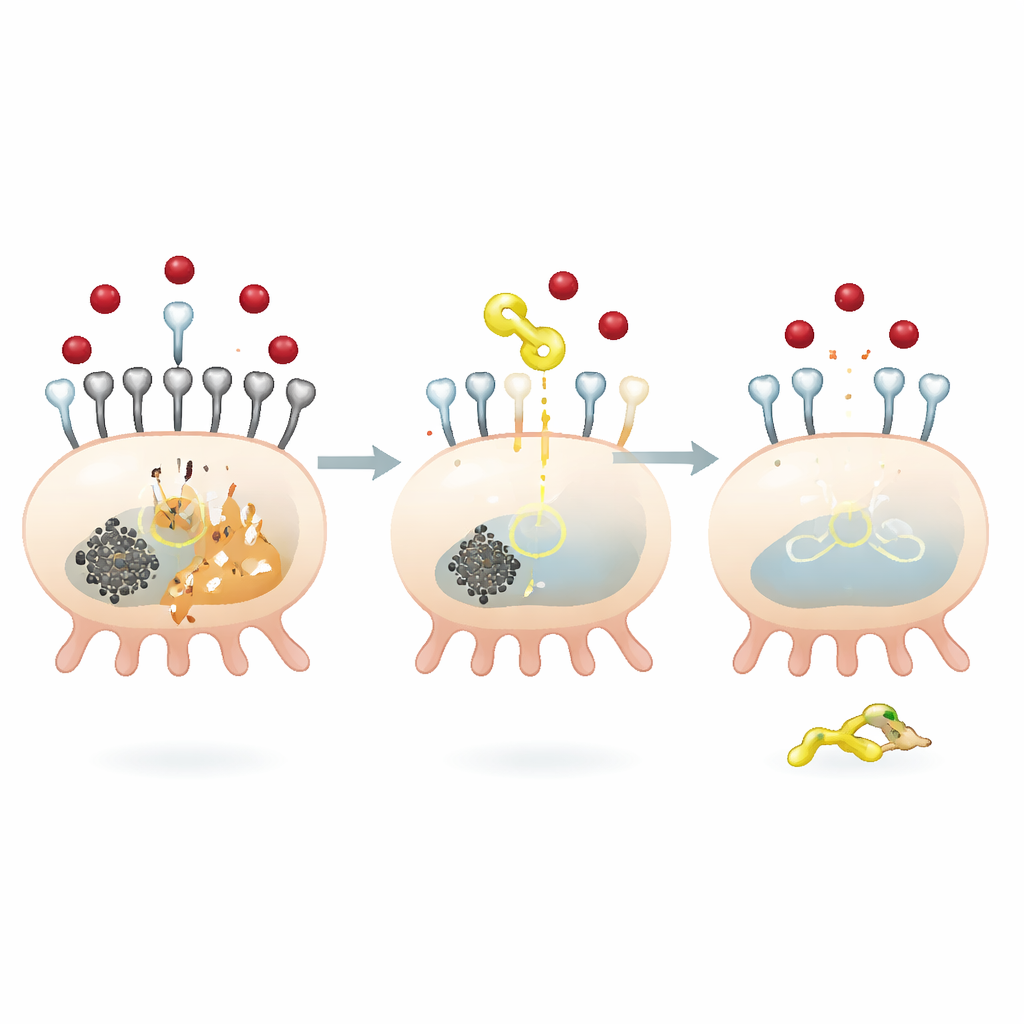
Eine molekulare Bremse für den Eiseneintritt in Nierenzellen
Um zu verstehen, wie QODG diese Schutzwirkung vermittelt, richtete das Team den Blick auf ein Protein namens SIRT5, ein Enzym, das eine kleine chemische Markierung, die Succinylgruppe, von anderen Proteinen entfernt. Hoher Glukosespiegel erhöhte die globale Succinylierung in Podocyten und verringerte die SIRT5-Spiegel. QODG kehrte dies um: Es steigerte SIRT5 und senkte gleichzeitig die Gesamt-Succinylierung, ohne die Verfügbarkeit des Succinyl-Donormoleküls zu verändern. Die Forschenden fanden heraus, dass SIRT5 die Succinylierung von TFR1 an einer bestimmten Stelle kontrolliert — der Aminosäureposition Lysin 626. Wurde SIRT5 ausgeschaltet, wurde TFR1 stärker succinyliert, stabiler und häufiger vorhanden, was zu erhöhter Eisenaufnahme und stärkeren Ferroptosesignalen führte. Umgekehrt führte die Wiederherstellung von SIRT5 zu geringerer TFR1-Stabilität und -Expression, wodurch Eisenzufluss und Zelltod gedämpft wurden.
Der Nachweis der Verbindung zwischen dem Regulator und dem Eisenportal
Das Team nutzte mehrere komplementäre Techniken, um zu bestätigen, dass SIRT5 physisch an TFR1 bindet und dessen Modifikationszustand verändert. Mutationen an verschiedenen potenziellen Succinylierungsstellen auf TFR1 zeigten, dass nur Veränderungen am Lysin 626 sowohl die Succinylierung als auch die Gesamtmenge an TFR1-Protein veränderten — womit dieser Ort als kritischer Kontrollpunkt identifiziert wurde. Biochemische Pull-down-Experimente und ein proximitätsbasiertes Bildgebungsverfahren bestätigten die direkte Wechselwirkung zwischen SIRT5 und TFR1. Funktionell machte allein die Überexpression von SIRT5 Podocyten widerstandsfähiger gegen Ferroptose, aber das erzwungene Wiederanstieg von TFR1 hob diesen Schutz auf und stellte Eisenakkumulation sowie oxidativen Schaden wieder her. Diese Befunde ordnen SIRT5 und TFR1 in einen gemeinsamen Pfad ein, der bestimmt, wie anfällig Nierenzellen unter diabetischen Bedingungen für eisengetriebene Schäden sind.
Was das für künftige Therapien bedeuten könnte
Insgesamt zeigt die Studie, dass QODG diabetische Nierenschäden in Zellen und Mäusen lindern kann, indem es SIRT5 hochreguliert, das wiederum eine chemische Markierung von TFR1 entfernt, dieses Eisenaufnahmeportal destabilisiert und so die Ferroptose dämpft. Für nichtfachliche Leser lautet die Kernaussage: Eine pflanzenbasierte Verbindung scheint Nierenfilterzellen zu schützen, indem sie die „Eisentür“ schließt, die eine zerstörerische Form des Zelltods nährt. Zwar sind weitere Studien in größeren Tiermodellen und schließlich am Menschen nötig, doch heben diese Ergebnisse eine vielversprechende Strategie hervor: das gezielte Eingreifen in Eisenhaushalt und oxidativen Zelltod mit natürlichen Molekülen, um das Fortschreiten der diabetischen Nierenerkrankung zu verlangsamen oder zu verhindern.
Zitation: Wu, M., Ye, W. & Ye, X. Quercetin-4’-O-β-D-glucopyranoside inhibits ferroptosis though SIRT5-mediated desuccinylation of TFR1 in diabetic nephropathy. Sci Rep 16, 12384 (2026). https://doi.org/10.1038/s41598-026-41148-4
Schlüsselwörter: diabetische Nephropathie, Nierenschutz, Ferroptose, Flavonoide, Eisenstoffwechsel