Clear Sky Science · zh
在伴发感染性休克的急性肾损伤(AKI)中由TREM1–NLRP3驱动的焦亡及并行自噬变化
为什么这个肾脏故事重要
感染性休克是一种对感染的危及生命的过度反应,常常首先波及肾脏,导致数百万人每年发生急性肾衰竭。一旦肾功能受损,死亡风险急剧上升,但临床上仍缺乏精确的早期预警信号和有针对性的治疗。本研究探讨了在感染性休克时肾细胞内新发现的一系列连锁反应——一种可能将保护性免疫防御转变为自我破坏性风暴的过程——并考察中断该链条是否既能更早提示危险,又能保护肾脏免受重度损伤。
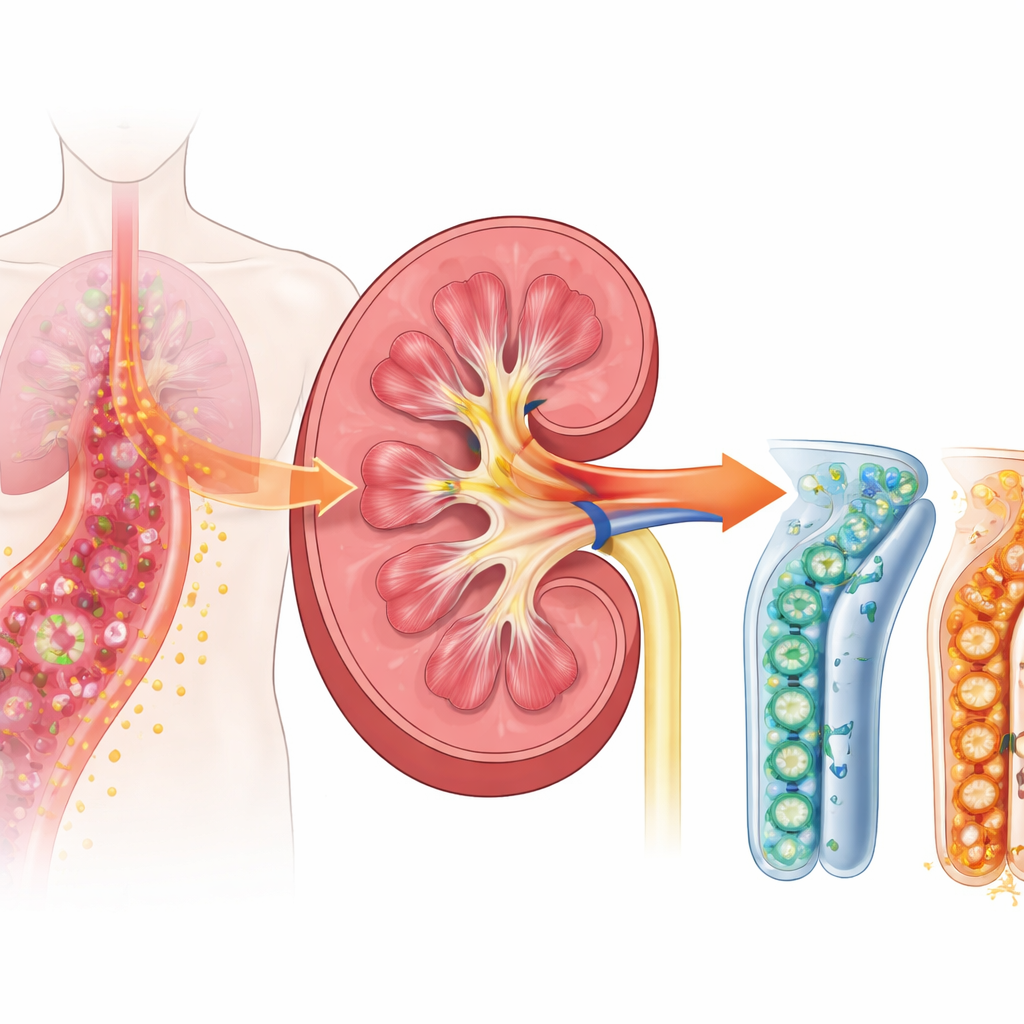
感染性休克中的危险连锁反应
当发生感染性休克时,机体免疫系统为了对抗入侵微生物而进入过度状态。肾脏不仅仅是过滤器;其肾小管细胞也参与感染的感知与响应。研究者关注一种称为TREM-1的表面受体,该受体存在于免疫细胞上,且近来的研究表明也存在于肾小管细胞上。TREM-1类似于炎症的音量旋钮:一旦被调高,它会极大放大驱动肿胀、发热和组织损伤的报警信号。既往病人研究显示,这种受体的可溶形式在血液和尿液中提前升高并与肾脏问题相关,提示TREM-1可能是导致损伤的重要上游触发因子。
从警报信号到细胞爆裂
在肾小管细胞内,研究团队考察了TREM-1如何与一个称为炎症小体的分子机器相连,该机器控制着一种有时被形容为细胞爆炸的戏剧性细胞死亡。在接受标准感染性休克模型处理的小鼠中,作者发现感染性休克显著提高了肾脏和血液中TREM-1的水平,同时激活了以NLRP3蛋白为核心的炎症小体。一旦被激活,这个复合体会激活能够在细胞膜上打孔并释放强效炎症分子的酶,从而导致细胞死亡。这种激烈的死亡程序称为焦亡,能帮助清除感染,但如果不受控制,也会摧毁大量脆弱的肾组织。
调低音量旋钮并检验通路
为了解TREM-1在这一连锁反应中的关键性,研究者使用了缺失Trem1基因的转基因小鼠。与经受同样感染性冲击的正常小鼠相比,这些基因敲除动物的肾小管结构损伤较轻,血液中肌酐和尿素等代谢废物水平较低,循环中的炎性分子也更少。它们的肾脏还显示出较低的NLRP3炎症小体活性和焦亡细胞死亡的迹象。当研究组直接用药物抑制NLRP3时,即便在正常小鼠中肾损伤也得到改善,而在Trem1缺失时强行激活NLRP3则加重了损伤。这些实验共同将TREM-1明确置于NLRP3之前的损伤级联反应上游。
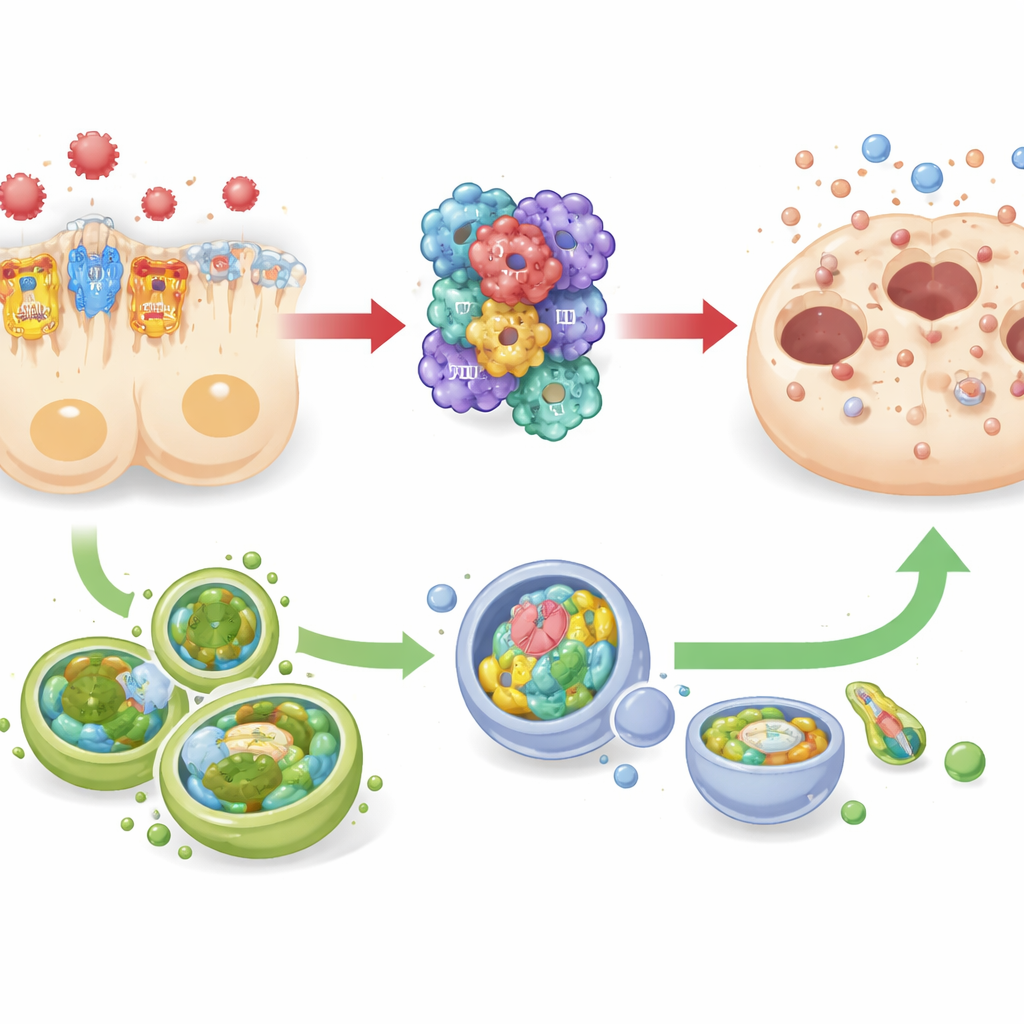
与细胞清理系统的拉锯战
该研究还追踪了自噬的变化——自噬是细胞内的一种内建清理与回收系统,通过移除受损成分帮助细胞在压力下存活。在感染性休克小鼠和体外培养的人肾小管细胞中,降低TREM-1与自噬相关标志物水平升高相关,而更强的TREM-1信号则与自噬降低同时出现。与此同时,炎症小体活性和细胞死亡标志物呈相反变化。该模式暗示了一种推拉关系:TREM-1与NLRP3共同充当破坏性炎症的“加速踏板”,而自噬更像是可能抵消这一驱动的“刹车”。然而,由于研究者并未直接开关自噬,他们提醒其保护作用尽管强烈被怀疑,但尚需进一步证明。
这对患者可能意味着什么
对感染性休克患者而言,这些发现有两点重要含义。首先,血液或尿液中可溶性TREM-1可能作为一种早期预警标志,提示在临床出现全面肾功能衰竭前该损伤通路在肾脏内已被激活。其次,抑制TREM-1或NLRP3炎症小体的药物未来或可用于保护肾脏免受感染性休克相关损伤,尤其适用于那些实验室检测显示该通路强烈激活的患者。本研究将感染性休克相关肾损伤描绘成炎症加速器与细胞内清理系统之间的较量,并将TREM-1确定为一个有前景的靶点,既可用于识别高危患者,也可用于设计更精准的治疗方案。
引用: Liu, X., Chen, Q., Chen, X. et al. TREM1–NLRP3–driven pyroptosis in sepsis-associated acute kidney injury (AKI) with parallel autophagy changes. Sci Rep 16, 14239 (2026). https://doi.org/10.1038/s41598-026-40893-w
关键词: 感染性休克相关的急性肾损伤, TREM-1, NLRP3 炎症小体, 焦亡, 自噬