Clear Sky Science · it
Piroptosi guidata da TREM1–NLRP3 nell’insufficienza renale acuta associata a sepsi (AKI) con cambiamenti paralleli dell’autofagia
Perché questa storia renale è importante
La sepsi, una reazione potenzialmente letale a un’infezione, colpisce spesso i reni per primi, provocando insufficienza renale improvvisa in milioni di persone ogni anno. Quando i reni cedono, il rischio di morte aumenta drasticamente, eppure i medici dispongono ancora di segnali precoci poco precisi e di terapie mirate limitate. Questo studio esplora una catena di eventi recentemente scoperta all’interno delle cellule renali durante la sepsi—una catena che può trasformare le difese immunitarie protettive in una tempesta autodistruttiva—e valuta se interrompere questa sequenza possa sia segnalare il pericolo più precocemente sia proteggere i reni da danni gravi.
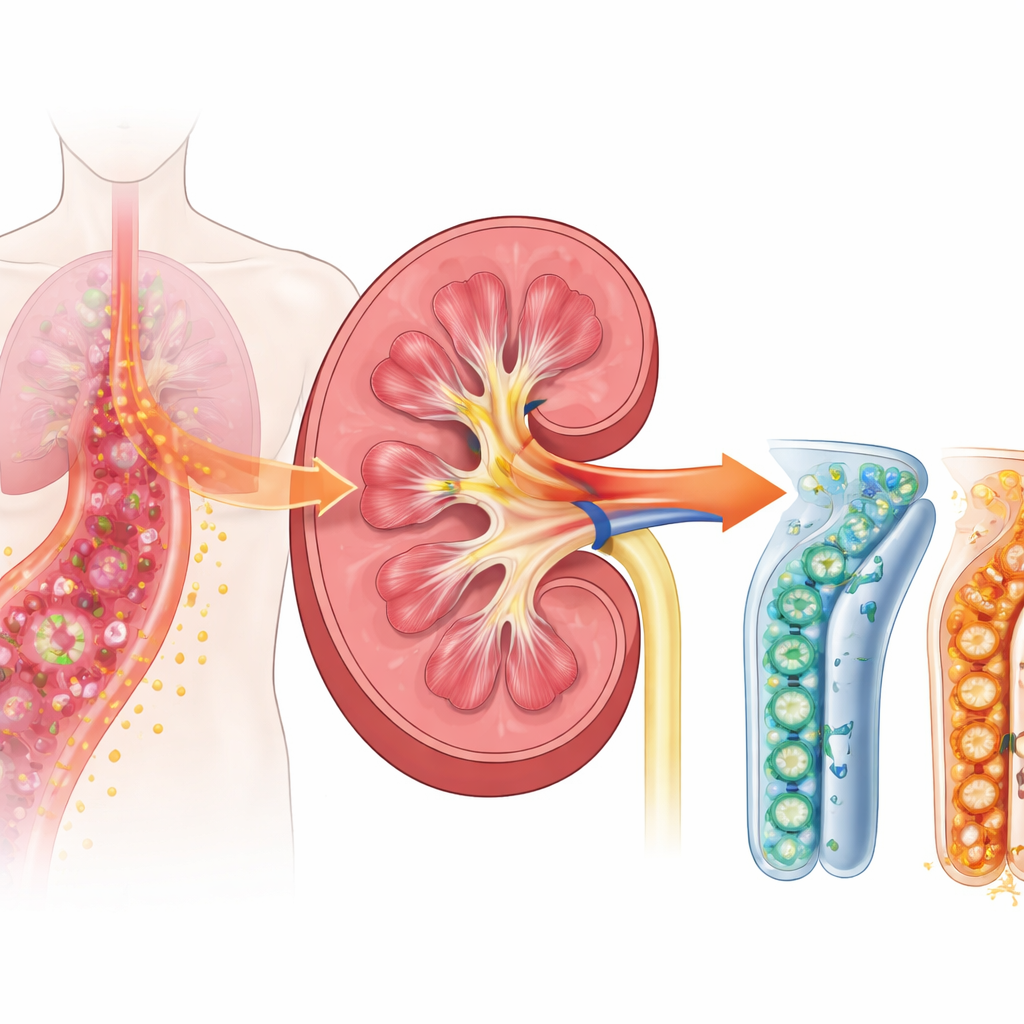
Una pericolosa reazione a catena nella sepsi
Quando la sepsi si sviluppa, il sistema immunitario entra in iperattivazione per combattere i microbi invasori. I reni non sono solo filtri; le loro cellule tubolari contribuiscono anche a percepire e rispondere all’infezione. I ricercatori si sono concentrati su un recettore di membrana chiamato TREM-1, presente sulle cellule immunitarie e, come suggerisce lavoro più recente, anche sulle cellule tubulari renali. TREM-1 funziona come una manopola del volume per l’infiammazione: una volta aumentato, può amplificare notevolmente i segnali d’allarme che guidano gonfiore, febbre e danno tissutale. Studi precedenti sui pazienti hanno mostrato che una forma solubile di questo recettore, rilasciata in sangue e urine, aumenta precocemente nella sepsi ed è associata a problemi renali, suggerendo che TREM-1 possa essere un importante innesco a monte del danno.
Dal segnale d’allarme all’esplosione cellulare
All’interno delle cellule tubulari renali, il team ha esaminato come TREM-1 si colleghi a una macchina molecolare chiamata inflammasoma, che regola un tipo drammatico di morte cellulare a volte descritta come esplosione cellulare. In topi sottoposti a un modello standard di sepsi, gli autori hanno riscontrato che la sepsi aumentava fortemente i livelli di TREM-1 nei reni e nel sangue, insieme all’attivazione di un inflammasoma costruito attorno a una proteina chiamata NLRP3. Una volta attivato, questo complesso accende enzimi che perforano le membrane cellulari e rilasciano potenti molecole infiammatorie, uccidendo la cellula nel processo. Questo programma di morte infiammatoria, noto come piroptosi, può aiutare a eliminare l’infezione ma, se non controllato, può anche distruggere ampie aree di tessuto renale fragile.
Abbassare la manopola del volume e testare la via
Per verificare quanto sia cruciale TREM-1 in questa reazione a catena, i ricercatori hanno utilizzato topi ingegnerizzati geneticamente privi del gene Trem1. Rispetto ai topi normali sottoposti allo stesso insulto settico, questi animali knockout mostravano minori danni strutturali nei tubuli renali, livelli ematici inferiori di scorie come creatinina e urea e una minore presenza di molecole infiammatorie nel sangue. I loro reni mostravano anche segni ridotti di attività dell’inflammasoma NLRP3 e di morte cellulare piroptotica. Quando il team bloccò direttamente NLRP3 con un farmaco, il danno renale migliorò anche nei topi normali, mentre forzare l’attivazione di NLRP3 aggravò il danno anche in assenza di Trem1. Insieme, questi esperimenti collocano TREM-1 chiaramente a monte di NLRP3 nella cascata di danno.
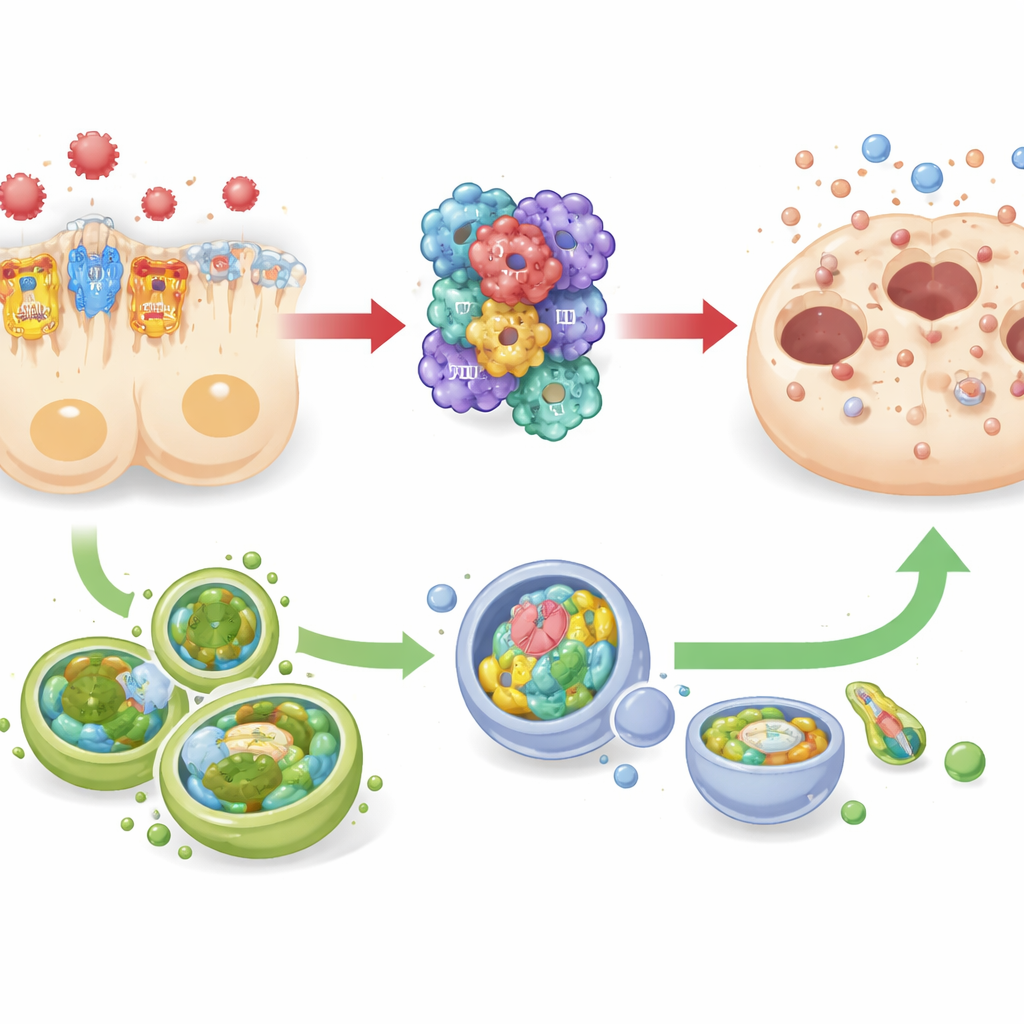
Una lotta tra il pedale dell’infiammazione e l’equipe di pulizia cellulare
Lo studio ha tracciato anche i cambiamenti dell’autofagia—un sistema di pulizia e riciclo intrinseco che aiuta le cellule a sopravvivere allo stress rimuovendo componenti danneggiati. Sia nei topi settici sia in cellule tubulari renali umane coltivate in laboratorio, l’abbassamento di TREM-1 è risultato correlato a livelli più alti di marcatori legati all’autofagia, mentre un segnale TREM-1 più forte coincideva con una riduzione dell’autofagia. Allo stesso tempo, l’attività dell’inflammasoma e i marcatori di morte cellulare si muovevano nella direzione opposta. Questo schema suggerisce una relazione push–pull: TREM-1 e NLRP3 che agiscono insieme come un “pedale dell’acceleratore” per un’infiammazione distruttiva, e l’autofagia che si comporta più come un “freno” che potrebbe controbilanciare questa spinta. Tuttavia, poiché i ricercatori non hanno attivato o inibito direttamente l’autofagia, avvertono che il suo ruolo protettivo, pur fortemente sospettato, resta da dimostrare.
Cosa potrebbe significare per i pazienti
Per le persone con sepsi, i risultati hanno due implicazioni principali. Primo, la forma solubile di TREM-1 nel sangue o nelle urine potrebbe fungere da marcatore di allerta precoce, indicando che questa via dannosa è attiva nei reni prima che si manifesti un’insufficienza conclamata. Secondo, farmaci che attenuano TREM-1 o l’inflammasoma NLRP3 potrebbero un giorno proteggere i reni dal danno legato alla sepsi, in particolare nei pazienti i cui esami mostrano una forte attivazione di questa via. Il lavoro delinea l’insufficienza renale associata a sepsi come una battaglia tra un acceleratore infiammatorio e un sistema di pulizia interno, e identifica TREM-1 come una leva promettente sia per individuare i pazienti ad alto rischio sia per progettare terapie più mirate.
Citazione: Liu, X., Chen, Q., Chen, X. et al. TREM1–NLRP3–driven pyroptosis in sepsis-associated acute kidney injury (AKI) with parallel autophagy changes. Sci Rep 16, 14239 (2026). https://doi.org/10.1038/s41598-026-40893-w
Parole chiave: insufficienza renale acuta associata a sepsi, TREM-1, inflammasoma NLRP3, piroptosi, autofagia