Clear Sky Science · ru
Пироптоз, опосредованный TREM1–NLRP3, при сепсис-ассоциированной острой почечной недостаточности (ОПН) с параллельными изменениями аутфагии
Почему эта история о почках важна
Сепсис, угрожающее жизни чрезмерное реагирование на инфекцию, часто поражает сначала почки, приводя к внезапной почечной недостаточности у миллионов людей ежегодно. Как только почки дают сбой, риск смерти резко возрастает, однако врачам по‑прежнему не хватает точных ранних сигналов тревоги и таргетных методов лечения. В этом исследовании изучается недавно обнаруженная цепная реакция внутри клеток почек при сепсисе — та, что может превратить защитные иммунные реакции в саморазрушительную бурю — и выясняется, можно ли прервать эту цепочку, чтобы раньше обнаруживать опасность и защитить почки от тяжёлых повреждений.
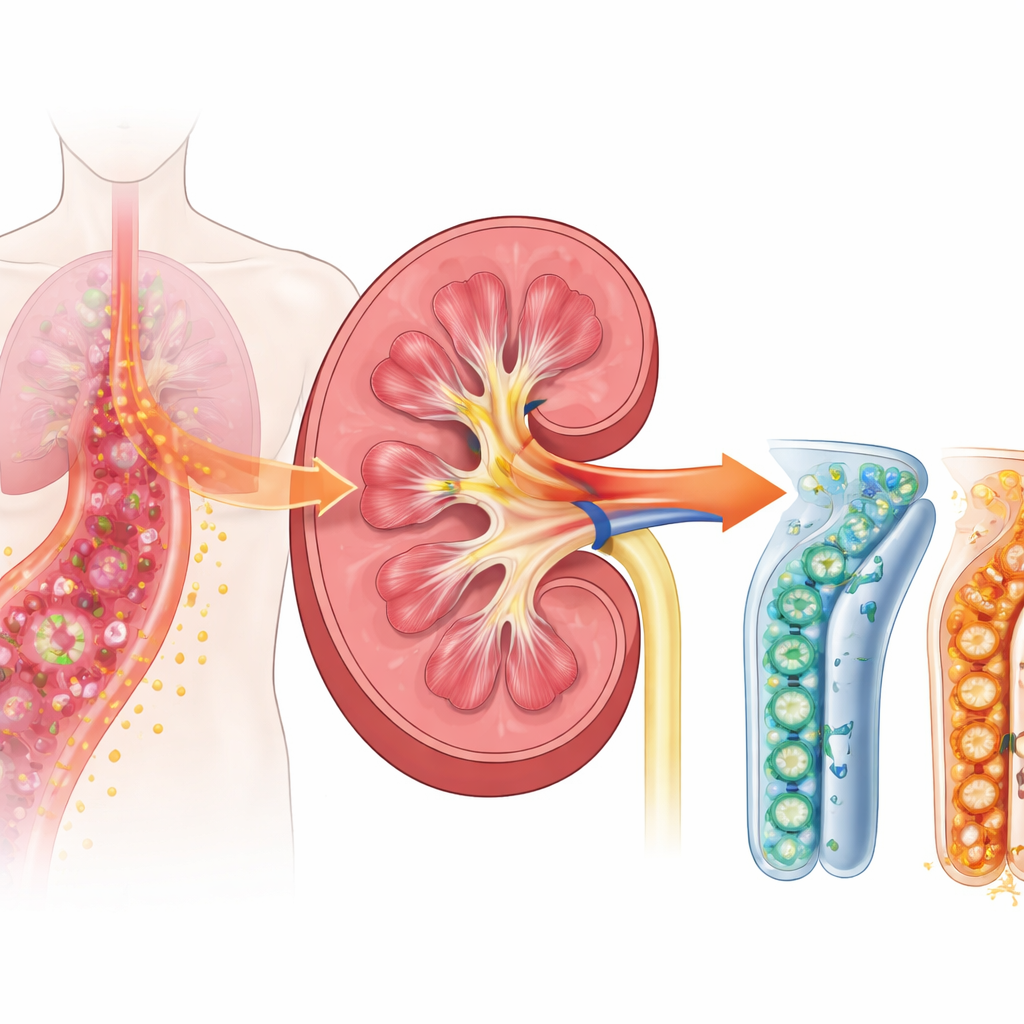
Опасная цепная реакция при сепсисе
При развитии сепсиса иммунная система организма входит в режим повышенной готовности, чтобы сражаться с вторгающимися микроорганизмами. Почки — это не только фильтры; их канальцевые клетки также помогают распознавать и реагировать на инфекцию. Исследователи сосредоточились на поверхностном рецепторе под названием TREM-1, который расположен на иммунных клетках и, как показывают новые данные, также на клетках канальцев почек. TREM-1 действует как ручка усиления воспаления: при включении он может значительно усилить сигналы тревоги, ведущие к отёку, лихорадке и повреждению тканей. Предыдущие исследования у пациентов показали, что растворимая форма этого рецептора, попадающая в кровь и мочу, повышается на ранних стадиях сепсиса и связана с проблемами почек, что указывает на то, что TREM-1 может быть важным верхнеуровневым триггером повреждения.
От сигнала тревоги до взрыва клетки
Внутри клеток канальцев почек команда исследователей изучала, как TREM-1 связывается с молекулярным комплексом — инфламмасомой, управляющей драматическим типом гибели клетки, иногда описываемым как клеточный взрыв. У мышей, подвергнутых стандартной модели сепсиса, авторы обнаружили резкое повышение уровней TREM-1 в почках и в крови, а также активацию инфламмасомы, собранной вокруг белка NLRP3. После включения этот комплекс активирует ферменты, которые проделывают отверстия в мембранах клеток и высвобождают мощные провоспалительные молекулы, убивая клетку в процессе. Эта «огненная» программа гибели, известная как пироптоз, может помогать в очищении инфекции, но при отсутствии контроля может также уничтожать большие участки хрупкой почечной ткани.
Уменьшение громкости и тестирование пути
Чтобы оценить, насколько важен TREM-1 в этой цепочке, исследователи использовали мышей, генетически лишённых гена Trem1. По сравнению с обычными мышами, подвергнутыми тому же септическому воздействию, у этих нокаутов было меньше структурных повреждений канальцев почек, ниже уровни в крови продуктов обмена, таких как креатинин и мочевина, и меньше циркулирующих провоспалительных молекул. В их почках также наблюдалось снижение признаков активности инфламмасомы NLRP3 и пироптотической гибели клеток. Когда команда напрямую блокировала NLRP3 с помощью препарата, повреждение почек уменьшалось даже у обычных мышей, тогда как принудительная активация NLRP3 усугубляла повреждения даже при отсутствии Trem1. В совокупности эти эксперименты чётко помещают TREM-1 выше NLRP3 в каскаде повреждений.
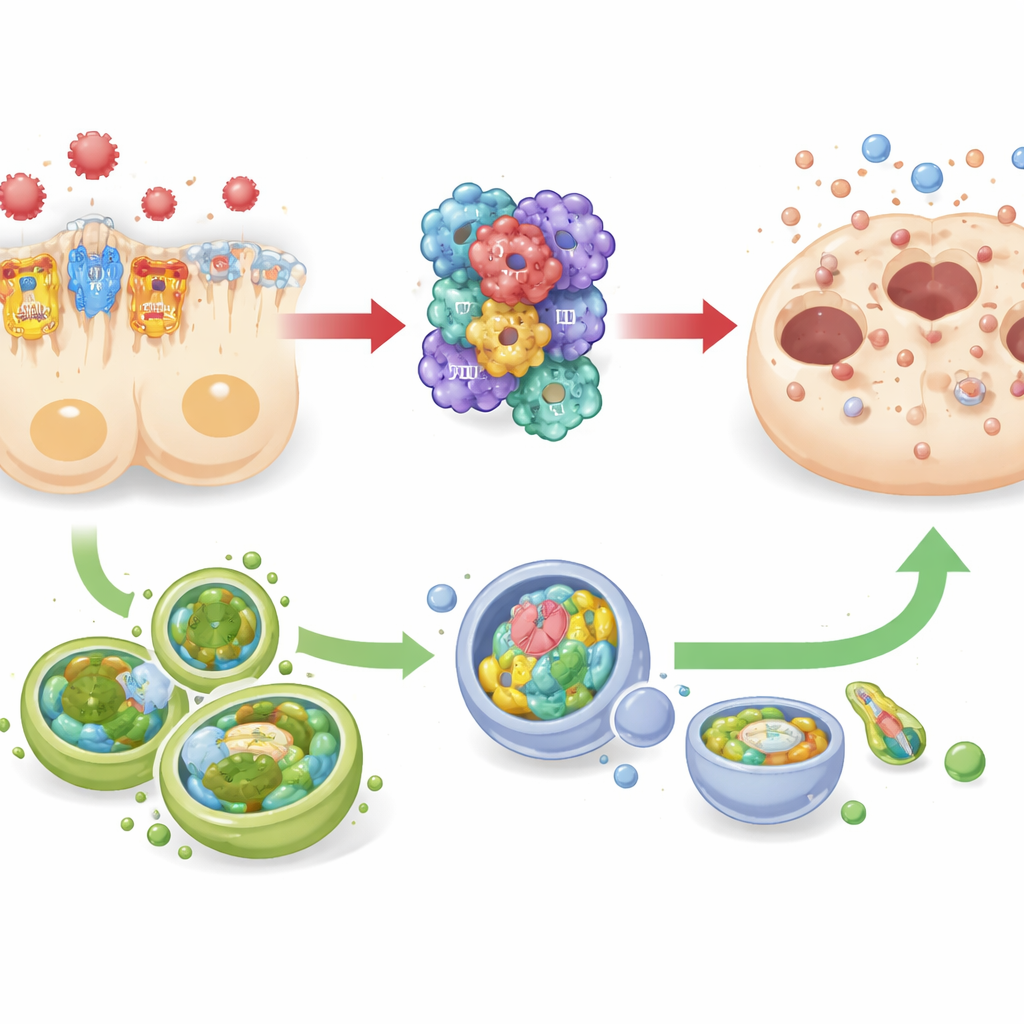
Перетягивание каната с системой уборки клетки
Исследование также отслеживало изменения в аутфагии — встроенной системе очистки и переработки, которая помогает клеткам переживать стресс, удаляя повреждённые компоненты. И в септических мышах, и в культивируемых в лаборатории человеческих клетках канальцев понижение активности TREM-1 сопровождалось повышением маркёров, связанных с аутфагией, тогда как усиление сигнализации TREM-1 совпадало со снижением аутфагии. Одновременно активность инфламмасомы и маркёры гибели клеток менялись в противоположном направлении. Этот шаблон указывает на взаимообратную зависимость: TREM-1 и NLRP3 работают как «педаль газа» для деструктивного воспаления, а аутфагия ведёт себя скорее как «тормоз», который может уравновешивать это движение. Однако поскольку исследователи не включали и не выключали аутфагию напрямую, они отмечают, что её защитная роль, хотя и сильно предполагается, всё ещё требует подтверждения.
Что это может значить для пациентов
Для людей с сепсисом результаты имеют два ключевых последствия. Во‑первых, растворимая форма TREM-1 в крови или моче может служить ранним маркером, указывающим на активность этого повреждающего пути в почках до появления полной почечной недостаточности. Во‑вторых, препараты, ослабляющие TREM-1 или инфламмасому NLRP3, возможно, однажды смогут защитить почки от сепсис-ассоциированного повреждения, особенно у пациентов, в анализах которых видно сильную активацию этого пути. Работа рисует картину сепсис-ассоциированной почечной недостаточности как борьбы между воспалительным акселератором и внутренней системой очистки и выделяет TREM-1 как перспективную мишень для выявления пациентов высокого риска и разработки более точных терапий.
Цитирование: Liu, X., Chen, Q., Chen, X. et al. TREM1–NLRP3–driven pyroptosis in sepsis-associated acute kidney injury (AKI) with parallel autophagy changes. Sci Rep 16, 14239 (2026). https://doi.org/10.1038/s41598-026-40893-w
Ключевые слова: сепсис-ассоциированная острая почечная недостаточность, TREM-1, inflammasome NLRP3, пироптоз, аутфагия