Clear Sky Science · nl
TREM1–NLRP3–gedreven pyroptose bij sepsis-geassocieerde acute nierbeschadiging (AKI) met gelijktijdige veranderingen in autofagie
Waarom dit nierverhaal ertoe doet
Sepsis, een levensbedreigende reactie op een infectie, treft vaak als eerste de nieren en leidt jaarlijks bij miljoenen mensen tot plotseling nierfalen. Zodra de nieren falen, stijgt het sterfterisico scherp, maar artsen missen nog steeds exacte vroege waarschuwingstekens en gerichte behandelingen. Deze studie onderzoekt een recent blootgelegd kettingreactie binnen niercellen tijdens sepsis — een reactie die beschermende immuunverdedigingen kan veranderen in een zelfvernietigende storm — en vraagt of het onderbreken van deze keten zowel eerder gevaar kan signaleren als de nieren tegen ernstige schade kan beschermen.
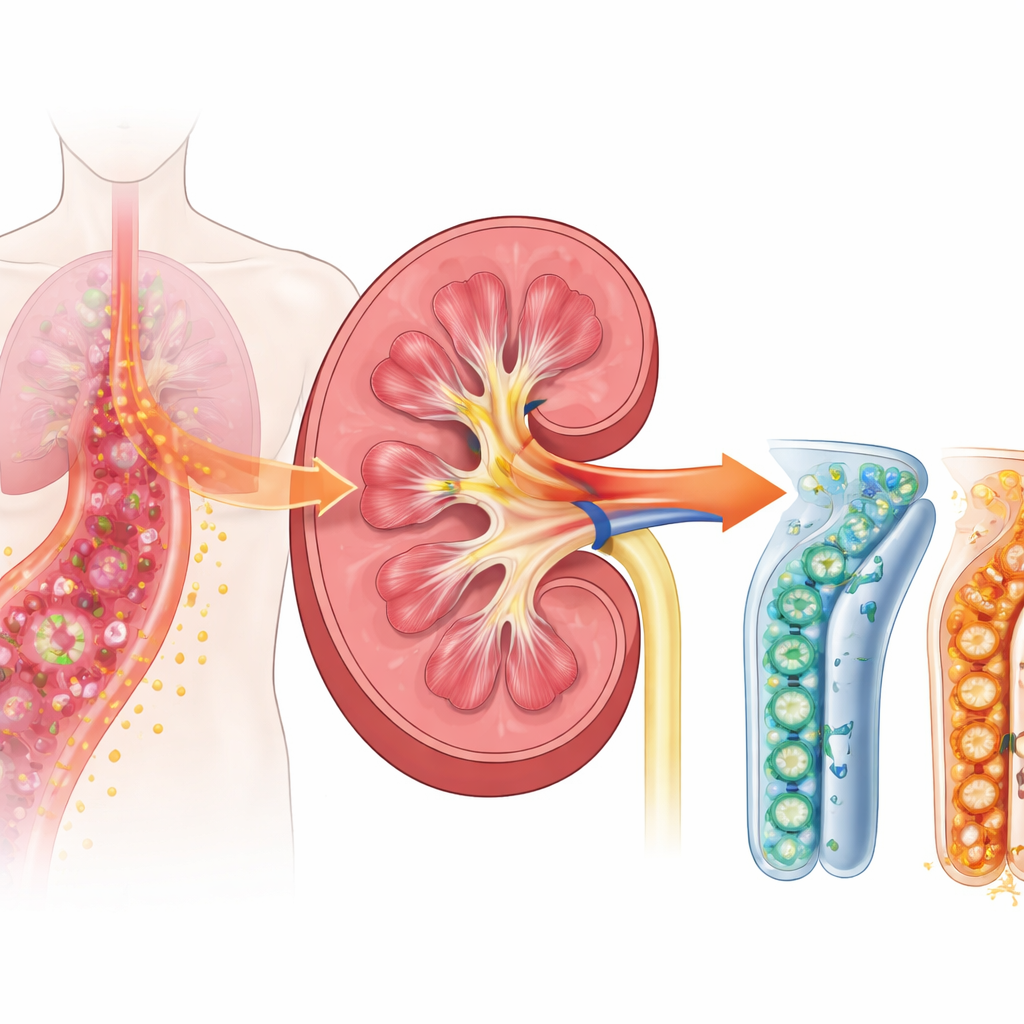
Een gevaarlijke kettingreactie bij sepsis
Wanneer sepsis zich ontwikkelt, gaat het immuunsysteem van het lichaam in overdrive om binnendringende microben te bestrijden. De nieren zijn niet alleen filters; hun tubulaire cellen helpen ook bij het waarnemen en reageren op infectie. De onderzoekers richtten zich op een oppervlaktereceptor genaamd TREM-1, die op immuuncellen zit en, zoals recenter werk suggereert, ook op tubulaire nercellen. TREM-1 werkt als een volumeknop voor ontsteking: eenmaal opgevoerd kan het alarmsignalen sterk versterken die zwelling, koorts en weefselschade aansturen. Eerdere patiëntstudies toonden aan dat een oplosbare vorm van deze receptor, afgescheiden in bloed en urine, vroeg tijdens sepsis stijgt en geassocieerd is met nierproblemen, wat suggereert dat TREM-1 een belangrijke upstream-trigger van schade kan zijn.
Van waarschuwingssignaal naar celdodend explosie
In de nier-tubulaire cellen onderzochten de onderzoekers hoe TREM-1 verbonden is met een moleculair apparaat dat het inflammasoom wordt genoemd, dat een dramatisch type celdood reguleert dat soms wordt beschreven als een cellulaire explosie. In muizen die aan een standaard sepsismodel werden blootgesteld, vonden de auteurs dat sepsis TREM-1-niveaus in de nieren en in de bloedbaan sterk verhoogde, samen met activatie van een inflammasoom gebouwd rond een eiwit genaamd NLRP3. Zodra dit complex wordt ingeschakeld, activeert het enzymen die gaten in celmembranen slaan en krachtige ontstekingsmoleculen vrijgeven, waardoor de cel gedood wordt. Dit vurige doodsprogramma, bekend als pyroptose, kan helpen bij het opruimen van infecties maar, wanneer ongecontroleerd, ook grote delen van kwetsbaar nierweefsel vernietigen.
De volumeknop terugdraaien en het pad testen
Om te zien hoe cruciaal TREM-1 is in deze ketenreactie, gebruikten de onderzoekers muizen die genetisch zo zijn gemodificeerd dat zij het Trem1-gen misten. Vergeleken met normale muizen die aan dezelfde sepsische belasting werden blootgesteld, hadden deze knockout-dieren minder structurele schade in hun nierbuizen, lagere bloedwaarden van afvalstoffen zoals creatinine en ureum, en minder ontstekingsmoleculen in hun bloed. Hun nieren toonden ook verminderde tekenen van NLRP3-inflammasoomactiviteit en pyroptotische celdood. Toen het team NLRP3 direct blokkeerde met een medicijn, verbeterde de nierbeschadiging zelfs bij normale muizen, terwijl het forceren van NLRP3-overactiviteit de schade verergerde, zelfs wanneer Trem1 ontbrak. Samen plaatsen deze experimenten TREM-1 duidelijk stroomopwaarts van NLRP3 in de schadekaskade.
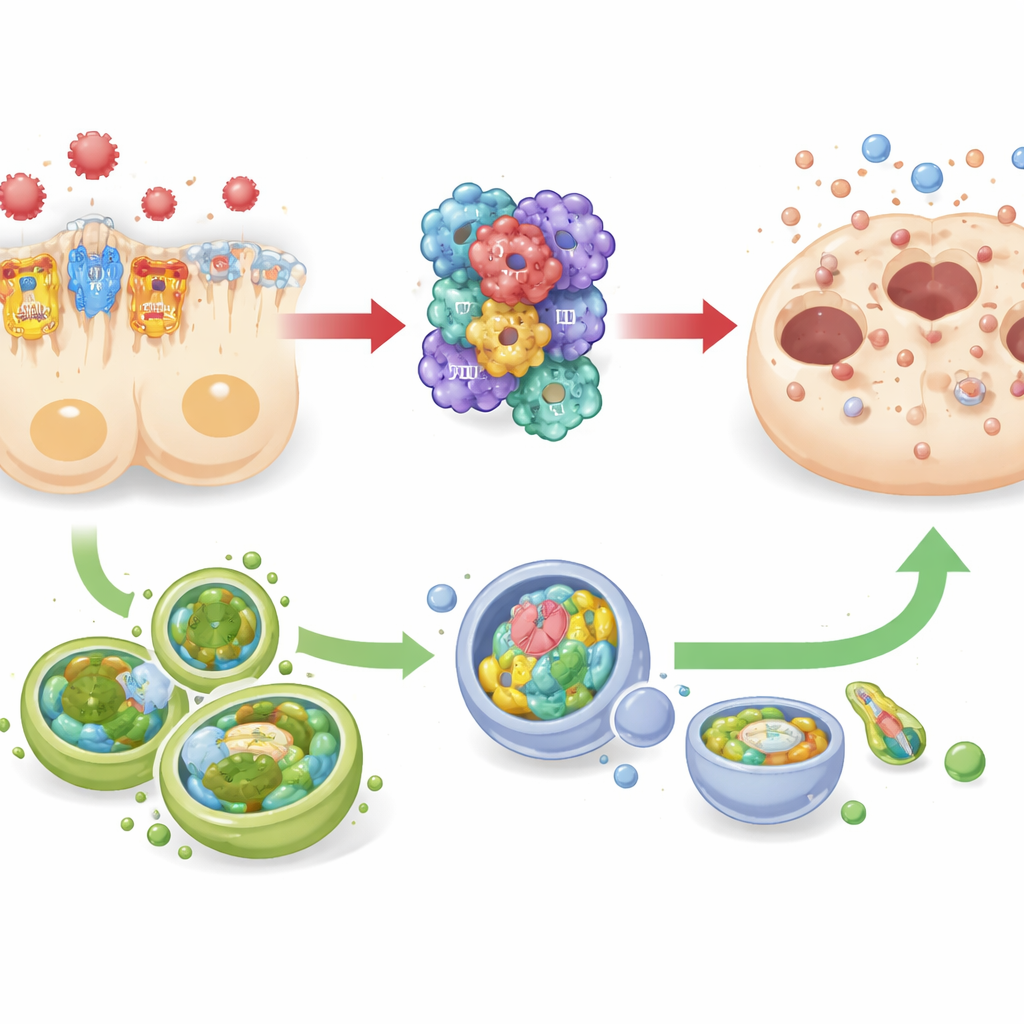
Touwtrekken met de reinigingsploeg van de cel
De studie volgde ook veranderingen in autofagie — een ingebouwd opruim- en recyclingsysteem dat cellen helpt stress te overleven door beschadigde componenten te verwijderen. In zowel sepsismuizen als menselijke nier-tubulaire cellen die in het laboratorium werden gekweekt, werd het terugdraaien van TREM-1 geassocieerd met hogere niveaus van autofagie-gerelateerde markers, terwijl sterkere TREM-1-signalen samen gingen met verminderde autofagie. Tegelijkertijd bewogen inflammasoomactiviteit en celdoodmarkers in de tegengestelde richting. Dit patroon suggereert een duw-trekrelatie: TREM-1 en NLRP3 treden samen op als het "gaspedaal" voor destructieve ontsteking, en autofagie gedraagt zich meer als een "rem" die deze aandrijving mogelijk tegenwerkt. Omdat de onderzoekers autofagie echter niet direct aan- of uitschakelden, waarschuwen ze dat de beschermende rol ervan, hoewel sterk vermoed, nog bewezen moet worden.
Wat dit voor patiënten kan betekenen
Voor mensen met sepsis hebben de bevindingen twee belangrijke implicaties. Ten eerste kan de oplosbare vorm van TREM-1 in bloed of urine dienen als een vroeg waarschuwingsmarker die aangeeft dat dit schadelijke pad in de nieren actief is voordat volledig falen optreedt. Ten tweede zouden geneesmiddelen die TREM-1 of het NLRP3-inflammasoom dempen, op den duur de nieren tegen sepsis-geassocieerde schade kunnen beschermen, vooral bij patiënten wier bloedwaarden sterke activering van dit pad laten zien. Het werk schetst sepsis-geassocieerde nierbeschadiging als een strijd tussen een inflammatoire versnellingspedaal en een intern opruimsysteem, en identificeert TREM-1 als een veelbelovend aangrijpingspunt om zowel hoogrisicopatiënten te signaleren als preciezere behandelingen te ontwerpen.
Bronvermelding: Liu, X., Chen, Q., Chen, X. et al. TREM1–NLRP3–driven pyroptosis in sepsis-associated acute kidney injury (AKI) with parallel autophagy changes. Sci Rep 16, 14239 (2026). https://doi.org/10.1038/s41598-026-40893-w
Trefwoorden: sepsis-geassocieerde acute nierbeschadiging, TREM-1, NLRP3-inflammasoom, pyroptose, autofagie