Clear Sky Science · sv
TREM1–NLRP3–driven pyroptosis in sepsis-associated acute kidney injury (AKI) with parallel autophagy changes
Varför den här njurberättelsen är viktig
Sepsis, en livshotande överreaktion mot infektion, drabbar ofta njurarna först och leder till plötslig njursvikt hos miljontals människor varje år. När njurarna sviktar ökar risken för död kraftigt, ändå saknar läkare fortfarande precisa tidiga varningssignaler och riktad behandling. Denna studie undersöker en nyligen upptäckt kedjereaktion inne i njurceller under sepsis—en process som kan förvandla skyddande immunförsvar till en självdestruktiv storm—och frågar om avbrott i denna kedja både kan ge tidigare varning och skydda njurarna från allvarlig skada.
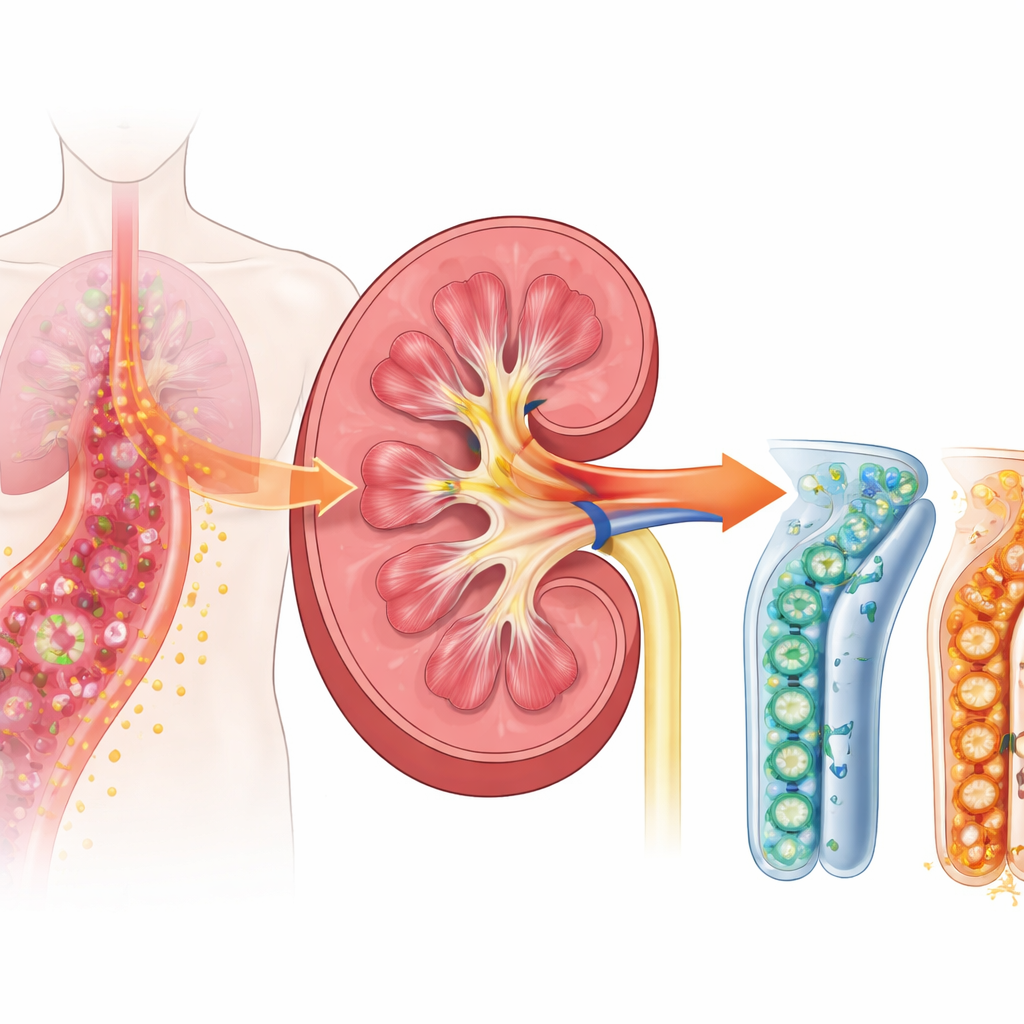
En farlig kedjereaktion vid sepsis
När sepsis utvecklas går kroppens immunsystem på högvarv för att bekämpa angripande mikrober. Njurarna är inte bara filter; deras tubulära celler hjälper också till att upptäcka och reagera på infektion. Forskarna fokuserade på en ytreceptor kallad TREM-1, som sitter på immunceller och, enligt nyare arbete, också på njurtubuliceller. TREM-1 fungerar som en volymknapp för inflammation: när den vrids upp kan den kraftigt förstärka larmsignalerna som driver svullnad, feber och vävnadsskada. Tidigare studier på patienter visade att en löslig form av denna receptor, som frigörs i blod och urin, stiger tidigt vid sepsis och är kopplad till njurproblem, vilket antyder att TREM-1 kan vara en viktig upstream‑utlösare av skada.
Från varningssignal till cellexplosion
Inne i njurtubulicellerna undersökte teamet hur TREM-1 kopplas till en molekylär maskin kallad inflammasom, som kontrollerar en dramatisk typ av celldöd som ibland beskrivs som en cellulär explosion. Hos möss som utsattes för en standardmodell för sepsis fann författarna att sepsis kraftigt ökade TREM-1-nivåerna i njurarna och i blodet, tillsammans med aktivering av ett inflammasom byggt kring ett protein kallat NLRP3. När detta komplex slås på aktiverar det enzymer som slår hål i cellmembran och frigör potenta inflammatoriska molekyler, vilket dödar cellen i processen. Detta brinnande dödsprogram, känt som pyroptos, kan hjälpa till att rensa infektion men kan, om det inte kontrolleras, också förstöra stora områden av den sköra njurvävnaden.
Att skruva ner volymknappen och testa vägen
För att se hur avgörande TREM-1 är i denna kedjereaktion använde forskarna möss som genetiskt modifierats för att sakna Trem1-genen. Jämfört med normala möss som utsattes för samma sepsisinsult hade dessa knockout‑djur mindre strukturell skada i njurtubuli, lägre blodnivåer av avfallsprodukter såsom kreatinin och urea, och färre inflammatoriska molekyler i cirkulationen. Deras njurar visade också minskade tecken på NLRP3‑inflammasomaktivitet och pyroptotisk celldöd. När teamet direkt blockerade NLRP3 med ett läkemedel förbättrades njurskadan även hos normala möss, medan att tvinga NLRP3 i överdrift förvärrade skadan även när Trem1 saknades. Tillsammans placerar dessa experiment TREM-1 tydligt upstream om NLRP3 i skadecaskaden.
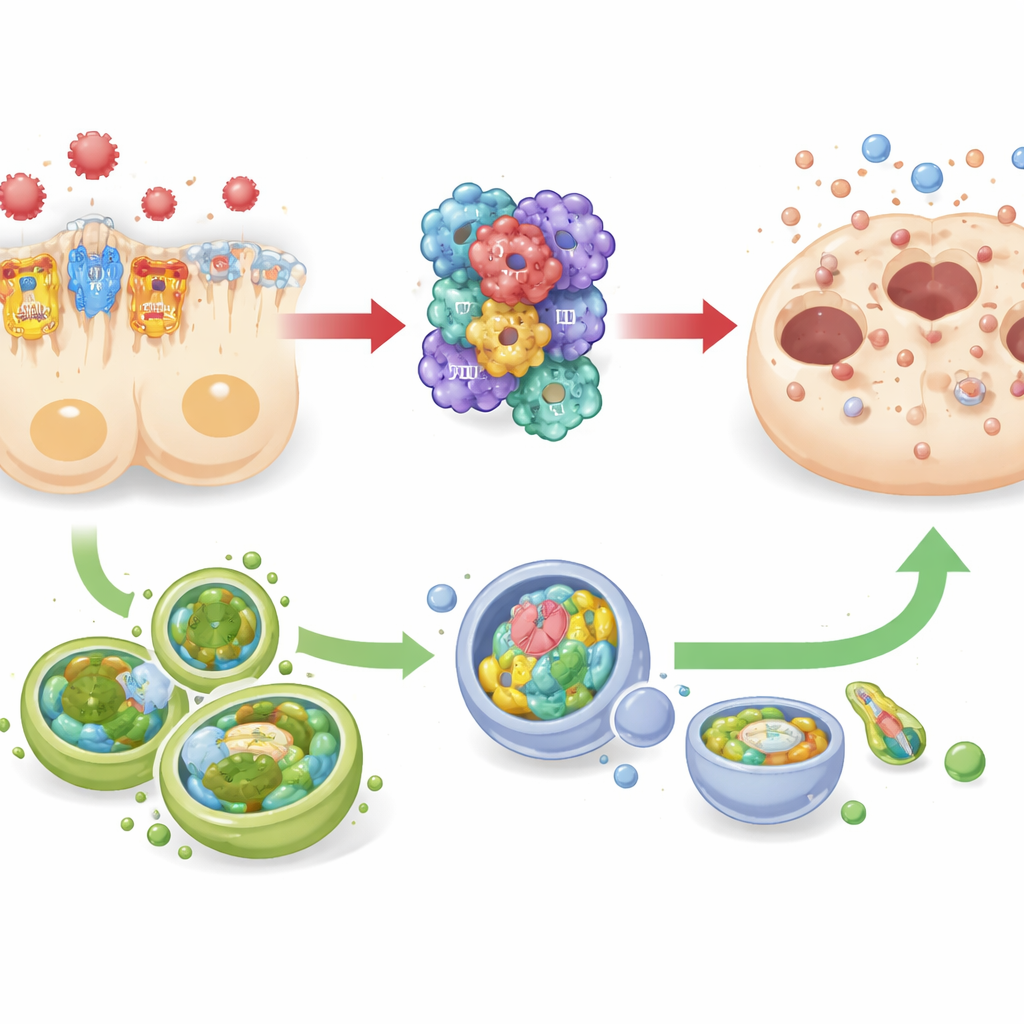
Dragkamp med cellens städpatrull
Studien följde också förändringar i autofagi—ett inbyggt städ- och återvinningssystem som hjälper celler att överleva stress genom att avlägsna skadade komponenter. Hos både septiska möss och humana njurtubuliceller odlade i labbet kopplades nedreglering av TREM-1 till högre nivåer av autofagi‑relaterade markörer, medan starkare TREM-1‑signalering sammanföll med minskad autofagi. Samtidigt rörde sig inflammasomaktivitet och celldödmarkörer i motsatt riktning. Detta mönster tyder på en tryck‑och‑drag‑relation: TREM-1 och NLRP3 agerar tillsammans som en ”gaspedal” för destruktiv inflammation, och autofagi beter sig mer som en ”broms” som kan motbalansera denna drivkraft. Eftersom forskarna dock inte direkt slog på eller av autofagi varnar de för att dess skyddande roll, även om den är starkt misstänkt, ännu inte är bevisad.
Vad detta kan betyda för patienter
För personer med sepsis har fynden två viktiga implikationer. För det första kan den lösliga formen av TREM-1 i blod eller urin fungera som en tidig varningsmarkör som visar att denna skadliga väg är aktiv i njurarna innan fullskalig svikt uppträder. För det andra kan läkemedel som dämpar TREM-1 eller NLRP3‑inflammasomet en dag skydda njurarna från sepsisrelaterad skada, särskilt hos patienter vars laboratorietester visar stark aktivering av denna väg. Arbetet målar upp en bild av sepsisassocierad njurskada som en kamp mellan en inflammatorisk accelerator och ett internt städssystem, och identifierar TREM-1 som ett lovande grepp för både att upptäcka högriskpatienter och utforma mer precisa behandlingar.
Citering: Liu, X., Chen, Q., Chen, X. et al. TREM1–NLRP3–driven pyroptosis in sepsis-associated acute kidney injury (AKI) with parallel autophagy changes. Sci Rep 16, 14239 (2026). https://doi.org/10.1038/s41598-026-40893-w
Nyckelord: sepsis-associated acute kidney injury, TREM-1, NLRP3 inflammasome, pyroptosis, autophagy