Clear Sky Science · he
פירופטוזיס מונע על ידי TREM1–NLRP3 בפגיעה כלייתית חריפה הקשורה לספסיס עם שינויים מקבילים באוטופגיה
מדוע הסיפור הכלייתי הזה חשוב
ספסיס, תגובה מסכנת חיים לזיהום, פוגע לעתים קרובות בכליות ראשית ומוביל לכשל כלייתי פתאומי במיליוני אנשים מדי שנה. ברגע שהכליות נחלשות, הסיכון למוות עולה בצורה חדה, ועדיין לרופאים חסרים איתותים מדויקים לתקופה המוקדמת וטיפולים ממוקדים. המחקר חוקר מסלול תגובתי חדש שנתגלה בתוך תאי הכליה בזמן ספסיס — מסלול שיכול להפוך את ההגנות החיסוניות למעשן משחית — ושואל האם ניתוק המסלול הזה יכול גם לאותת על סכנה מוקדם יותר וגם להגן על הכליות מפגיעה חמורה.
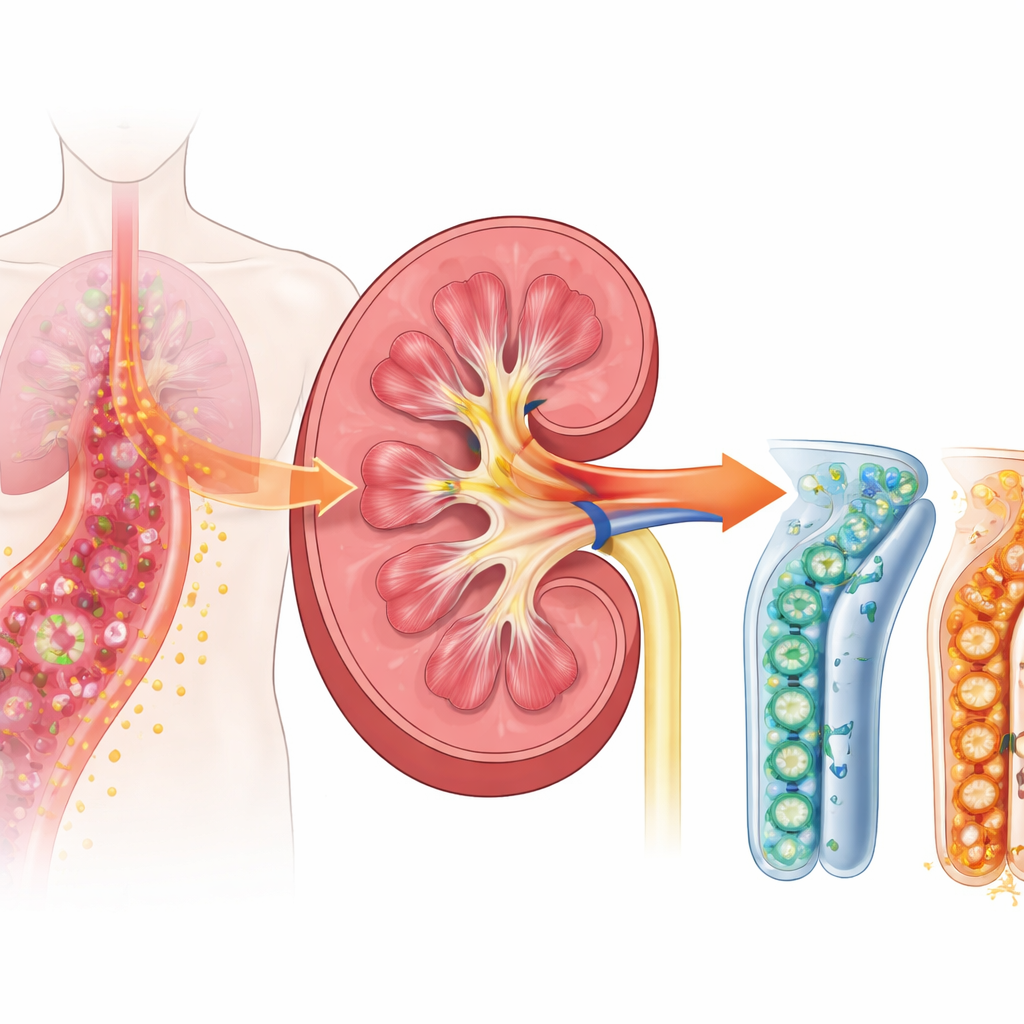
תגובה שרשרת מסוכנת בספסיס
כשמפותח ספסיס, מערכת החיסון של הגוף נכנסת להגברה כדי להילחם במיקרובים הפולשים. הכליות אינן רק מסננות; תאי הצינוריות שלהן גם עוזרים לחוש ולהגיב לזיהום. החוקרים התמקדו בקולטן ממברנה הנקרא TREM-1, שמצוי על תאי חיסון וכפי שמחקרים חדשים מרמזים, גם על תאי צינוריות כלייתיים. TREM-1 פועל כמו כפתור שליטה בעוצמת הדלקת: ברגע שמגבירים אותו, הוא יכול להעצים מאוד את אותות האזעקה שדוחפים לנפיחות, חום ופגיעה ברקמות. מחקרים קודמים בחולים הראו שצורתו המומסת של הקולטן, שמשתחררת לדם ולשתן, עולה מוקדם בספסיס וקשורה לבעיות כליה, מה שמעיד ש‑TREM-1 עשוי להיות טריגר על־זרם משמעותי של נזק.
מאותת אזהרה לפיצוץ תאי
בתוך תאי צינורית הכליה, הצוות בחן כיצד TREM-1 מתחבר למכונה מולקולרית בשם אינפלמסום, ששולטת בסוג דרמטי של מוות תאי שתיארו לעתים כ׳פיצוץ תאי׳. בעכברים שנחשפו למודל סטנדרטי של ספסיס, המחברים מצאו שספסיס הגביר בצורה בולטת את רמות ה‑TREM-1 בכליות ובמחזור הדם, יחד עם הפעלת אינפלמסום סביב חלבון בשם NLRP3. ברגע שהמערכת הזו נדלקת, היא מפעילה אנזימים שיוצרים חורים בממברנות התאים ומשחררים מולקולות דלקת חזקות, והורגת את התא בתהליך. תוכנית המוות הבוערת הזו, הידועה כפירופטוזיס, יכולה לסייע לנקות זיהום אך, כאשר אינה מבוקרת, עלולה להשמיד שטחים נרחבים של רקמת כליה עדינה.
להנמיך את עוצמת הקול ולבדוק את המסלול
כדי לבדוק עד כמה TREM-1 חשוב בשרשרת זו, החוקרים השתמשו בעכברים מהונדסים גנטית חסרי גן Trem1. בהשוואה לעכברים רגילים שנחשפו לאותו הורע ספטי, לחיות האלה היו פחות נזק מבני בצינוריות הכליה, רמות נמוכות יותר בדם של חומרים פסולת כגון קריאטינין ואוריאה, ופחות מולקולות דלקתיות במחזור הדם. בכליותיהם נצפו גם סימנים מופחתים של פעילות אינפלמסום NLRP3 ומוות תאי פירופטוטי. כאשר הצוות חסם ישירות את NLRP3 בעזרת תרופה, פגיעת הכליה השתפרה גם בעכברים רגילים, בעוד שהפעלת-יתר של NLRP3 החמיר את הנזק אפילו כאשר Trem1 נעדר. יחד, הניסויים הללו מציבים את TREM-1 בבירור מקומי לפני NLRP3 במפל הפגיעה.
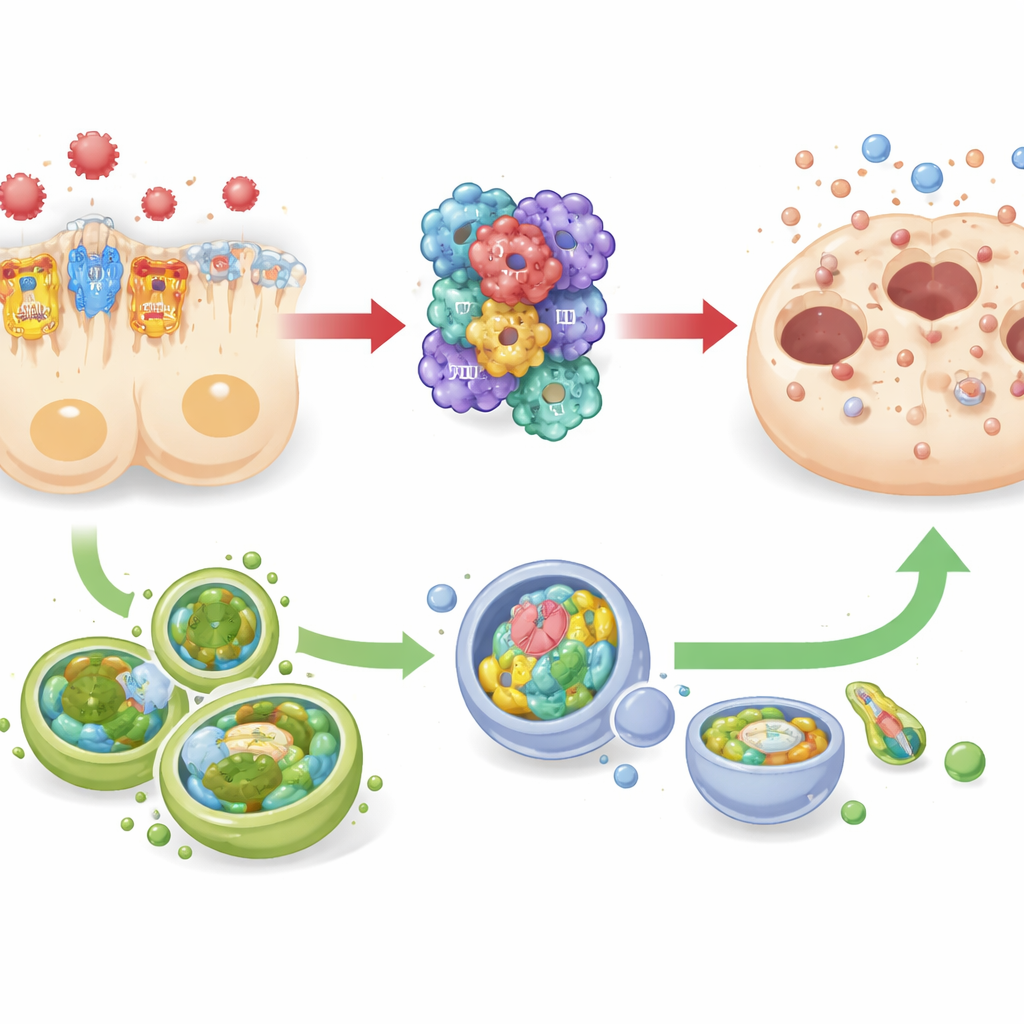
מאבק כוח מול צוות הניקיון התאי
המחקר גם עקב אחרי שינויים באוטופגיה — מערכת ניקיון ומיחזור פנימית שעוזרת לתאים לשרוד מתח על‑ידי הסרת רכיבים פגומים. גם בעכברים ספטיים וגם בתאי צינורית כלייתיים אנושיים אשר גודלו במעבדה, הפחתת פעילות TREM-1 נקשרה לרמות גבוהות יותר של סמני אוטופגיה, בעוד שאותות TREM-1 חזקים יותר לוּוּ בעיכוב האוטופגיה. במקביל, פעילות האינפלמסום וסימני המוות התאי נעו בכיוון ההפוך. דפוס זה מצביע על יחסי דחיפה־משיכה: TREM-1 ו‑NLRP3 פועלים יחד כ׳דוושת גז׳ לדלקת משחיתה, ואילו האוטופגיה מתנהגת יותר כמו ׳בלם׳ שעשוי לנטרל את המניע הזה. עם זאת, מאחר שהחוקרים לא הפעלו או כיבו את האוטופגיה ישירות, הם הזהירו שתפקידה המגן, אף על פי שמחשדים חזקים תומכים בכך, טרם הוכח סופית.
מה המשמעות עבור חולים
לאנשים עם ספסיס הממצאים נושאים שתי השלכות מרכזיות. ראשית, הצורה המומסת של TREM-1 בדם או בשתן עשויה לשמש כסמן אזהרה מוקדם שמצביע על כך שהמסלול המזיק פעיל בכליות לפני שהכשל המלא מתגלה. שנית, תרופות שמרגיעות את TREM-1 או את אינפלמסום NLRP3 עשויות בעתיד להגן על הכליות מפגיעה הקשורה לספסיס, במיוחד בחולים שבבדיקות המעבדה שלהם נראית הפעלת-יתר של המסלול הזה. העבודה מציירת תמונה של פגיעה כלייתית קשורה לספסיס כקרב בין מאיצת דלקת לבין מערכת ניקוי פנימית, ומזהה את TREM-1 כידית מבטיחה הן לזיהוי חולים בסיכון גבוה והן לעיצוב טיפולים מדויקים יותר.
ציטוט: Liu, X., Chen, Q., Chen, X. et al. TREM1–NLRP3–driven pyroptosis in sepsis-associated acute kidney injury (AKI) with parallel autophagy changes. Sci Rep 16, 14239 (2026). https://doi.org/10.1038/s41598-026-40893-w
מילות מפתח: פגיעה כלייתית חריפה הקשורה לספסיס, TREM-1, אינפלמסום NLRP3, פירופטוזיס, אוטופגיה