Clear Sky Science · pl
Pyroptoza napędzana przez TREM1–NLRP3 w sepsie związanej z ostrą niewydolnością nerek (AKI) wraz z równoległymi zmianami autofagii
Dlaczego ta historia nerek ma znaczenie
Sepsa, zagrażająca życiu reakcja na infekcję, często uderza najpierw w nerki, prowadząc do nagłej ich niewydolności u milionów ludzi rocznie. Gdy nerki zawodzą, ryzyko śmierci gwałtownie wzrasta, a lekarzom nadal brakuje precyzyjnych wczesnych sygnałów ostrzegawczych i ukierunkowanych terapii. Niniejsze badanie bada nowo odkryty łańcuch reakcji w komórkach nerkowych podczas sepsy — taki, który może przemienić ochronne mechanizmy odpornościowe w samodestrukcyjną burzę — i pyta, czy przerwanie tego łańcucha mogłoby zarówno wcześniej sygnalizować niebezpieczeństwo, jak i chronić nerki przed ciężkim uszkodzeniem.
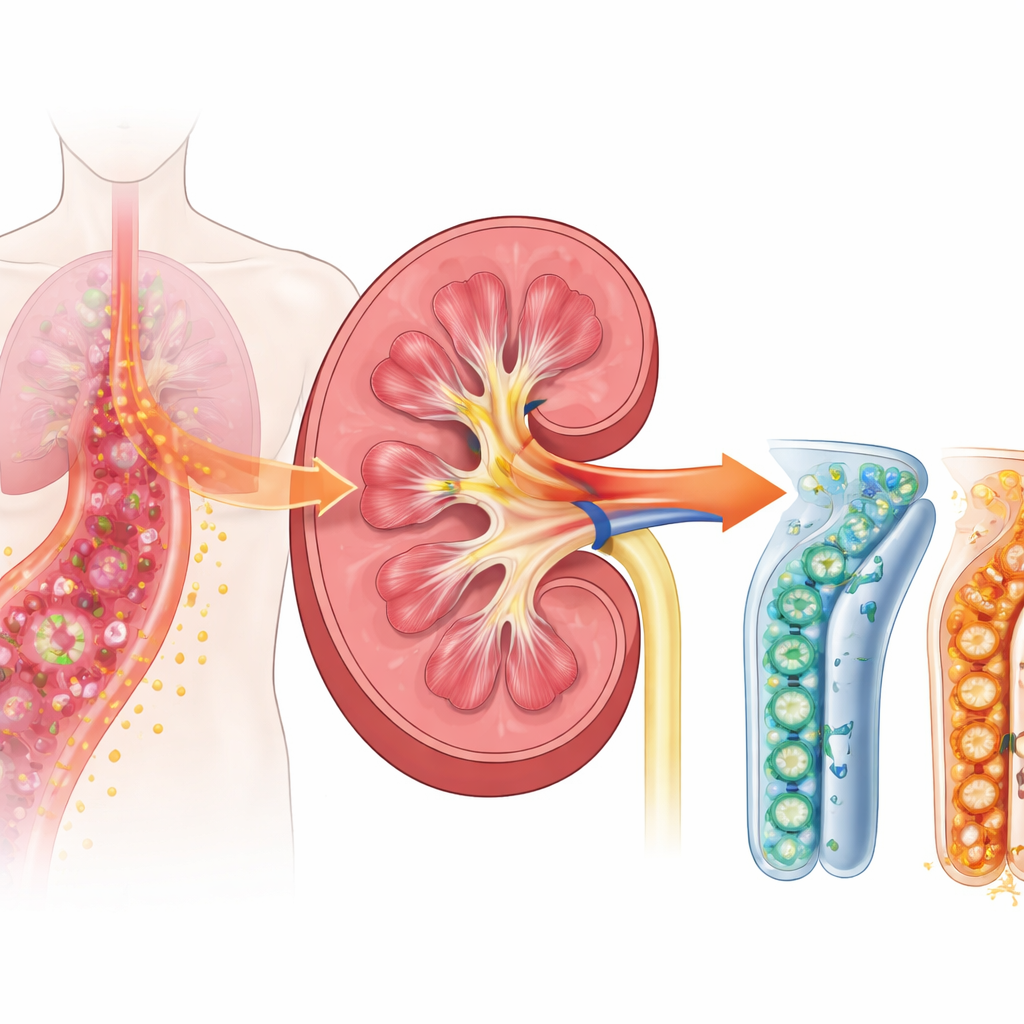
Niebezpieczny łańcuch reakcji w sepsie
Gdy rozwija się sepsa, układ odpornościowy organizmu przełącza się na tryb nadmiernej odpowiedzi, by zwalczać najeźdźcze drobnoustroje. Nerki nie są jedynie filtrami; ich komórki cewek nerkowych także pomagają wykrywać i reagować na infekcję. Badacze skupili się na receptorze powierzchniowym zwanym TREM-1, występującym na komórkach odpornościowych, a jak nowe prace sugerują — także na komórkach cewek nerkowych. TREM-1 działa jak pokrętło głośności dla zapalenia: po jego podkręceniu może znacząco wzmocnić sygnały alarmowe wywołujące obrzęk, gorączkę i uszkodzenie tkanek. Wcześniejsze badania u pacjentów wykazały, że rozpuszczalna forma tego receptora, uwalniana do krwi i moczu, pojawia się wcześnie w sepsie i wiąże się z problemami nerkowymi, co sugeruje, że TREM-1 może być istotnym wczesnym wyzwalaczem uszkodzeń.
Od sygnału ostrzegawczego do eksplozji komórki
Wewnątrz komórek cewek nerkowych zespół badał, jak TREM-1 łączy się z maszyną molekularną zwaną inflammasomem, która rządzi dramatycznym typem śmierci komórkowej czasem opisywanym jako eksplozja komórkowa. U myszy poddanych standardowemu modelowi sepsy autorzy stwierdzili, że sepsa wyraźnie zwiększa poziomy TREM-1 w nerkach i we krwi, równocześnie aktywując inflammasom zbudowany wokół białka NLRP3. Po włączeniu ten kompleks aktywuje enzymy, które tworzą dziury w błonach komórkowych i uwalniają silne molekuły zapalne, zabijając komórkę w tym procesie. Ten płomienny program śmierci, znany jako pyroptoza, może pomagać w eliminacji infekcji, ale jeśli pozostanie niepowstrzymany, może też zniszczyć duże obszary delikatnej tkanki nerkowej.
Przyciszanie pokrętła i testowanie ścieżki
Aby sprawdzić, jak kluczowy jest TREM-1 w tym łańcuchu reakcji, badacze użyli myszy genetycznie zmodyfikowanych w celu braku genu Trem1. W porównaniu z normalnymi myszami poddanymi temu samemu septycznemu urazowi, zwierzęta-z „knockoutami” miały mniejsze uszkodzenia strukturalne cewek nerkowych, niższe poziomy we krwi produktów przemiany materii, takich jak kreatynina i mocznik, oraz mniej krążących molekuł zapalnych. Ich nerki wykazywały też zmniejszone oznaki aktywności inflammasomu NLRP3 i śmierci komórkowej typu pyroptozy. Gdy zespół bezpośrednio zablokował NLRP3 lekiem, uraz nerek poprawił się nawet u normalnych myszy, natomiast wymuszenie nadmiernej aktywności NLRP3 pogorszyło uszkodzenia nawet przy braku Trem1. Razem te eksperymenty umieszczają TREM-1 wyraźnie powyżej NLRP3 w kaskadzie uszkodzeń.
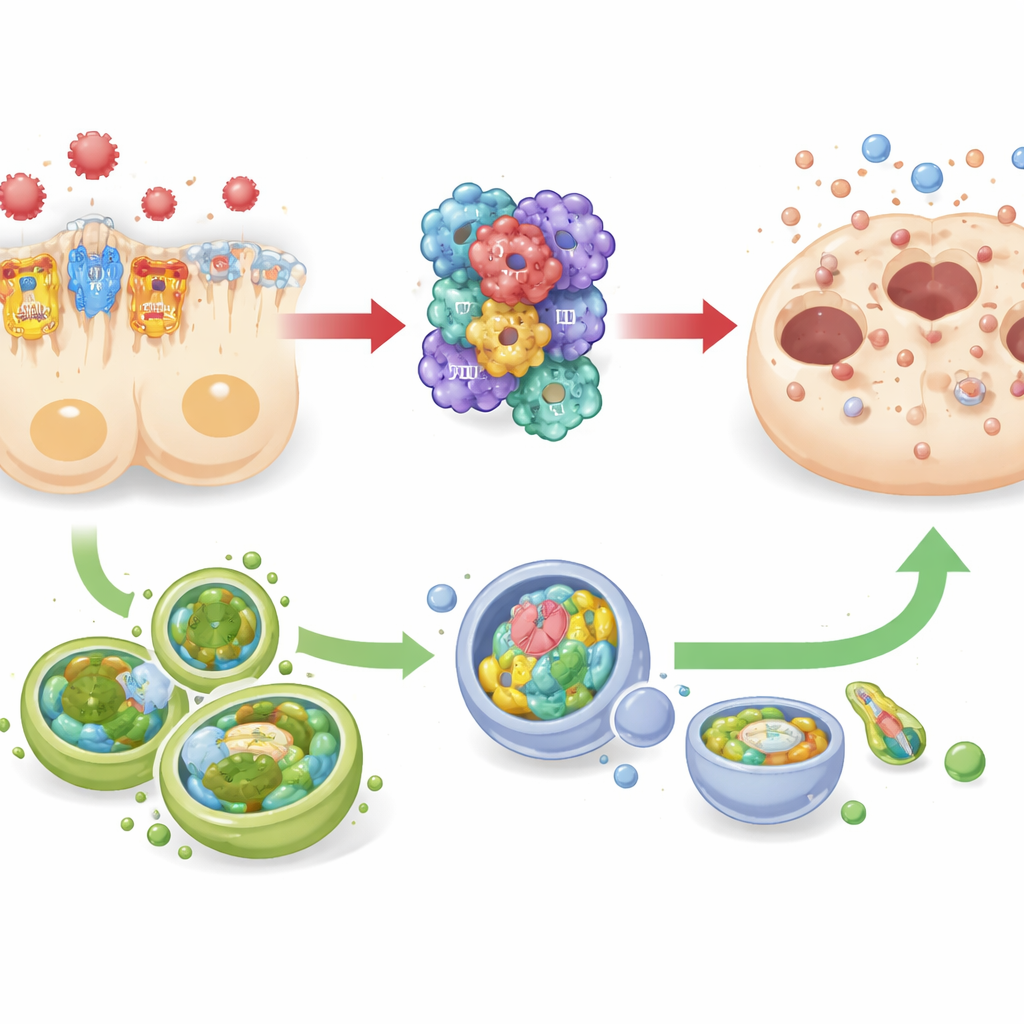
Przeciąganie liny z komórkowym zespołem sprzątającym
Badanie śledziło także zmiany w autofagii — wrodzonym systemie sprzątania i recyklingu, który pomaga komórkom przetrwać stres poprzez usuwanie uszkodzonych składników. Zarówno u septycznych myszy, jak i w ludzkich komórkach cewek nerkowych hodowanych w laboratorium, przyciszenie TREM-1 wiązało się z wyższymi poziomami markerów związanych z autofagią, podczas gdy silniejszy sygnał TREM-1 pokrywał się z obniżoną autofagią. Jednocześnie aktywność inflammasomu i markery śmierci komórkowej poruszały się w przeciwnym kierunku. Ten wzorzec sugeruje relację naprzemienną: TREM-1 i NLRP3 działające razem jak „pedał gazu” dla destrukcyjnego stanu zapalnego, a autofagia zachowująca się bardziej jak „hamulec”, który może przeciwdziałać temu napędowi. Jednak ponieważ badacze nie włączali ani nie wyłączali bezpośrednio autofagii, zastrzegają, że jej rola ochronna, chociaż jest silnie podejrzewana, pozostaje do udowodnienia.
Co to może znaczyć dla pacjentów
Dla osób z sepsą wyniki mają dwa kluczowe implikacje. Po pierwsze, rozpuszczalna forma TREM-1 we krwi lub moczu może służyć jako wczesny marker ostrzegawczy, wskazujący, że ta szkodliwa ścieżka jest aktywna w nerkach zanim rozwinie się pełna niewydolność. Po drugie, leki tłumiące TREM-1 lub inflammasom NLRP3 mogłyby pewnego dnia chronić nerki przed uszkodzeniem związanym z sepsą, szczególnie u pacjentów, których badania laboratoryjne wykazują silną aktywację tej drogi. Praca kreśli obraz uszkodzenia nerek w sepsie jako walki między zapalnym przyspieszaczem a wewnętrznym systemem sprzątającym, i identyfikuje TREM-1 jako obiecujący punkt uchwytu zarówno do wykrywania pacjentów wysokiego ryzyka, jak i do projektowania bardziej precyzyjnych terapii.
Cytowanie: Liu, X., Chen, Q., Chen, X. et al. TREM1–NLRP3–driven pyroptosis in sepsis-associated acute kidney injury (AKI) with parallel autophagy changes. Sci Rep 16, 14239 (2026). https://doi.org/10.1038/s41598-026-40893-w
Słowa kluczowe: sepsa związana z ostrą niewydolnością nerek, TREM-1, inflammasom NLRP3, pyroptoza, autofagia