Clear Sky Science · tr
Sepsis ilişkili akut böbrek hasarında (AKI) TREM1–NLRP3 kaynaklı piroptozis ve eşzamanlı otofaji değişiklikleri
Bu böbrek öyküsü neden önemli
Enfeksiyona karşı hayatı tehdit eden bir yanıt olan sepsis, sıklıkla böbrekleri ilk hedef alır ve her yıl milyonlarca insanda ani böbrek yetmezliğine yol açar. Böbrekler işlevini yitirdiğinde ölüm riski keskin biçimde artar; buna rağmen hekimlerin erken uyarı sinyalleri ve hedefe yönelik tedavileri hâlâ sınırlıdır. Bu çalışma, sepsis sırasında böbrek hücrelerinde keşfedilen yeni bir zincir reaksiyonunu inceliyor—koruyucu bağışıklık tepkilerini kendi kendini yok eden bir fırtınaya dönüştürebilen bir süreci—ve bu zinciri kesmenin hem tehlikeyi daha erken ortaya çıkarıp çıkaramayacağını hem de böbrekleri ağır hasardan koruyup koruyamayacağını sorguluyor.
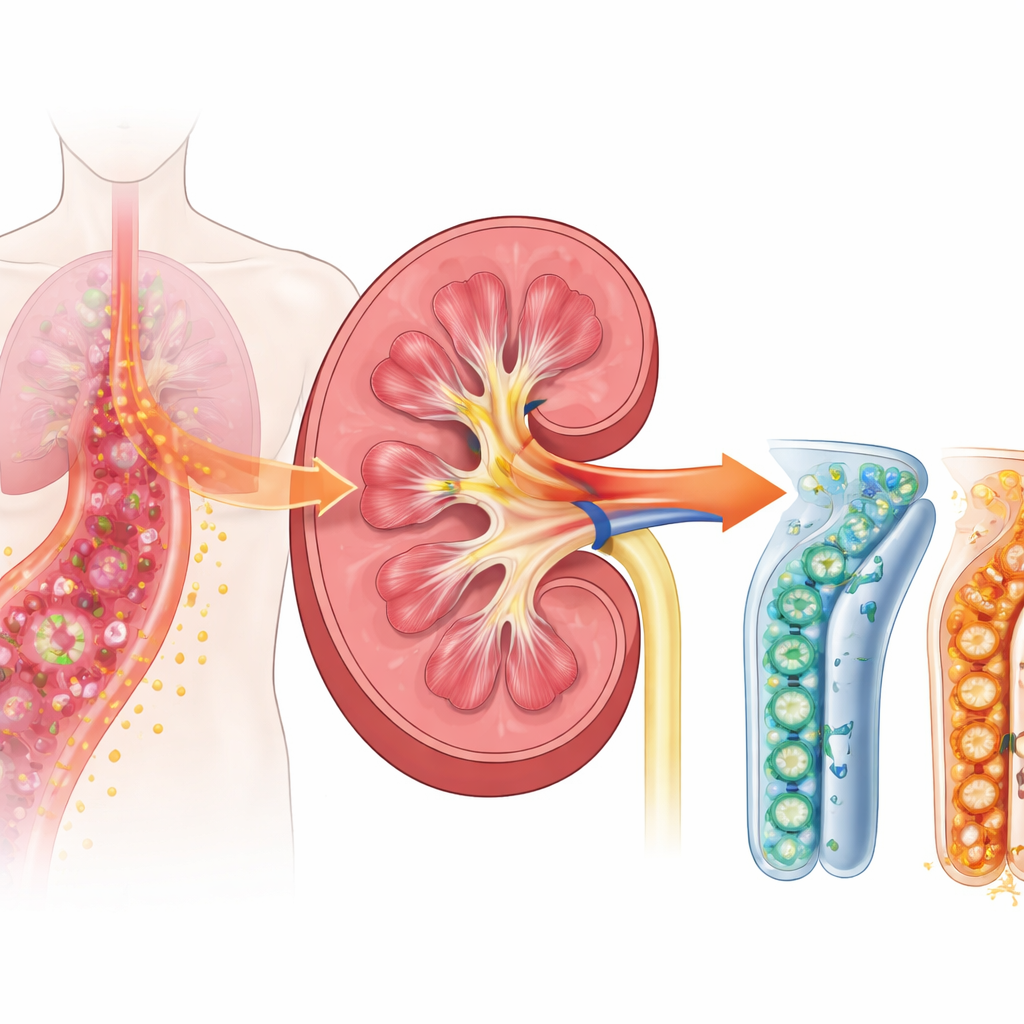
Sepsiste tehlikeli bir zincir reaksiyonu
Sepsis geliştiğinde vücudun bağışıklık sistemi istilacı mikroplarla mücadele etmek için aşırı düzeye çıkar. Böbrekler yalnızca filtreler değildir; tübüler hücreleri de enfeksiyonu algılamaya ve yanıt vermeye yardımcı olur. Araştırmacılar, bağışıklık hücrelerinin üzerinde ve yeni çalışmaların işaret ettiği üzere böbrek tübül hücrelerinde de bulunan TREM-1 adında bir yüzey reseptörüne odaklandı. TREM-1, iltihap için bir ses düğmesi gibi davranır: açıldığında, şişlik, ateş ve doku hasarını tetikleyen alarm sinyallerini büyük ölçüde güçlendirebilir. Daha önceki hasta çalışmaları, bu reseptörün çözünebilir bir formunun kana ve idrara erken dönemde karıştığını ve böbrek sorunlarıyla ilişkili olduğunu göstererek TREM-1’in hasarın önemli bir yukarı akış tetikleyicisi olabileceğini ima etmişti.
Uyarı sinyalinden hücresel patlamaya
Böbrek tübül hücrelerinin içinde ekip, TREM-1’in inflammasom adı verilen ve bazen hücresel patlama olarak tanımlanan dramatik bir hücre ölümü türünü yöneten moleküler makineyle nasıl bağlandığını inceledi. Standart bir sepsis modeline maruz kalan farelerde, yazarlar sepsisin böbreklerde ve kan dolaşımında TREM-1 düzeylerini keskin biçimde artırdığını ve NLRP3 adlı bir protein etrafında kurulu inflammasomun etkinleştiğini buldular. Bir kez aktifleştiğinde bu kompleks, hücre zarlarında delikler açan ve güçlü inflamatuar molekülleri salan enzimleri etkinleştirir; bu süreçte hücre öldürülür. Piroptozis olarak bilinen bu ateşli ölüm programı enfeksiyonun temizlenmesine yardımcı olabilir, ancak kontrolsüz kaldığında hassas böbrek dokusunun geniş bölgelerini yok edebilir.
Ses düğmesini kısmak ve yolak üzerinde sınamalar
Bu zincir reaksiyonunda TREM-1’in ne kadar kritik olduğunu görmek için araştırmacılar Trem1 geninden yoksun olacak şekilde genetik olarak değiştirilmiş fareler kullandılar. Aynı septik saldırıya maruz kalan normal farelerle karşılaştırıldığında, bu gen kesme hayvanlarında tübüllerde daha az yapısal hasar, kreatinin ve üre gibi atık ürünlerin kanda daha düşük düzeyleri ve dolaşımdaki daha az inflamatuar molekül görüldü. Ayrıca böbreklerinde NLRP3 inflammasom aktivitesi ve piroptotik hücre ölümü belirtileri azalmıştı. Ekip doğrudan bir ilaçla NLRP3’ü bloke ettiğinde böbrek hasarı normal farelerde bile iyileşti; oysa NLRP3’ü aşırı aktive etmek, Trem1 eksik olsa bile hasarı kötüleştirdi. Bu deneylerin tümü, bu hasar kaskadında TREM-1’i açıkça NLRP3’ün yukarısında konumlandırıyor.
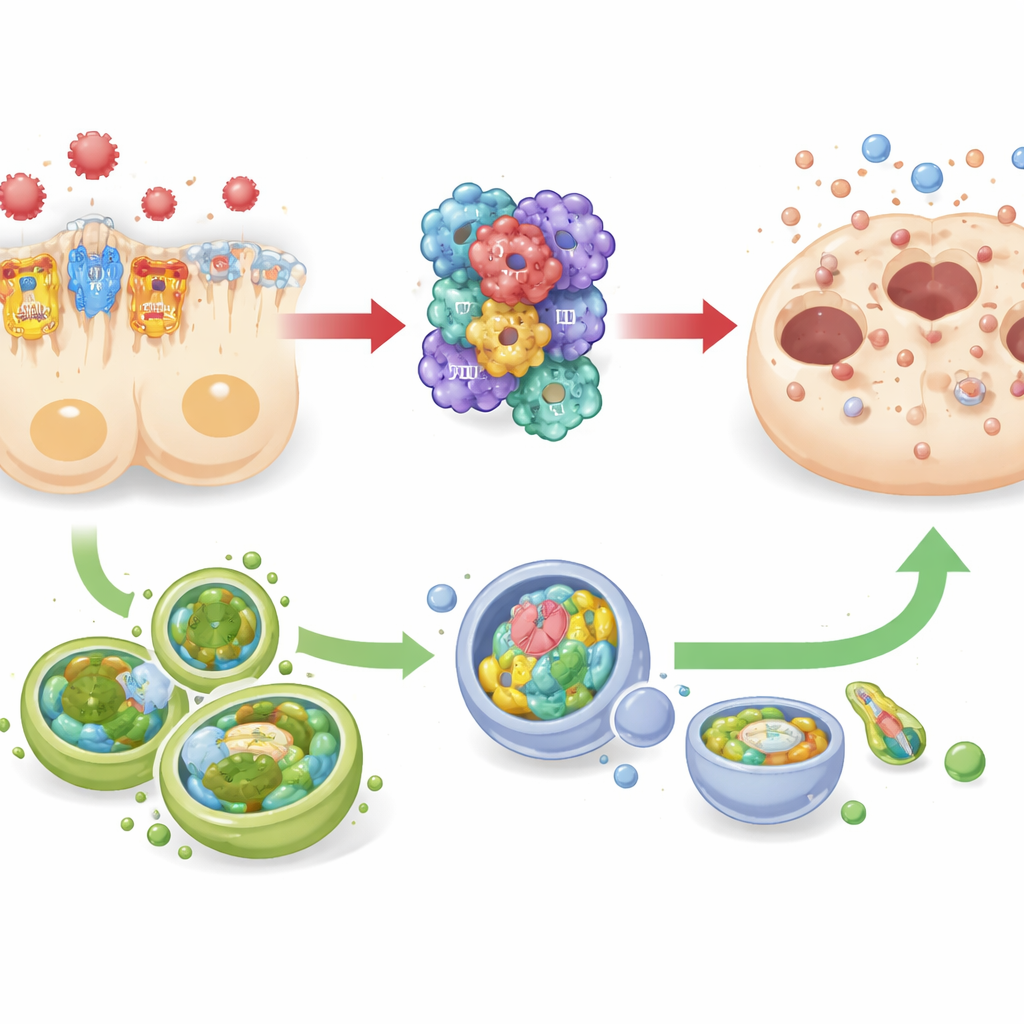
Hücresel temizlik ekibiyle bir çekişme
Çalışma ayrıca hücrelerin stresle başa çıkmasına yardımcı olmak için hasarlı bileşenleri uzaklaştıran yerleşik temizlik ve geri dönüşüm sistemi olan otofajideki değişiklikleri izledi. Hem septik farelerde hem de laboratuvarda büyütülen insan böbrek tübül hücrelerinde TREM-1’in kısılması, otofajiyle ilişkili belirteçlerin daha yüksek seviyeleriyle ilişkilendirildi; güçlü TREM-1 sinyali ise otofajide azalma ile örtüştü. Aynı zamanda inflammasom aktivitesi ve hücre ölümü belirteçleri zıt yönde hareket etti. Bu desen, TREM-1 ve NLRP3’ün birlikte yıkıcı iltihap için bir “gaz pedalı” gibi, otofajinin ise bu sürüşü dengeleyebilecek bir “fren” gibi davrandığını düşündürüyor. Ancak araştırmacılar otofajiyi doğrudan açıp kapatmadıkları için, koruyucu rolünün kuvvetle şüphelenilse de henüz kanıtlanmadığını belirtiyorlar.
Bu hastalar için ne anlama gelebilir
Sepsisli hastalar için bulguların iki önemli çıkarımı var. Birincisi, kandaki veya idrardaki çözünebilir TREM-1 formu, bu yıkıcı yolun böbreklerde tam yetmezlik ortaya çıkmadan önce aktif olduğunu gösteren erken bir uyarı işareti olarak kullanılabilir. İkincisi, TREM-1’i veya NLRP3 inflammasomunu baskılayan ilaçlar, bir gün özellikle bu yolun güçlü aktivasyonunu gösteren hastalarda sepsis kaynaklı böbrek hasarını önleyebilir. Çalışma, sepsis ilişkili böbrek hasarını iltihap hızlandırıcısı ile hücre içi temizlik sistemi arasındaki bir mücadele olarak resmediyor ve yüksek riskli hastaları tespit etmek ile daha doğru tedaviler tasarlamak için TREM-1’i umut vaat eden bir hedef olarak tanımlıyor.
Atıf: Liu, X., Chen, Q., Chen, X. et al. TREM1–NLRP3–driven pyroptosis in sepsis-associated acute kidney injury (AKI) with parallel autophagy changes. Sci Rep 16, 14239 (2026). https://doi.org/10.1038/s41598-026-40893-w
Anahtar kelimeler: sepsis ilişkili akut böbrek hasarı, TREM-1, NLRP3 inflammasomu, piroptozis, otofaji