Clear Sky Science · pt
Piroptose dirigida por TREM1–NLRP3 na lesão renal aguda associada à sepse (LRA) com alterações paralelas na autofagia
Por que esta história dos rins importa
A sepse, uma reação à infecção que pode pôr a vida em risco, muitas vezes atinge os rins primeiro, causando insuficiência renal aguda em milhões de pessoas todos os anos. Quando os rins falham, o risco de morte aumenta de forma acentuada, e ainda faltam aos médicos sinais precoces precisos e tratamentos direcionados. Este estudo explora uma cadeia de reações recém-descoberta dentro das células renais durante a sepse — uma cadeia que pode transformar defesas imunes protetoras em uma tempestade autodestrutiva — e investiga se interromper essa sequência poderia tanto sinalizar o perigo mais cedo quanto proteger os rins de danos severos.
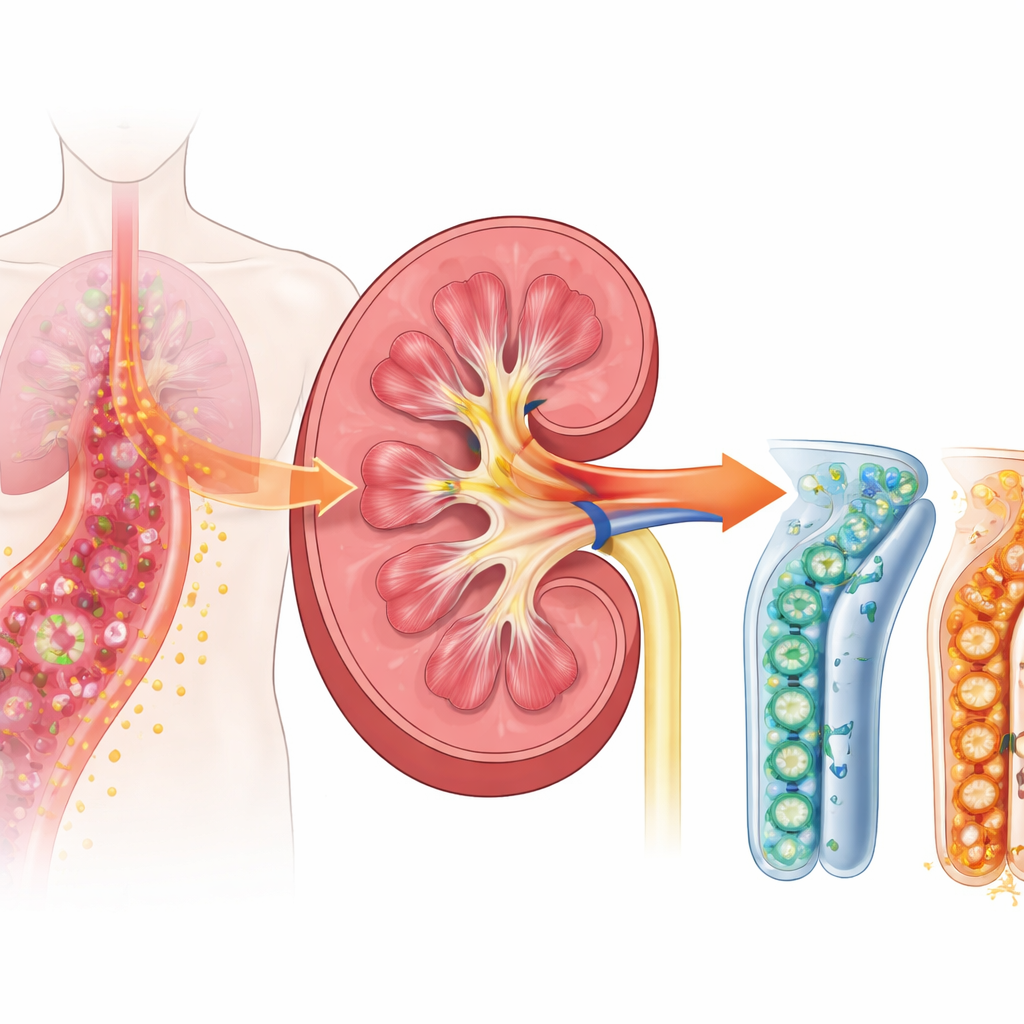
Uma reação em cadeia perigosa na sepse
Quando a sepse se instala, o sistema imunológico entra em excesso de atividade para combater microrganismos invasores. Os rins não são apenas filtros; as células dos túbulos renais também ajudam a detectar e responder à infecção. Os pesquisadores concentraram-se em um receptor de superfície chamado TREM-1, que fica em células imunes e, como trabalhos mais recentes sugerem, também em células dos túbulos renais. O TREM-1 age como um controle de volume para a inflamação: uma vez aumentado, pode amplificar fortemente os sinais de alarme que provocam inchaço, febre e lesão tecidual. Estudos prévios em pacientes mostraram que uma forma solúvel desse receptor, liberada no sangue e na urina, aumenta precocemente na sepse e se associa a problemas renais, sugerindo que o TREM-1 pode ser um gatilho importante e a montante do dano.
Do sinal de alerta à explosão celular
No interior das células dos túbulos renais, a equipe examinou como o TREM-1 se conecta a uma máquina molecular chamada inflamassoma, que controla um tipo dramático de morte celular às vezes descrito como explosão celular. Em camundongos submetidos a um modelo padrão de sepse, os autores observaram que a sepse aumentou fortemente os níveis de TREM-1 nos rins e na corrente sanguínea, juntamente com a ativação de um inflamassoma centrado em uma proteína chamada NLRP3. Uma vez ativado, esse complexo dispara enzimas que fazem furos nas membranas celulares e liberam moléculas inflamatórias potentes, matando a célula no processo. Esse programa de morte inflamatória, conhecido como piroptose, pode ajudar a eliminar a infecção, mas, quando descontrolado, também pode destruir grandes áreas de tecido renal frágil.
Abaixando o volume e testando a via
Para avaliar a importância do TREM-1 nessa reação em cadeia, os pesquisadores usaram camundongos geneticamente modificados sem o gene Trem1. Comparados a camundongos normais submetidos ao mesmo insulto séptico, esses animais knockout apresentaram menos dano estrutural nos túbulos renais, níveis sanguíneos mais baixos de resíduos como creatinina e ureia, e menos moléculas inflamatórias circulando no sangue. Seus rins também mostraram sinais reduzidos de atividade do inflamassoma NLRP3 e de morte celular por piroptose. Quando a equipe bloqueou diretamente o NLRP3 com um fármaco, a lesão renal melhorou mesmo em camundongos normais, ao passo que forçar a hiperativação do NLRP3 agravou o dano mesmo na ausência do Trem1. Juntos, esses experimentos posicionam o TREM-1 claramente a montante do NLRP3 na cascata de lesão.
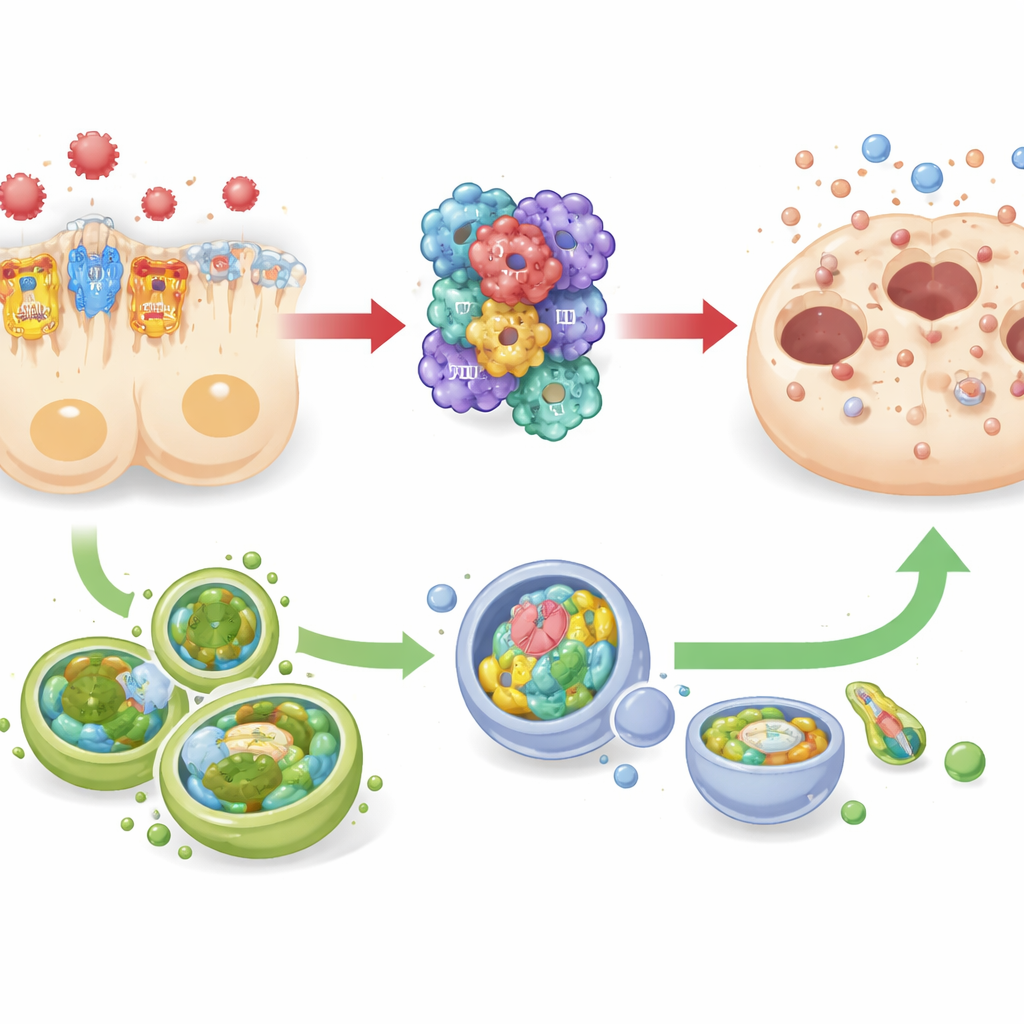
Uma disputa com a equipe de limpeza celular
O estudo também acompanhou alterações na autofagia — um sistema interno de limpeza e reciclagem que ajuda as células a sobreviver ao estresse removendo componentes danificados. Tanto em camundongos sépticos quanto em células de túbulos renais humanos cultivadas em laboratório, a redução do TREM-1 relacionou-se com níveis mais altos de marcadores associados à autofagia, enquanto sinalização mais forte do TREM-1 coincidia com diminuição da autofagia. Ao mesmo tempo, a atividade do inflamassoma e os marcadores de morte celular moveram-se na direção oposta. Esse padrão sugere uma relação de empurra-puxa: TREM-1 e NLRP3 atuando juntos como um “acelerador” para a inflamação destrutiva, e a autofagia comportando-se mais como um “freio” que pode contrabalançar essa aceleração. Contudo, como os pesquisadores não ativaram ou desativaram diretamente a autofagia, eles alertam que seu papel protetor, embora fortemente suspeito, ainda precisa ser comprovado.
O que isso pode significar para pacientes
Para pessoas com sepse, os achados têm duas implicações principais. Primeiro, a forma solúvel do TREM-1 no sangue ou na urina pode servir como um marcador de alerta precoce indicando que essa via danosa está ativa nos rins antes que uma falência total apareça. Segundo, fármacos que atenuem o TREM-1 ou o inflamassoma NLRP3 podem um dia proteger os rins da lesão relacionada à sepse, especialmente em pacientes cujos exames laboratoriais mostram forte ativação dessa via. O trabalho pinta um quadro da lesão renal associada à sepse como uma batalha entre um acelerador inflamatório e um sistema interno de limpeza, e identifica o TREM-1 como uma alça promissora tanto para identificar pacientes de alto risco quanto para projetar tratamentos mais precisos.
Citação: Liu, X., Chen, Q., Chen, X. et al. TREM1–NLRP3–driven pyroptosis in sepsis-associated acute kidney injury (AKI) with parallel autophagy changes. Sci Rep 16, 14239 (2026). https://doi.org/10.1038/s41598-026-40893-w
Palavras-chave: lesão renal aguda associada à sepse, TREM-1, inflamassoma NLRP3, piroptose, autofagia